I. Preambolo
Alcuni di voi potrebbero essersi già imbattuti nell’articolo di Chest Rockwell intitolato “The Science of Trenbolone” il quale si trova da qualche tempo su alcuni siti dedicati al BodyBuilding. L’intento dell’autore è stato quello di creare un articolo approfondito sul Trenbolone. Tale articolo è stato progettato per essere una guida di riferimento rapida volta a rispondere a molte domande riguardanti questo AAS. La mole di informazioni presenti in esso ha reso questo articolo un punto di riferimento per comprendere le caratteristiche e le potenziali applicazioni del Trenbolone. Il mio intento è quello di realizzare una “guida” sul Trenbolone, sul modello di quella realizzata da Chest Rockwell, in grado di fornire una serie di importanti informazioni riguardanti questo AAS e utilizzabili da atleti e preparatori.
II. Introduzione

Il Trenbolone è senza dubbio l’AAS con una reputazione quasi mitica all’interno del mondo del BodyBuilding. Poiché i dati sugli esseri umani sono molto limitati, spesso dobbiamo fare affidamento sugli aneddoti nel tentativo di formulare ipotesi su di esso. Come si può leggere in quasi tutti i forum dedicati al BodyBuilding, le esperienze con il Trenbolone variano ampiamente – con alcuni utenti che adorano assolutamente il composto mentre altri ne consigliano estrema cautela nell’uso o dicono agli altri utenti di evitarlo a tutti i costi. Nonostante questa grande divergenza di opinioni, non si può contestare la sua popolarità poiché numerosi studi hanno dimostrato negli anni che tale molecola è uno dei composti anabolizzanti più frequentemente usati, con una percentuale compresa tra il 20 e il 25% dei culturisti supplementari chimicamente che hanno riferito di averlo usato nell’arco degli ultimi dodici mesi. (1)(2)(3)
Il mio obiettivo con questo articolo sarà quello di utilizzare quante più informazioni disponibili per cercare di formulare alcune solide conclusioni riguardo al funzionamento e al potenziale utilizzo del composto. Allo stesso tempo spero di contribuire a dissipare alcuni miti che vengono ancora propagandati troppo spesso.
Come precedentemente accennato, esistono solo un paio di studi sull’uomo di cui sono a conoscenza, quindi la maggior parte del materiale citato proverrà da studi svolti su animali o in vitro. La domanda che dovrebbe essere posta è la seguente: possiamo prendere questi dati e applicarli concretamente sui BodyBuilder? Personalmente, ritengo che ci sono dei dati molto concreti e universalmente applicabili sugli esseri umani e poi ce ne sono altri che potrebbero richiedere un disclaimer. Cercherò di fare del mio meglio per indicarli nel corso di questo articolo.
III. Nozioni di base sul Trenbolone
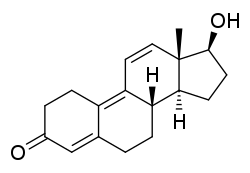
Il Trenbolone è considerabile quale Modulatore Selettivo del Recettore degli Androgeni (SARM), non progettato per l’uso umano (4), anche se venne commercializzato come farmaco da prescrizione per uso umano dalla Negma Laboratoires in Francia sotto il nome di Parabolan (Trenbolone Hexahydrobenzylcarbonato). Nonostante la sua primaria designazione, questo AAS continua ad essere pesantemente utilizzato dai Bodybuilder per promuovere la crescita muscolare, la riduzione del grasso e, di conseguenza, migliorare la composizione corporea.(5)(6) Quando sentiamo parlare di SARM colleghiamo tale termine ad una classe di agenti anabolizzanti non steroidei (vedi Ostarina, Andarina, LGD4033, ecc…). Però, tale definizione “particolaristica” non è del tutto corretta. Infatti, tutti gli AAS aventi un indice terapeutico (dato dalla Anabolico:Androgeno ratio) superiore a “1” sono considerabili quali SARM (l’indice terapeutico del Trenbolone è di circa 3,4). Si sa perfettamente che i SARM sono analoghi modificati degli ormoni sessuali maschili che normalmente esibiscono attività anabolica favorevole mentre, contemporaneamente, presentano una attività androgenica da moderata a minima in vivo rispetto agli androgeni endogeni.(7)(8)(9) Sono composti in fase di sviluppo da parte di molte aziende farmaceutiche nel tentativo di creare mezzi alternativi per il trattamento di condizioni come l’ipogonadismo e gli stati di deperimento muscolare e osseo. In sostanza, l’obiettivo è quello di ricreare gli aspetti positivi dati da dosi sovrafisiologiche di testosterone eliminando al contempo il rischio di eventi avversi che tendono a verificarsi quando si utilizzano tali dosaggi.(10) Questo obbiettivo lo si ritrova, appunto, concretizzato in tutti gli AAS che presentano modifiche dello scheletro carbossilico tali da permettere tale effetto.
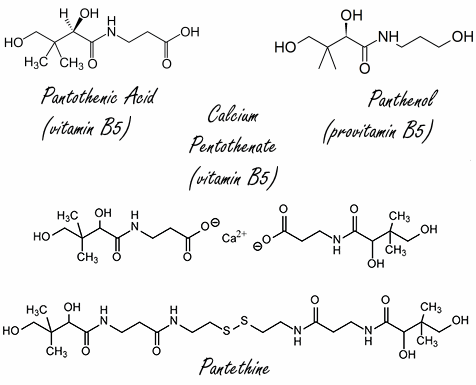
La maggior parte dei SARM steroidei hanno come base di partenza una molecola di Testosterone. La struttura chimica della molecola di Testosterone viene quindi tradizionalmente modificata in uno dei seguenti tre modi (11)(12):
- Esterificazione del gruppo 17β-idrossile che aumenta l’idrofobicità o la probabilità che la molecola possa essere respinta da una massa d’acqua;
- Alchilazione in posizione 7α la quale riduce l’affinità di legame con l’enzima 5α-reduttasi;
- Modifica strategica dei legami di carbonio in C1, C2, C9, C11 o C19 per ottenere una vasta gamma di effetti terapeutici.
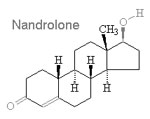
Il Trenbolone è un C19-norsteroide (19-nor), derivato dal Nandrolone (Nortestosterone). La rimozione del gruppo metilico nella posizione C19 dello scheletro carbossilico steroideo riduce significativamente la suscettibilità dei 19-norsteroidi all’azione dell’enzima aromatasi e a quella dell’enzima 5α-reduttasi.(4) Entreremo più nel dettaglio dei meccanismi sopracitati in seguito ma, per ora, è necessario che si comprenda semplicemente come le sottili modifiche allo scheletro carbossilico della molecola di Testosterone possano tradursi direttamente in cambiamenti significativi del comportamento della nuova molecola derivata. Alcuni di questi cambiamenti possono includere l’affinità di legame del composto per il recettore degli androgeni e la sua affinità di legame con numerosi enzimi in grado di convertirlo in altri steroidi.(13)
Il Trenbolone differisce dal suo precursore (Nandrolone) per:
1- Il doppio legame inserito in C9– C10, che inibisce totalmente l’aromatizzazione e aumenta la resistenza al passaggio epatico;
2- l’insaturazione in C11-C12 che aumenta l’affinità per il recettore androgeno, rendendo il Trenbolone uno degli anabolizzante con la più forte affinità AR. (14)
Il valore Anabolico/Androgeno del Trenbolone rispetto al Testosterone (100/100) è pari a 625:185.
Quindi, il Trenbolone ha proprietà SARM-simili in quanto presenta una affinità significativamente minore ai percorsi metabolici ai quali è soggetto il Testosterone. Ma di questo ne parleremo in seguito.
IV. Storia del Trenbolone

L’enorme potenziale anabolizzante del Trenbolone, così come dei suoi analoghi, è stato riportato fin dagli anni ’60. Come molti di voi già sapranno, venne sintetizzata anche una versione orale denominata Metribolone (conosciuta anche come Methyltrienolone o Methyltrenbolone), tuttavia non è mai stata commercializzata come agente anabolizzante a causa della sua tossicità epatica estrema – causando colestasi intraepatica a quantità somministrate per via orale pari a 1 mg/giorno.(15)

A parte la parentesi francese del Parabolan (Trenbolone Hexahydrobenzylcarbonato), commercializzato dalla Negma fino al 1997, il Trenbolone non è mai stato approvato per l’uso umano e il suo utilizzo è stato (ed è) principalmente quello di agente per la promozione della crescita nel bestiame.(16)(17) Per tale scopo viene usato sia singolarmente che in combinazione con Estradiolo (E2).(18) L’uso di impianti per il bestiame contenenti la combinazione di Trenbolone ed Estradiolo è stata approvata dalla FDA nel 1992 (19), e ora circa il 90% dei bovini da carne negli Stati Uniti viene trattato con un mix di estrogeni, androgeni e/o progestinici volto a promuoverne la crescita.(20) Gli impianti per il bestiame sono un grande business con fino a 20 milioni di bovini all’anno impiantati con Trenbolone e un reddito annuo probabilmente superiore a un miliardo di dollari.(21)

Nonostante l’approvazione da parte della FDA, sussistono ancora problemi di sicurezza poiché il Trenbolone Acetato (TBA), estere utilizzato per trattare il bestiame, ei suoi metaboliti sono stati identificati come potenziali sostanze chimiche dannose per il sistema endocrino (EDC). Gli EDC sono molecole esogene che possono imitare o inibire l’azione dei recettori ormonali come i recettori degli estrogeni, degli androgeni e degli ormoni tiroidei. Questi EDC possono anche alterare la sintesi, l’azione, il metabolismo e la secrezione di ormoni endogeni la quale può portare a problemi gravi come obesità, diabete e persino il cancro. (22)(23)

A causa della potenziale gravità degli EDC, negli ultimi due decenni si è registrata una maggiore attenzione internazionale sull’esposizione ambientale e sugli effetti degli EDC nell’uomo e nella fauna selvatica.(24)(25) Come precedentemente accennato, il TBA ei suoi metaboliti sono stati identificati come EDC attraverso numerosi studi, possono essere diffusi in ambienti agricoli e sono associati a tossicità riproduttiva. (26)(27)(28) Il problema è che è necessaria soltanto un’esposizione a concentrazioni molto basse per causare potenziali problemi, come è stato dimostrato negli animali come i pesci, i quali hanno mostrato disordini nel comportamento sessuale e una diminuzione della fertilità. (29)
Sarà anche importante essere in grado di distinguere i vari tipi di impianti contenenti TBA, dal momento che molti degli studi che esamineremo in seguito utilizzeranno tipi diversi sugli animali presi in esame. Quello che segue è un elenco dei tipi di impianti comuni usati negli Stati Uniti, con specificazione delle loro concentrazioni ormonali:
- Revalor-XS (200mg TBA / 40mg E2)
- Revalor-200 (200mg TBA / 20mg E2)
- Revalor-H (140mg TBA / 14mg E2)
- Revalor-S (120mg TBA / 24mg E2)
- Revalor-IS (80mg TBA / 16mg E2)
- Revalor-IH (80mg TBA / 8mg E2)
- Revalor-G (40mg TBA / 8mg E2)
- Synovex PLUS (200mg TBA / 28mg E2)
- Synovex-C (100mg Progesterone / 10mg E2)
- Synovex-ONE Grass (150mg TBA / 15mg E2)
- Synovex-S (200mg Progesterone / 20mg E2)
- Synovex-H (200mg Testosterone / 20mg E2)
V. Metabolismo e fisiologia
Precedentemente ho fatto breve menzione ai metaboliti del TBA, quindi, ora, per completezza è giusto entrare nei dettagli. E’ corretto rammentare che la maggior parte delle informazioni riguardanti il metabolismo del Trenbolone in vivo provengono da osservazioni su bestiame e roditori (30)(31)(32). È fondamentale anche comprendere che vi sono differenze marcate nella quantità di vari metaboliti osservati nei modelli di ratti e mucche, i due mammiferi più intensamente studiati. (33) Torneremo a trattare questo argomento dopo aver esaminato alcuni dei principi fondamentali.

Il nome chimico del TBA è 17ß-idrossi-estra-4,9,11-trien-3-one-17-acetato, talvolta abbreviato in 17β-TBOH-acetato. Dopo un’iniezione intramuscolare, viene rapidamente idrolizzato nel metabolita biologicamente attivo noto come 17β-idrossi-estra-4,9,11-trien-3-one o 17β-TBOH.(34) Da lì viene ulteriormente convertita in metaboliti inclusi i glucuronidi (per esempio Trendione / TBO) e altri cinque metaboliti idrossilati polari.(35) La serie di questi processi metabolici può essere riassunta come segue:
- 17ß-hydroxy-estra-4,9,11-trien-3-one-17-acetato / 17β-TBOH-acetato (Trenbolone Acetato)
- 17ß-hydroxy-estra-4,9,11-trien-3-one / 17β-TBOH
- Estra-4,9,11-triene-3,17-dione / TBO (Trendione)
- 17a-hydroxy-estra-4,9,11-trien-3-one / 17α-TBOH (Epitrenbolone)

Il 17β-TBOH ha una maggiore affinità per gli AR rispetto a qualsiasi altro dei suoi metaboliti primari suggerendo che la biotrasformazione del Trenbolone riduce l’attività biologica dello steroide.(26)(27)(35) Per mettere questo in prospettiva, in uno studio l’elevata affinità del 17β-TBOH nei confronti del recettore degli androgeni umani e del recettore del progesterone bovino è stata ridotta dopo che la molecola è stata metabolizzata in 17α-TBOH e TBO a meno di 1/24 della dose originale del composto.(36) Questo comportamento è in netto contrasto con quello osservato nel Testosterone la cui conversione in DHT e in estrogeni porta a composti più potenti in relazione all’affinità del legame con il recettore bersaglio.(37)(38) Tuttavia, il comportamento del TBA è simile per natura ad altri composti 19-norsteroidei (come il Nandrolone), la cui affinità AR diminuisce una volta 5α-ridotta.(39)
Come accennato in precedenza, vi è una certa variazione nel metabolismo del 17-TBOH tra i mammiferi poiché i metaboliti primari sono il 17ß-idrossi-estra-4,9,11-trien-3-one e l’Estra-4,9,11-triene- 3,17-dione con, a loro volta, metaboliti 16α e 16ß-idrossilati nel ratto. Nella mucca questi metaboliti sono trascurabili e il 17α-TBOH è il prodotto principale insieme a piccole quantità di 16α e 16ß-idrossi-17α-TBOH (30)(31). Segue un grafico dettagliato che confronta le differenze tra gli animali:
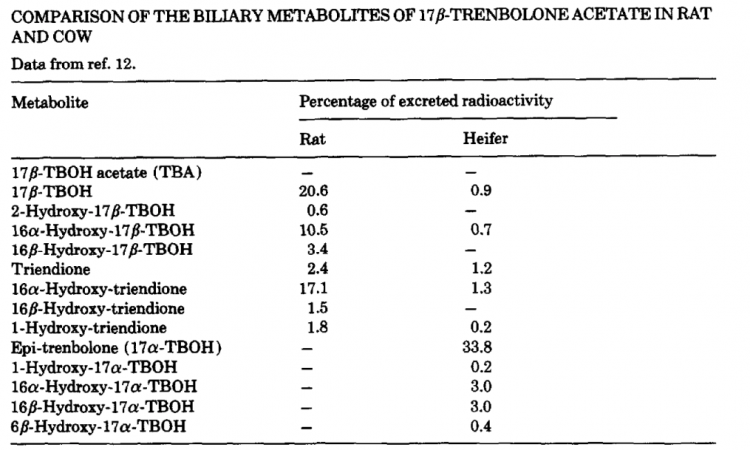
Fortunatamente per noi, esiste uno studio su esseri umani che ci può aiutare a chiarire come l’uomo metabolizzi il Trenbolone – almeno dopo che questo è stato ingerito per via orale. (35) Lo studio è stato progettato per indagare sugli effetti dell’ingestione di cibo contaminato e quindi il team di ricerca ha iniettato il 17β-TBOH in un pezzo di hamburger fritto da 5g, con una dose di 0,04 mg/kg di peso corporeo. Dopo un singolo consumo, il 63% della dose somministrata è stata escreta tramite l’urina entro 72 ore; a 24 ore il 50% della dose somministrata è stata osservata nei campioni di urina.
I risultati hanno anche rivelato che, negli esseri umani, il 17β-TBOH ingerito è principalmente escreto intatto come 17β-TBOH, come Epitrenbolone (17α-TBOH) o come Trendione (TBO) – con la maggior parte in forma 17α-TBOH. In questo senso, la biotrasformazione del 17ß-TBOH negli esseri umani assomiglia più da vicino a quella delle mucche che a quella dei roditori. Inoltre, nell’urina umana sono stati rilevati numerosi metaboliti polari di 17β-TBOH, sebbene in concentrazione molto inferiore rispetto a quei metaboliti precedentemente menzionati. (40)

Il 17β-TBOH presenta una bassa biodisponibilità orale dal momento che non presenta una metilazione in posizione 17α. I risultati di due saggi di Hershberger dimostrano che il Trenbolone è circa 80-100 volte meno efficace assunto per via orale rispetto a somministrazione tramite iniezione (comportamento legato appunto alla biodisponibilità).(26) Nonostante questo, il TBA e, ovviamente, 17β-TBOH hanno ancora dimostrato di alterare il sistema riproduttivo di umani, maiali, topi, ratti e altre specie di mammiferi a livelli di dosaggio relativamente bassi quando somministrati per via orale.
Nella prossima parte di questa serie di articoli, esploreremo l’impatto del Trenbolone su vari percorsi anabolici e marker della salute metabolica. Vedremo anche come il Trenbolone influenzi la produzione endogena di ormoni e inizieremo ad analizzare in maniera approfondita i suoi effetti su anabolismo e ipertrofia.
Stay tuned!
Gabriel Bellizzi
Riferimenti:
- The Science of Trenbolone – By Chest Rockwell
- Perry PJ, Lund BC, Deninger MJ, Kutscher EC, Schneider J. Anabolic steroid use in weightlifters and bodybuilders: an internet survey of drug utilization. Clin J Sport Med. 2005 Sep;15(5):326-30.
- Parkinson AB, Evans NA. Anabolic androgenic steroids: a survey of 500 users. Med Sci Sports Exerc. 2006 Apr;38(4):644-51.
- Ip EJ, Barnett MJ, Tenerowicz MJ, Perry PJ. The Anabolic 500 survey: characteristics of male users versus nonusers of anabolic-androgenic steroids for strength training. Pharmacotherapy. 2011 Aug;31(8):757-66.
- Donner DG, Beck BR, Bulmer AC, Lam AK, Du Toit EF. Improvements in body composition, cardiometabolic risk factors and insulin sensitivity with trenbolone in normogonadic rats. Steroids. 2015 Feb;94:60-9.
- Daniels JM, van Westerloo DJ, de Hon OM, Frissen PH. [Rhabdomyolysis in a bodybuilder using steroids]. Ned Tijdschr Geneeskd. 2006 May 13;150(19):1077-80. Dutch.
- Geraci MJ, Cole M, Davis P. New onset diabetes associated with bovine growth hormone and testosterone abuse in a young body builder. Hum Exp Toxicol. 2011 Dec;30(12):2007-12.
- Omwancha J, Brown TR. Selective androgen receptor modulators: in pursuit of tissue-selective androgens. Curr Opin Investig Drugs. 2006 Oct;7(10):873-81. Review.
- Gao W, Dalton JT. Expanding the therapeutic use of androgens via selective androgen receptor modulators (SARMs). Drug Discov Today. 2007 Mar;12(5-6):241-8. Review.
- Thevis M, Schänzer W. Synthetic anabolic agents: steroids and nonsteroidal selective androgen receptor modulators. Handb Exp Pharmacol. 2010;(195):99-126.
- Calof OM, Singh AB, Lee ML, Kenny AM, Urban RJ, Tenover JL, Bhasin S. Adverse events associated with testosterone replacement in middle-aged and older men: a meta-analysis of randomized, placebo-controlled trials. J Gerontol A Biol Sci Med Sci. 2005 Nov;60(11):1451-7.
- Kicman AT. Pharmacology of anabolic steroids. British Journal of Pharmacology. 2008;154(3):502-521.
- Haendler B, Cleve A. Recent developments in antiandrogens and selective androgen receptor modulators. Mol Cell Endocrinol. 2012 Apr 16;352(1-2):79-91.
- Fragkaki AG, Angelis YS, Koupparis M, Tsantili-Kakoulidou A, Kokotos G, Georgakopoulos C. Structural characteristics of anabolic androgenic steroids contributing to binding to the androgen receptor and to their anabolic and androgenic activities. Applied modifications in the steroidal structure. Steroids. 2009 Feb;74(2):172-97.
- Unique steroid congeners for receptor studies. Ojasoo, Raynaud. Cancer Research 38 (1978):4186-98.
- Krüskemper HL, Noell G. Liver toxicity of a new anabolic agent: methyltrienolone (17-alpha-methyl-4,9,11-estratriene-17 beta-ol-3-one). Steroids. 1966 Jul;8(1):13-24.
- Hunt DW, Henricks DM, Skelley GC, Grimes LW. Use of trenbolone acetate and estradiol in intact and castrate male cattle: effects on growth, serum hormones, and carcass characteristics. J Anim Sci. 1991 Jun;69(6):2452-62.
- Chung KY, Johnson BJ. Application of cellular mechanisms to growth and development of food producing animals. J Anim Sci. 2008 Apr;86(14 Suppl):E226-35.Epub 2007 Oct 26. Review.
- Metzler M, Pfeiffer E. Genotoxic potential of xenobiotic growth promoters and their metabolites. APMIS. 2001 Feb;109(2):89-95. Review.
- Chung KY, Baxa TJ, Parr SL, Luqué LD, Johnson BJ. Administration of estradiol, trenbolone acetate, and trenbolone acetate/estradiol implants alters adipogenic and myogenic gene expression in bovine skeletal muscle. J Anim Sci. 2012 May;90(5):1421-7.
- Balter M. Scientific cross-claims fly in continuing beef war. Science. 1999 May 28;284(5419):1453, 1455.
- Lawrence JD, Ibarburu MA. Proceedings of the NCCC-134 Conference on Applied Commodity Price Analysis, Forecasting, and Market Risk Management; 16 and 17 April 2007; Chicago.
- Diamanti-Kandarakis E, Bourguignon JP, Giudice LC, Hauser R, Prins GS, Soto AM, Zoeller RT, Gore AC. Endocrine-disrupting chemicals: an Endocrine Society scientific statement. Endocr Rev. 2009 Jun;30(4):293-342. Review.
- Rachoń D. Endocrine disrupting chemicals (EDCs) and female cancer: Informing the patients. Rev Endocr Metab Disord. 2015 Dec;16(4):359-64.
- Birnbaum LS. State of the science of endocrine disruptors. Environ Health Perspect. 2013 Apr;121(4):A107.
- Baynes RE, Dedonder K, Kissell L, Mzyk D, Marmulak T, Smith G, Tell L, Gehring R, Davis J, Riviere JE. Health concerns and management of select veterinary drug residues. Food Chem Toxicol. 2016 Feb;88:112-22.
- Wilson VS, Lambright C, Ostby J, Gray LE Jr. In vitro and in vivo effects of 17beta-trenbolone: a feedlot effluent contaminant. Toxicol Sci. 2002 Dec;70(2):202-11.
- Durhan EJ, Lambright CS, Makynen EA, Lazorchak J, Hartig PC, Wilson VS, Gray LE, Ankley GT. Identification of metabolites of trenbolone acetate in androgenic runoff from a beef feedlot. Environ Health Perspect. 2006 Apr;114 Suppl 1:65-8.
- Gall HE, Sassman SA, Lee LS, Jafvert CT. Hormone discharges from a midwest tile-drained agroecosystem receiving animal wastes. Environ Sci Technol. 2011 Oct 15;45(20):8755-64.
- Jensen KM, Makynen EA, Kahl MD, Ankley GT. Effects of the feedlot contaminant 17alpha-trenbolone on reproductive endocrinology of the fathead minnow. Environ Sci Technol. 2006 May 1;40(9):3112-7.
- Pottier J, Busigny M, Grandadam JA. Plasma kinetics, excretion in mild and tissue levels in the cow following implantation of trenbolone acetate. J Anim Sci. 1975 Sep;41(3):962-8.
- Pottier J, Cousty C, Heitzman RJ, Reynolds IP. Differences in the biotransformation of a 17 beta-hydroxylated steroid, trenbolone acetate, in rat and cow. Xenobiotica. 1981 Jul;11(7):489-500.
- Evrard P, Maghuin-Rogister G, Rico AG. Fate and residues of trenbolone acetate in edible tissues from sheep amd calves implanted with tritium-labeled trenbolone acetate. J Anim Sci. 1989 Jun;67(6):1489-96
- Metzler M. Metabolism of some anabolic agents: toxicological and analytical aspects. J Chromatogr. 1989 Apr 7;489(1):11-21.
- Dorts J, Richter CA, Wright-Osment MK, Ellersieck MR, Carter BJ, Tillitt DE. The genomic transcriptional response of female fathead minnows (Pimephales promelas) to an acute exposure to the androgen, 17beta-trenbolone. Aquat Toxicol.2009 Jan 18;91(1):44-53.
- Spranger B, Metzler M. Disposition of 17 beta-trenbolone in humans. J Chromatogr. 1991 Apr 5;564(2):485-92.
- Bauer ER, Daxenberger A, Petri T, Sauerwein H, Meyer HH. Characterisation of the affinity of different anabolics and synthetic hormones to the human androgen receptor, human sex hormone binding globulin and to the bovine progestin receptor. APMIS. 2000 Dec;108(12):838-46.
- Wilson JD. The role of 5alpha-reduction in steroid hormone physiology. Reprod Fertil Dev. 2001;13(7-8):673-8. Review.
- Santen RJ, Brodie H, Simpson ER, Siiteri PK, Brodie A. History of aromatase: saga of an important biological mediator and therapeutic target. Endocr Rev. 2009 Jun;30(4):343-75.
- Sundaram K, Kumar N, Monder C, Bardin CW. Different patterns of metabolism determine the relative anabolic activity of 19-norandrogens. J Steroid Biochem Mol Biol. 1995 Jun;53(1-6):253-7.
- Yarrow JF, McCoy SC, Borst SE. Tissue selectivity and potential clinical applications of trenbolone (17beta-hydroxyestra-4,9,11-trien-3-one): A potent anabolic steroid with reduced androgenic and estrogenic activity. Steroids. 2010 Jun;75(6):377-89.