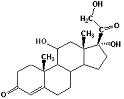
La Yohimbina (17α-hydroxy-yohimban-16α-carboxylic acid methyl ester) è un alcaloide estratto dalla corteccia della Pausinystalia Johimbe e dalle foglie della Rauvolfia serpentina (nota anche come radice di serpente indiana) venduto in alcuni paesi dietro prescrizione medica per il trattamento della disfunzione erettile, per il trattamento del disturbo da ridotto desiderio sessuale (riduzione della libido), e viene anche utilizzata per i suoi presunti effetti afrodisiaci.
La Yohimbina è un noto antagonista degli adrenocettori α-2. Ciò significa semplicemente che la Yohimbina può bloccare i recettori sulle cellule adipose che normalmente bloccano il processo di rilascio dei grassi nel torrente ematico. Ciò è controllato dagli ormoni Adrenalina e Noradrenalina (detti anche Epinefrina e Norepinefrina) che normalmente si legano agli adrenocettori delle cellule adipose per segnalare il rilascio dei grassi nel sistema circolatorio affinché possano essere bruciati come fonte energetica. Il corpo cerca di fermare questo processo attraverso la stimolazione dei recettori α-2 che dicono alle cellule grasse di accumulare materiale. Quando la Yohimbina blocca i recettori α-2 viene rilasciato più grasso che poi viene bruciato come fonte energetica.
Il principale studio che supporta quanto sopraddetto è “Does yohimbine act as a slimming drug?” di Kucio C., Jonderko, K., Piskorska D., Dipartimento di gastroenterologia, Silesian School of Medicine, Katowice, Polonia [Isr J Med Sci. 1991 Oct;27(10):550-6].
Dal momento che la Yohimbina è un antagonista degli α2-recettori, è stata esaminata per la sua efficacia nella cura dell’obesità.
20 donne obese sono state sottoposte a 3 settimane di dieta ipocalorica (1.000 kcal/giorno) dopo di che sono state assegnate a caso a due trattamenti secondo la procedura dello studio a doppio cieco: 10 soggetti hanno ricevuto 5mg di Yohimbina 4 volte al giorno mentre altri 10 hanno ricevuto un placebo, tutti hanno seguito una dieta ipocalorica di 1.000 kcal/giorno.
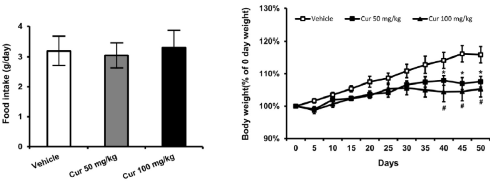
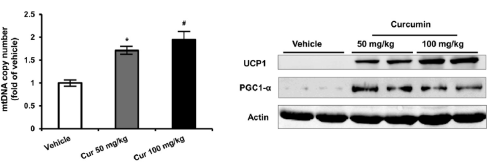
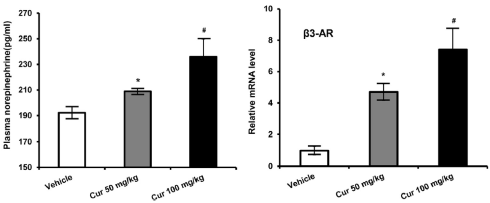
I risultati di questo studio hanno mostrato che i soggetti che hanno ricevuto la Yohimbina hanno sperimentato una perdita di grasso media di 3,55 kg mentre il gruppo placebo ha perso solo 2,21 kg. Questi studi hanno mostrato anche che il rilascio di Insulina dovuto all’ingestione del cibo inibisce le azioni della Yohimbina mentre una dieta molto ipocalorica ne agevola l’efficacia. Meno cibo significa anche meno rilascio di Insulina. Quindi una dieta ipocalorica combinata con una somministrazione multidose di Yohimbina può aumentare il dispendio calorico di oltre il 30%.
Ci sono almeno due punti chiave per massimizzare gli effetti della Yohimbina:
1. Una dose adeguata – Molte volte viene consigliata una dose troppo bassa. Negli studi, la quantità minima di Yohimbina assunta oralmente è stata di 0,2 mg/kg al giorno. Quindi una persona di 90 kg ha bisogno di 18 mg di Yohimbina al giorno per ottenere l’effetto lipolitico desiderato. Attenzione: con la Yohimbina alcune persone sperimentano delle risposte molto forti del ritmo cardiaco e della pressione ematica. Per valutare la propria tolleranza è consigliabile cominciate con circa 1/3 della dose ottimale (quindi una persona di 90 kg comincerebbe con 6 mg) incrementando la dose nel corso di un periodo di alcuni giorni (generalmente 2-3 giorni). Se il ritmo cardiaco o la pressione ematica aumentano troppo si consiglia l’interruzione dell’assunzione di Yohimbina.
2. Deve essere assunta a stomaco vuoto – È una cosa fondamentale perché anche una piccola risposta insulinica impedirà qualsiasi effetto della Yohimbina. Assumere la Yohimbina con il cibo produrrà una risposta insulinica maggiore rispetto all’assunzione del cibo da solo (la cosa è legata ai recettori α nel pancreas). In base a questa regola, uno dei momenti migliori per assumere la Yohimbina è prima dell’allenamento aerobico del mattino. Se non si svolge una sessione aerobica al mattino, credo che un altro momento favorevole per assumere la Yohimbina sia 30 minuti prima della sessione di allenamento serale, o comunque almeno 3-4 ore dopo aver mangiato affinché i livelli di Insulina calino a sufficienza. Comunque penso che la prima parte della giornata sia il momento migliore.
Alcuni atleti assumono la Yohimbina con un po’ di Caffeina circa 30 minuti prima della sessione aerobica. Assumono anche l’associazione ECA, ma mai insieme alla Yohimbina. La combinazione ECA + Yohimbina, come l’associazione Yohimbina + Clenbuterolo, è potenzialmente pericolosa (più dei due composti presi singolarmente) a causa dell’interazione sul ritmo cardiaco e sulla pressione ematica. Gli atleti in questione assumono la Yohimbina prima della sessione aerobica del mattino, e per la prima dose di ECA aspettano 4 ore dopo l’assunzione di Yohimbina. L’emivita della Yohimbina è di 0,25-2 ore.
Ricapitolando, gli effetti collaterali della Yohimbina a seconda del dosaggio assunto possono comportare anche importanti alterazioni della pressione arteriosa, in senso ipertensivo, che spesso si accompagnano ad aumento della frequenza cardiaca. Gli eventi avversi a carico del tratto gastrointestinale comprendono nausea e vomito. Per i suoi effetti eccitatori a carico del SNC la molecola comporta spesso la comparsa di irritabilità, ansia generalizzata, eccitazione, iperattività motoria, reazioni maniacali, allucinazioni, insonnia, tremore e vertigine. La contemporanea assunzione di Yohimbina e farmaci antidepressivi o fenotiazine può comportare un aumentato rischio di comparsa e aggravamento degli effetti collaterali.
Concludendo, la Yohimbina si presenta come un efficace agente lipolitico specie nei confronti del grasso testardo. Dati i suoi possibili effetti collaterali, la Yohimbina deve essere usata con cautela calcolando accuratamente le dosi così da evitare o diminuire la comparsa di effetti avversi.
Gabriel Bellizzi
Riferimenti
– Domande & Risposte senza censura di Author L. Rea (Olympian’s News)
– Chemical Muscle Enhancement II (Author L. Rea)
– Chiedete a Lyle McDonald (THINK MUSCLE – Olympian’s News)