Introduzione:

Gli incretino-mimetici sono una recente classe di farmaci antidiabete che prevede la modulazione del sistema delle Incretine. Si legano e attivano i recettori del peptide glucagone-simile-1 (GLP-1) sulle beta-cellule pancreatiche, dando inizio alla secrezione e alla sintesi di Insulina. Gli incretino-mimetici di ultima generazione hanno attività sia sul recettore del GLP-1 sia su quello del Polipeptide Inibitore Gastrico (GIP), un ormone inibitore della famiglia delle secretine (Incretine) con ruolo principale, essendo un’Incretina, di stimolare la secrezione di Insulina.
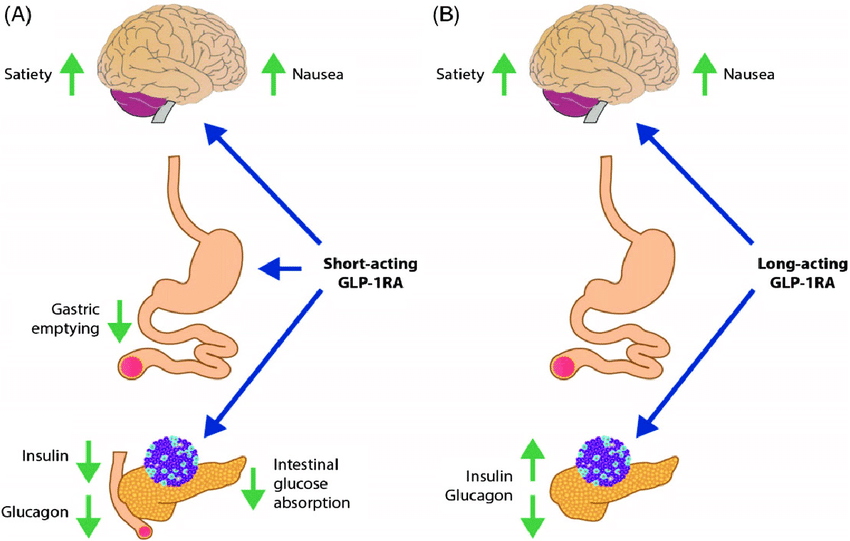
Poiché questi composti non hanno attività insulinotropica a concentrazioni di glucosio inferiori, il rischio di ipoglicemia – una nota carenza degli attuali trattamenti antidiabete – è basso. Inoltre, è stato dimostrato che gli incretino-mimetici sono associati a effetti benefici sui fattori di rischio cardiovascolare, come la perdita di peso, la riduzione della pressione sanguigna e le modifiche del profilo lipidico. Ciò nonostante, gli effetti avversi che possono causare non sono trascurabili e la loro diffusione per uso “Off-Label” ne ha mostrato le limitazioni sia in soggetti obesi che in utilizzatori per finalità estetiche.
La disamina che seguirà sarà divisa in due parti preposte a spiegare, a partire dalla loro genesi, il funzionamento delle incretine per poi passare in rassegna le caratteristiche di quelle che sono le forme farmaceutiche di incretino-mimetici utilizzate in medicina e in ambito “Off-Label/ricreativo”.
In questa prima parte vedremo nel dettaglio le incretine endogene e le molecole incretino-mimentiche presenti nel mercato…
Ormoni Incretinici [Incretine]:

Negli anni ’70, Jens Juul Holst e Joel Habener iniziarono la ricerca sull’ormone GLP-1, inizialmente in relazione alla malattia dell’ulcera duodenale.[1] Esaminarono gli ormoni secreti durante l’alimentazione e li testarono su pancreas di maiale, portando alla scoperta della notevole potenza del GLP-1 nel 1988. Il loro lavoro, che in seguito ha contribuito in modo significativo al trattamento del diabete e dell’obesità, è valso a loro e a Daniel Drucker il premio della Fondazione Warren Alpert del 2021.[1] La ricerca è proseguita e nel 1993 Michael Nauck è riuscito a infondere il GLP-1 in persone affette da diabete di tipo II, stimolando l’Insulina e inibendo il Glucagone e portando la glicemia a livelli normali. Tuttavia, il trattamento dei pazienti diabetici con gli ormoni GLP-1 ha provocato notevoli effetti collaterali, inducendo i ricercatori finanziati da Novo Nordisk a cercare di sviluppare un composto adatto all’uso terapeutico.[1]
Nel 1998 un team di ricercatori di Novo Nordisk, guidato dalla scienziata Lotte Bjerre Knudsen, ha sviluppato la Liraglutide, un agonista del recettore del peptide glucagone-simile-1 con potenziale di utilizzo per il trattamento del diabete di tipo II.[2]

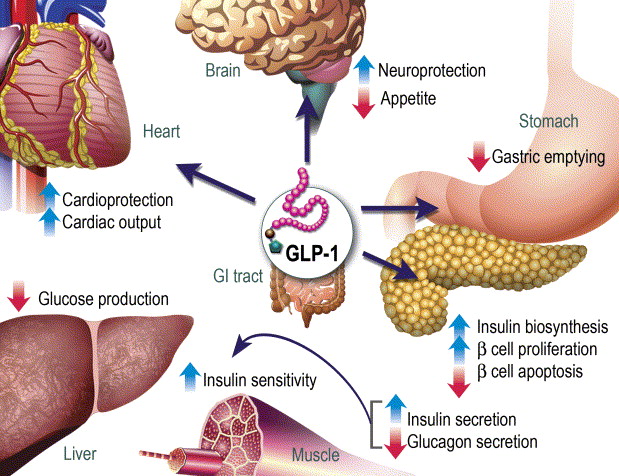
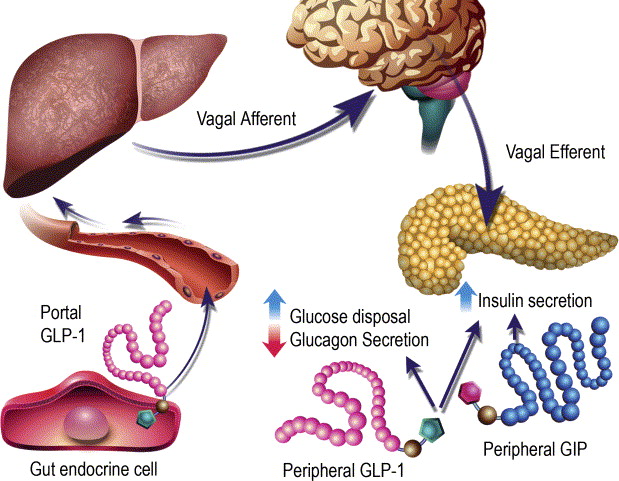
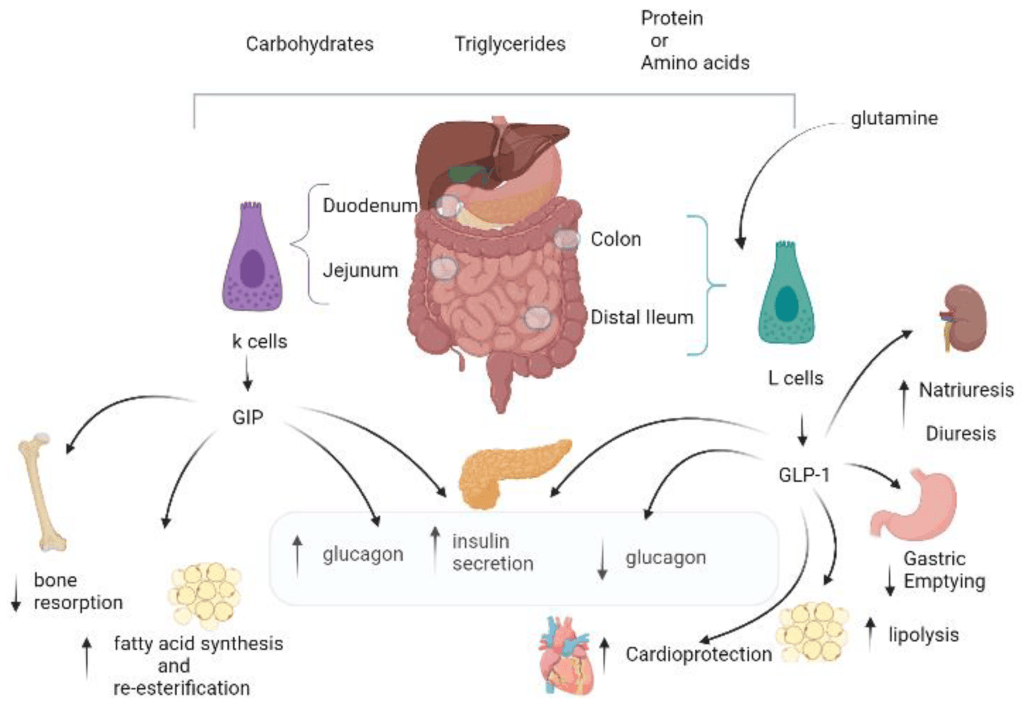
Gli ormoni incretinici GLP-1 e il GIP sono ormoni peptidici intestinali rilasciati in risposta all’ingestione di cibo.(3) L’effetto più importante del GLP-1 e del GIP è la loro capacità di potenziare la secrezione di Insulina indotta dal Glucosio da parte del pancreas – il cosiddetto effetto incretinico. Nei soggetti sani l’effetto incretinico rappresenta fino al 70% dell’Insulina secreta in risposta all’ingestione di Glucosio.(4) Il GLP-1 è un polipeptide di 30 aminoacidi sintetizzato dal proglucagone nelle cellule endocrine L distribuite principalmente nella mucosa della parte distale dell’intestino tenue e del colon. Il GIP è un polipeptide di 42 aminoacidi rilasciato dalle cellule endocrine K presenti nella mucosa del duodeno e della parte superiore del digiuno.(5) Mentre il GLP-1 viene rapidamente degradato (dall’enzima ubiquitario dipeptidil peptidasi-4 (DPP-4)) in circolo con un’emivita apparente di 1 – 1,5 minuti,(6) il GIP viene degradato più lentamente, con un’emivita per l’ormone intatto di 7 minuti.(7) L’ormone aumenta la secrezione di Insulina all’inizio del pasto, ma non ha alcuna attività insulinotropica a concentrazioni di glucosio inferiori (meno di 4mM), non favorendo così l’ipoglicemia. Il GLP-1 aumenta anche la biosintesi dell’Insulina e l’espressione genica della stessa. Inoltre, esercita azioni trofiche e protettive sulle beta-cellule(8) e inibisce fortemente la secrezione pancreatica di Glucagone in modo glucosio-dipendente.(9) Al contrario, è stato dimostrato che la GIP stimola la secrezione di Glucagone. Gli ormoni esercitano il loro effetto insulinotropico attraverso recettori accoppiati a proteine G sulle beta-cellule pancreatiche.(10) Oltre agli effetti sul pancreas endocrino, entrambi gli ormoni hanno diverse altre funzioni. I recettori del GLP-1 si trovano in varie regioni del cervello (11) e, una volta attivati, promuovono il senso di sazietà che, in combinazione con l’inibizione della motilità gastrointestinale indotta dal GLP-1 (mediata dal nervo vago (12) ), riduce l’assunzione di cibo e, consequenzialmente, il peso corporeo. I recettori del GLP-1 si trovano anche nel cuore (13) e la maggior parte dei dati suggerisce che il GLP-1 esercita effetti protettivi sul miocardio. È stato inoltre riscontrato che il GLP-1 riduce l’aumento postprandiale dei trigliceridi e abbassa la concentrazione di acidi grassi liberi nell’uomo.(14) Infine, studi su animali e sull’uomo indicano che il GLP-1 ha proprietà natriuretiche e diuretiche attraverso la modulazione dello scambio renale Na+/H+ (15) – un meccanismo che potrebbe servire a ridurre la pressione sanguigna. La GIP non sembra avere effetti fisiologici sul tratto gastrointestinale, sull’appetito o sull’assunzione di cibo, ma può avere un ruolo nel metabolismo dei lipidi (16) e delle ossa.(17)
Nei pazienti con diabete di tipo II l’effetto incretinico è gravemente ridotto.(18, 19) Questo tratto fisiopatologico gioca probabilmente un ruolo centrale nell’incapacità di questi pazienti di secernere una quantità di Insulina sufficiente a prevenire l’iperglicemia in seguito all’assunzione di glucosio per via orale.(20-30) L’attenuata secrezione postprandiale (21) e la diminuita potenza insulinotropica del GLP-1 (22), in combinazione con l’abolizione dell’effetto insulinotropico del GIP (23) , sembrano essere responsabili del ridotto effetto incretinico nei pazienti con diabete di tipo II. Poiché l’effetto insulinotropico del solo GLP-1 (e non del GIP) è conservato nei pazienti con diabete di tipo II, sono state sviluppate modalità di trattamento antidiabete basate sull’effetto di questo peptide. È interessante notare che l’infusione endovenosa (iv) di GLP-1 nativo è in grado di normalizzare la glicemia nei pazienti con diabete di tipo 2, (24) ma a causa della breve emivita del GLP-1, la somministrazione terapeutica del GLP-1 nativo non è praticabile. Pertanto, per sfruttare le azioni benefiche del GLP-1 nel diabete di tipo II, sono stati sviluppati agonisti stabili a lunga durata d’azione del recettore del GLP-1 (incretino-mimetici). Nella sezione seguente verranno descritti gli incretino-mimetici disponibili, le loro caratteristiche e applicazioni.
Farmaci Incretino-mimetici:
- Exenatide [approvato nel 2005/2012]

L’Exenatide, il primo di questa classe di farmaci, è stato introdotto sul mercato negli Stati Uniti nel 2005 e in Europa nel 2007 con il nome commerciale Byetta® (Amylin Pharmaceuticals/Eli Lilly).
L’Exenatide è un peptide di 39 aminoacidi; è una versione sintetica dell’exendin-4, un peptide presente nel veleno del “mostro di Gila”.
L’ Exenatide è stata isolata per la prima volta nel 1992 presso il Veterans Administration Medical Center di New York City.[25]
L’Exenatide si lega al recettore umano intatto del Peptide Glucagone-Simile-1 (GLP-1R) in modo simile al GLP-1; l’Exenatide ha un’omologia aminoacidica del 50% con il GLP-1 e ha un’emivita più lunga in vivo.[26]
Si ritiene che l’Exenatide faciliti il controllo del glucosio in almeno cinque modi:
- L’Exenatide aumenta la risposta del Pancreas[27] (cioè aumenta la secrezione di Insulina) in risposta al consumo dei pasti; il risultato è il rilascio di una quantità di Insulina maggiore e più appropriata che aiuta a ridurre l’aumento della glicemia dovuto al consumo di cibo. Una volta che i livelli di glucosio nel sangue si avvicinano ai valori normali, la risposta del Pancreas alla produzione di Insulina si riduce; altri farmaci (come la rInsulina ) sono efficaci nell’abbassare la glicemia, ma possono “superare” il loro obiettivo e causare un abbassamento eccessivo della glicemia, provocando la pericolosa condizione di ipoglicemia.
- L’Exenatide sopprime anche il rilascio di Glucagone da parte del Pancreas in risposta al pasto, impedendo al fegato di produrre eccessivamente glucosio quando non è necessario e prevenendo così l’iperglicemia (livelli elevati di glucosio nel sangue).
- L’Exenatide contribuisce a rallentare lo svuotamento gastrico e quindi a ridurre la velocità di comparsa nel sangue del glucosio derivato dai pasti.
- L’Exenatide ha un effetto sottile ma prolungato di riduzione dell’appetito e di promozione della sazietà attraverso i recettori ipotalamici (recettori diversi da quelli dell’Amilina). La maggior parte delle persone che utilizzano l’Exenatide perdono lentamente peso e, in genere, la perdita di peso maggiore è ottenuta dalle persone più in sovrappeso all’inizio della terapia con l’Exenatide. Gli studi clinici hanno dimostrato che l’effetto di riduzione del peso continua allo stesso ritmo per 2,25 anni di uso continuato. Se suddivisi in quartili di perdita di peso, il 25% più alto registra una sostanziale perdita di peso, mentre il 25% più basso non registra alcuna perdita o un lieve aumento di peso.
- L’Exenatide riduce il contenuto di grasso nel fegato. L’accumulo di grasso nel fegato o la malattia del fegato grasso non alcolico (NAFLD) è fortemente correlata a diversi disturbi metabolici, in particolare a un basso livello di HDL e a Trigliceridi elevati, presenti nei pazienti con diabete di tipo II. È emerso che l’Exenatide ha ridotto il grasso epatico nei topi[28], nei ratti[29] e nell’uomo.[30]
I principali effetti collaterali del Exenatide (che condivide con tutte le molecole apopartenenti alla sua “famiglia”) sono nausea e vomito da lievi a moderati e transitori. L’incidenza dell’ipoglicemia associata al trattamento è bassa (31) – apparentemente dovuta agli effetti insulinotropi e glucagonostatici del GLP-1, dipendenti dal glucosio. Tuttavia, in combinazione con altri ipoglicemizzanti l’incidenza aumenta e dipende dalla dose di questi. Nella maggior parte degli studi con Exenatide gli episodi ipoglicemici minori sono definiti come glucosio plasmatico <3,3mM; negli studi LEAD sono definiti come glucosio plasmatico <3,1 mM. Negli studi che utilizzano Exenatide in combinazione con ipoglicemizzanti il rischio di episodi ipoglicemici minori è riportato tra il 15% e il 36%.(32) Nello studio Exenatide/Insulina Glargine l’1,5% dei pazienti ha sperimentato un’ipoglicemia grave.(33) Non c’è stata differenza tra i gruppi e l’incidenza è stata simile nei due gruppi.
Circa il 40% dei pazienti trattati con Exenatide in studi a lungo termine, controllati con placebo, ha sviluppato anticorpi contro il peptide durante le prime 30 settimane di trattamento.(32) L’esatto impatto degli anticorpi a lungo termine deve essere stabilito. L’Exenatide non è raccomandata durante la gravidanza o l’allattamento a causa della mancanza di dati sufficienti. L’Exenatide non deve essere utilizzata in pazienti con insufficienza renale, poiché viene eliminata principalmente nei reni attraverso la filtrazione glomerulare (31) e sono stati segnalati casi di insufficienza renale acuta. Nessun dato indica l’inibizione o l’induzione degli enzimi di metabolizzazione dei farmaci del citocromo P450. Dal 2005 la Food and Drug Administration (FDA) statunitense ha ricevuto 170 segnalazioni di pancreatite in pazienti trattati con Exenatide e ha ricevuto segnalazioni di pancreatite acuta, alcune delle quali erano casi gravi di pancreatite emorragica o necrotizzante in pazienti che assumevano Exenatide. Negli studi LEAD sono state osservate in totale (al 2010) 9 segnalazioni di pancreatite, nei pazienti trattati con Exanatide. E’ tutt’ora poco chiaro il nesso causale tra pancreatite ed Exenatide. Tuttavia, si raccomanda di interrompere il trattamento con incretino-mimetici in caso di sospetta pancreatite.(34) È stato suggerito che i risultati sul cancro nei roditori siano causati da un meccanismo non genotossico e specifico mediato dal recettore GLP-1 a cui i roditori sono particolarmente sensibili. La rilevanza per l’uomo è probabilmente insignificante dal punto di vista clinico, ma sono necessari ulteriori studi per chiarire i potenziali meccanismi alla base dello sviluppo del tumore delle cellule C nei pazienti trattati con analoghi del GLP-1 e le loro possibili implicazioni cliniche.(35)
Nel marzo 2013, la FDA ha pubblicato una Drug Safety Communication in cui annunciava l’avvio di indagini sui mimetici dell’incretina a causa dei risultati ottenuti da ricercatori accademici.[36] Poche settimane dopo, l’Agenzia europea per i medicinali ha avviato un’indagine simile sugli agonisti del GLP-1 e sugli inibitori della DPP-4.[37]
53 cause consolidate contro i produttori di “prodotti GLP-1/DPP-4” sono state archiviate nel 2015.[38]
Nel 2016 è stato pubblicato un lavoro che dimostra che è in grado di invertire l’alterata segnalazione del calcio nelle cellule epatiche steatotiche, che a sua volta potrebbe essere associata a un corretto controllo del glucosio.[39]
È in fase di valutazione per il trattamento del morbo di Parkinson.[40] Uno studio clinico di fase 3, iniziato nel gennaio 2020, ha avuto la sua data di completamento il 30 giugno 2024 (NCT04232969).[41]
L’Exenatide si presenta come soluzione parenterale destinata all’iniezione. Può essere somministrata nel sottocute dell’addome, del braccio o della coscia. Per migliorare la tollerabilità gastrointestinale, la terapia con Exenatide deve essere iniziata a 5mcg per dose somministrata due volte al giorno per almeno un mese. La dose di Exenatide può poi essere aumentata a 10mcg due volte al giorno.(31) La soddisfazione dei pazienti che hanno utilizzato Exenatide è stata valutata in un paio di studi. L’aggiunta di Exenatide a Metformina e altri ipoglicemizzanti ha determinato un miglioramento significativo della soddisfazione per il trattamento e della qualità di vita correlata alla salute dei pazienti dal basale a 26 settimane.(42) Il miglioramento è stato simile per i pazienti trattati con Insulina Glargine.
- Liraglutide [approvato nel 2010]
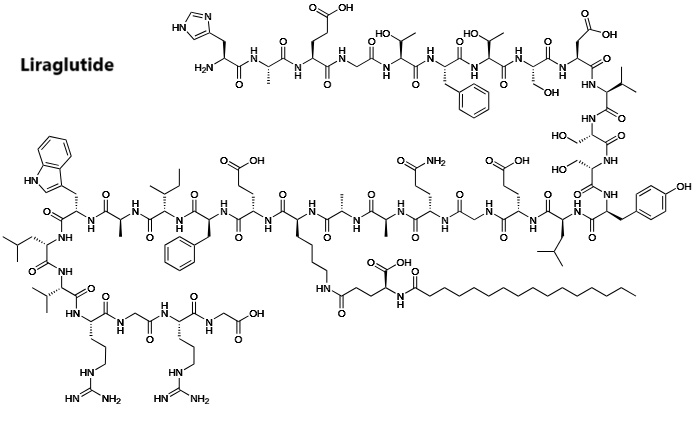
La Liraglutide è un analogo acilato del GLP-1 umano e presenta il 97% di omologia di sequenza con il GLP-1 nativo. L’analogo è prodotto con la tecnologia del DNA ricombinante nel lievito.(43) Ha un effetto sul recettore del GLP-1 simile a quello descritto per l’Exenatide. Un elevato grado di legame con le proteine plasmatiche causa una minore suscettibilità al metabolismo da parte della DPP-4 e l’emivita dopo la somministrazione di Liraglutide è di circa 13 ore.(44) Questo profilo d’azione prolungato rende Liraglutide adatto alla somministrazione una volta al giorno. Non ci sono differenze clinicamente significative nella farmacocinetica di Liraglutide tra soggetti di sesso maschile e femminile, soggetti di razza diversa o soggetti anziani e giovani.(45)
La Liraglutide, venduta tra l’altro con i marchi Victoza e Saxenda, è un farmaco antidiabetico utilizzato per il trattamento del diabete di tipo II e dell’obesità cronica.[46][47] Si tratta di una terapia di seconda linea per il diabete dopo la terapia di prima linea con la Metformina.[46][48] Non sono chiari i suoi effetti sugli esiti di salute a lungo termine, come le malattie cardiache e l’aspettativa di vita.[46][49] Viene somministrata mediante iniezione sotto cutanea.[46]
La Liraglutide è stata approvata per uso medico nell’Unione Europea nel 2009 e negli Stati Uniti nel 2010.[50][51] Nel 2021 è stato il 166° farmaco più comunemente prescritto negli Stati Uniti, con oltre 3 milioni di prescrizioni.[52][53]
L’azione prolungata della Liraglutide si ottiene attaccando una molecola di acido grasso in una posizione della molecola GLP-1-(7-37), consentendole di auto-associarsi e di legarsi all’albumina nel tessuto sottocutaneo e nel flusso sanguigno. Il GLP-1 attivo viene quindi rilasciato dall’albumina a un ritmo lento e costante. Il legame con l’albumina determina inoltre una degradazione più lenta e un’eliminazione renale ridotta rispetto a quella del GLP-1-(7-37).[54]
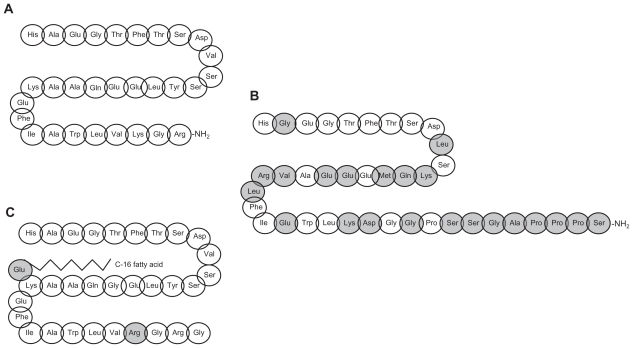
Come abbiamo visto, La Liraglutide è un agonista acilato del recettore del GLP-1, derivato dal GLP-1-(7-37) umano, una forma meno comune di GLP-1 endogeno.
Riduce l’iperglicemia correlata ai pasti (per 24 ore dopo la somministrazione) aumentando la secrezione di Insulina (solo) quando richiesto dall’aumento dei livelli di glucosio, ritardando lo svuotamento gastrico e sopprimendo la secrezione prandiale di Glucagone.[54][55]
Quindi, la Liraglutide provoca il rilascio di Insulina nelle cellule beta pancreatiche in presenza di una glicemia elevata. Questa secrezione di Insulina si attenua quando le concentrazioni di glucosio diminuiscono e si avvicinano all’euglicemia (livello normale di glucosio nel sangue). Diminuisce inoltre la secrezione di Glucagone in modo glucosio-dipendente e ritarda lo svuotamento gastrico. A differenza del GLP-1 endogeno, la Liraglutide è stabile contro la degradazione metabolica da parte delle peptidasi, con un’emivita plasmatica di 13 ore.[56][54]
Nei pazienti ad alto rischio cardiovascolare, è stato dimostrato che la Liraglutide riduce il rischio di morte per cause cardiovascolari, infarto miocardico non fatale o ictus non fatale. Le linee guida dell’ADA considerano attualmente Liraglutide una terapia farmacologica di prima linea per il diabete di tipo II (di solito insieme alla Metformina), in particolare per i pazienti con malattie cardiovascolari aterosclerotiche o obesità.[57] Una revisione Cochrane del 2011 ha dimostrato una riduzione dell’HbA1c dello 0,24% in più con Liraglutide. Del 24% in più con Liraglutide a 1,8 mg rispetto a Insulina Glargine, 0,33% in più rispetto a Exenatide 10mcg due volte al giorno, Sitagliptin e Rosiglitazone. In uno studio randomizzato e controllato (RCT) che ha confrontato Liraglutide, Insulina Glargine, Glimepiride e Sitagliptin (tutti aggiunti alla Metformina) con un follow-up di cinque anni, Insulina Glargine e Liraglutide sono risultate modestamente più efficaci nel raggiungimento e nel mantenimento dell’HbA1c target,[58] senza alcuna differenza negli esiti delle malattie microvascolari e cardiovascolari.[59]
La Liraglutide può anche essere utilizzata insieme alla dieta e all’esercizio fisico per la gestione cronica del peso negli adulti.[46] La Liraglutide ha portato a una perdita di peso maggiore rispetto ad alcuni precedenti analoghi del peptide glucagone-simile,[60] ma è meno efficace della dose standard di Semaglutide per la perdita di peso.[61][62]
In un recente studio pubblicato nel settembre 2024, Liraglutide ha aiutato i bambini di età compresa tra i 6 e i 12 anni a ridurre l’indice di massa corporea del 7,4% in uno studio di 56 settimane.[63] Se da un lato lo studio ha mostrato i potenziali benefici del farmaco, dall’altro solleva preoccupazioni riguardo all’uso di farmaci contro l’obesità in bambini così piccoli.[64] Novo Nordisk, l’azienda innovatrice che commercializza Liraglutide, ha chiesto alle autorità di regolamentazione statunitensi ed europee di estendere l’approvazione di Saxenda anche a questa fascia d’età più giovane, dato che attualmente è approvato solo per adolescenti e adulti.[65]
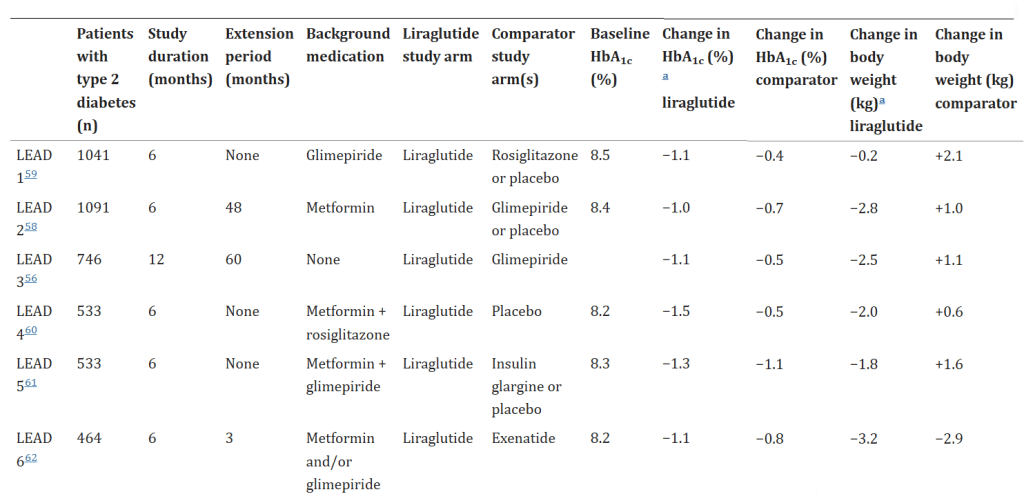
Come per l’Exenatide, la Liraglutide ha un effetto significativo sul peso corporeo, come dimostrano i dati relativi a Liraglutide somministrata a 1,8mg/die. Liraglutide ha ridotto il peso corporeo medio o è stato neutro rispetto al placebo o ai comparatori attivi, in monoterapia (66) e in combinazione con uno (67) o due (68) agenti antidiabete orali. Lo studio LEAD 662 ha esaminato il profilo lipidico con Exenatide e Liraglutide. Sono state osservate riduzioni significative maggiori dei trigliceridi (-0,4 vs -0,2 mM) e degli acidi grassi liberi (-0,17 vs -0,10 mM) nel gruppo Liraglutide. Entrambi i composti hanno causato una riduzione significativa della pressione arteriosa (pressione sistolica -2,2 mmHg e pressione diastolica -1,5 mmHg) senza differenze significative tra i due composti.
Tra gli effetti collaterali si annoverano ipoglicemia, nausea, vertigini, dolore addominale e dolore nel sito di iniezione.[46] Gli effetti collaterali gastrointestinali tendono a essere più forti all’inizio del periodo di trattamento e si attenuano con il tempo.[60] Altri effetti collaterali gravi possono includere angioedema, pancreatite, malattie della cistifellea e problemi renali. L’uso in gravidanza e durante l’allattamento non è sicuro.[46] Una black box warning avverte che nei ratti trattati con Liraglutide sono stati osservati tumori midollari della tiroide, ma è “Sconosciuto se Liraglutide causi tumori delle cellule C della tiroide, incluso il carcinoma midollare della tiroide (MTC), nell’uomo, poiché la rilevanza per l’uomo di tali tumori nei roditori non è stata determinata.”[46]

A proposito del MTC, a esposizioni otto volte superiori a quelle utilizzate nell’uomo, la Liraglutide ha causato un aumento statisticamente significativo dei tumori alla tiroide nei ratti. La rilevanza clinica di questi risultati è sconosciuta.[69] Negli studi clinici, il tasso di tumori alla tiroide nei pazienti trattati con Liraglutide è stato di 1,3 per 1000 anni-paziente (4 persone) rispetto a 1,0 per 1000 pazienti (1 persona) nei gruppi di confronto. L’unica persona nel gruppo di confronto e quattro delle cinque persone nel gruppo Liraglutide avevano marcatori sierici (calcitonina elevata) suggestivi di una malattia preesistente al basale.[69]
L’FDA ha dichiarato che la calcitonina sierica, un biomarcatore del carcinoma midollare della tiroide, era leggermente aumentata nei pazienti con Liraglutide, ma ancora nei limiti della norma, e che era necessario un monitoraggio continuo per 15 anni in un registro dei tumori.[70]
Un altro effetto collaterale preoccupante è rappresentato dalla possibilità (sebbene rara) di sviluppare pancreatite.
Nel 2013, un gruppo della Johns Hopkins ha riportato un’associazione con apparenza statisticamente significativa tra l’ospedalizzazione per pancreatite acuta e un precedente trattamento con derivati del GLP-1 (come la precedentemente vista Exenatide) e inibitori della DPP-4 (come il Sitagliptin).[71] In risposta, la FDA degli Stati Uniti e l’Agenzia Europea per i Medicinali hanno condotto una revisione di tutti i dati disponibili in merito alla possibile connessione tra i mimetici dell’Incretina e la pancreatite o il cancro al pancreas. In una lettera congiunta del 2014 al New England Journal of Medicine, le agenzie hanno concluso che “Un’analisi congiunta dei dati di 14.611 pazienti con diabete di tipo II provenienti da 25 studi clinici nel database di sitagliptin non ha fornito alcuna prova convincente di un aumento del rischio di pancreatite o di cancro al pancreas” e “Entrambe le agenzie concordano sul fatto che le affermazioni relative a un’associazione causale tra i farmaci a base di Incretine e la pancreatite o il cancro al pancreas, espresse di recente nella letteratura scientifica e nei media, non sono coerenti con i dati attuali”. L’FDA e l’EMA non hanno ancora raggiunto una conclusione definitiva su tale relazione causale. Sebbene la totalità dei dati esaminati fornisca rassicurazioni, la pancreatite continuerà a essere considerata un rischio associato a questi farmaci finché non saranno disponibili ulteriori dati; entrambe le agenzie continuano a indagare su questo segnale di sicurezza”[72].
- Albiglutide [approvato nel 2014]
L’Albiglutide (nome commerciale Eperzan in Europa e Tanzeum negli Stati Uniti) è un farmaco agonista del GLP-1 commercializzato da GlaxoSmithKline (GSK) per il trattamento del diabete di tipo II.
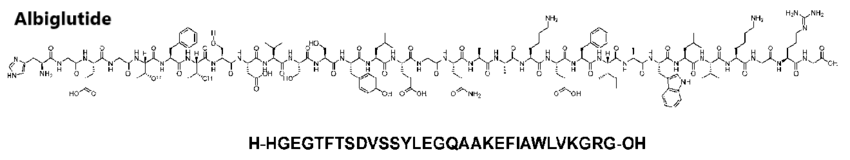
L’Albiglutide è un peptide composto da 645 aminoacidi proteinogenici con 17 ponti disolfuro. Gli aminoacidi 1-30 e 31-60 costituiscono due copie di GLP-1 umano modificato, in cui l’alanina in posizione 2 è stata scambiata con una glicina per migliorare la resistenza alla DPP-4.[73] La sequenza rimanente è costituita da albumina umana.
Viene bioingegnerizzata nel lievito Saccharomyces cerevisiae utilizzando la tecnologia del DNA ricombinante.[74]
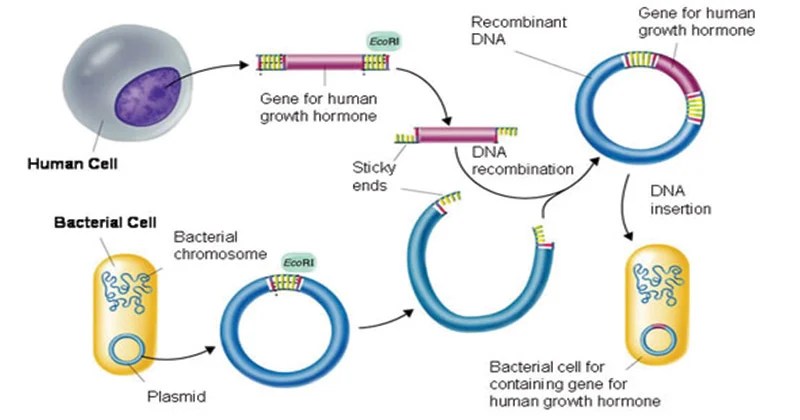
Il farmaco è stato brevettato dalla Human Genome Sciences e sviluppato in collaborazione con GSK.[75]
La GSK ha presentato domanda di approvazione alla FDA statunitense il 14 gennaio 2013 e all’Agenzia europea per i medicinali (EMA) il 7 marzo 2013. Nel marzo 2014, GSK ha ricevuto dalla Commissione Europea l’approvazione per la commercializzazione di Albiglutide con il nome di Eperzan.[76] Nell’aprile 2014, la FDA statunitense ha approvato Albiglutide con il nome di Tanzeum.[77]
Nell’agosto 2017, GSK annunciò l’intenzione di ritirare il farmaco dal mercato mondiale entro luglio 2018 per motivi economici.[78]
L’Albiglutide, come gli altri incretino-mimetici, è stato utilizzato per il trattamento del diabete di tipo II negli adulti. Può essere utilizzato da solo (se la terapia con Metformina è inefficace o non tollerata) o in combinazione con altri farmaci antidiabetici, comprese le forme di Insulina.[74]
Secondo un’analisi del 2015, l’Albiglutide è meno efficace di altri agonisti del GLP-1 per la riduzione dell’HbA1c e la perdita di peso. Sembra inoltre avere meno effetti collaterali rispetto alla maggior parte degli altri farmaci di questa classe, ad eccezione delle reazioni nel sito di iniezione che sono più comuni con Albiglutide rispetto, ad esempio, a Liraglutide.[79]
Dopo l’iniezione sottocutanea, l’Albiglutide raggiunge le massime concentrazioni ematiche dopo tre-cinque giorni. Le concentrazioni allo stato stazionario vengono raggiunte dopo tre-cinque settimane. Essendo resistente alla dipeptidil peptidasi-4 (DPP-4),[73] l’enzima che scompone il GLP-1, l’Albiglutide ha un’emivita biologica di cinque (da quattro a sette) giorni, notevolmente più lunga rispetto agli analoghi del GLP-1 più vecchi, l’Exenatide e la Liraglutide. [80][81] Ciò consente una somministrazione una volta alla settimana,[74] a differenza della Liraglutide ma come la forma a rilascio prolungato dell’Exenatide.
L’Albiglutide agisce come agonista del recettore GLP-1, il che lo rende un tipo di incretino-mimetico. Questo provoca un aumento della secrezione di insulina, soprattutto in presenza di glucosio elevato nel sangue, e rallenta anche lo svuotamento gastrico.[74]
La differenza nel meccanismo d’azione del Albiglutide con gli altri agonisti del recettore del GLP-1, dipende dalla sua struttura la quale rende difficile l’attraversamento della barriera emato-encefalica. Ciò significa che non influisce sul sistema nervoso centrale come altri agonisti del recettore del GLP-1 e potrebbe essere responsabile della limitata perdita di peso osservata con questo farmaco.[81]
- Dulaglutide [approvato nel 2014]
La Dulaglutide, venduta tra l’altro con il nome commerciale Trulicity,[8] è un farmaco utilizzato per il trattamento del diabete di tipo II in combinazione con la dieta e l’esercizio fisico.[83][84] È inoltre approvato negli Stati Uniti per la riduzione degli eventi cardiovascolari avversi maggiori negli adulti con diabete di tipo II che presentano una malattia cardiovascolare conclamata o molteplici fattori di rischio cardiovascolare.[85]
Come per gli altri incretino-mimetici visti in precedenza, la Dulaglutide si lega ai recettori del GLP-1, rallentando lo svuotamento gastrico e aumentando la secrezione di Insulina da parte delle cellule β pancreatiche. Contemporaneamente, il peptide riduce l’elevata secrezione di Glucagone inibendo le cellule α del pancreas, poiché è noto che il Glucagone è elevato in modo inappropriato nei pazienti diabetici.
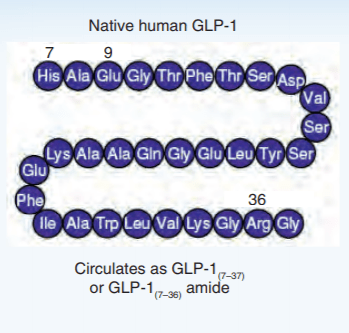
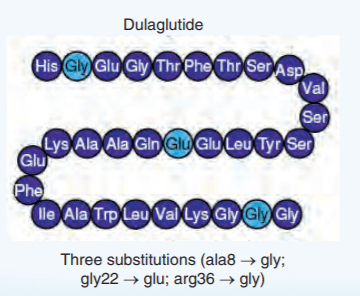
Più precisamente, la Dulaglutide è un agonista del recettore del GLP-1 costituito da GLP-1(7-37) legato covalentemente a un frammento Fc di IgG4 umana.
La sicurezza e l’efficacia della Dulaglutide sono state valutate in sei studi clinici in cui 3.342 soggetti con diabete di tipo II hanno ricevuto Dulaglutide. I soggetti che hanno ricevuto Dulaglutide hanno registrato un miglioramento del controllo glicemico, osservato con riduzioni del livello di HbA1c.[86]
La Food and Drug Administration (FDA) statunitense ha approvato la Dulaglutide con una strategia di valutazione e mitigazione dei rischi (REMS),[86] e ha concesso l’approvazione di Trulicity a Eli Lilly and Company.[86] La REMS consiste in una serie di misure che Eli Lilly adotterà per sensibilizzare i medici sul rischio di pancreatite e sul potenziale rischio di carcinoma midollare della tiroide associato al farmaco.[87]
Nel 2020, la FDA ha approvato due dosi più elevate del farmaco, 3,0mg e 4,5mg, sulla base dei risultati dello studio AWARD-11 che hanno dimostrato una migliore riduzione del glucosio e benefici sul peso.[88]
Il peptide è indicato per gli adulti con diabete di tipo II come aggiunta alla dieta e all’esercizio fisico per migliorare il controllo glicemico. La Dulaglutide non è indicato nel trattamento di soggetti con diabete di tipo I o di pazienti con chetoacidosi diabetica perché questi problemi sono dovuti all’incapacità delle isole pancreatiche di produrre Insulina e una delle azioni della Dulaglutide è quella di stimolare le isole funzionanti a produrre più Insulina. La Dulaglutide può essere utilizzata da solo o in combinazione con altri farmaci per il diabete di tipo II, in particolare Metformina, Sulfoniluree, Tiazolidinedioni e Insulina da assumere contemporaneamente ai pasti.[89]
Il programma di sperimentazione clinica di fase 3 del farmaco ha dimostrato riduzioni dell’emoglobina A1c di circa l’1% con le dosi di 0,75mg e 1,5mg del farmaco, insieme a una perdita di peso media di circa 5Kg. Le dosi più elevate da 3,0mg e 4,5mg, approvate nel 2020, hanno dimostrato riduzioni dell’emoglobina A1c più vicine all’1,5% e una perdita di peso leggermente superiore.[90]
Una meta-analisi del 2017 non ha supportato l’ipotesi che il trattamento con agonisti del GLP-1 o inibitori della DPP-4 aumenti la mortalità per tutte le cause nei diabetici di tipo II.[91]
La Dulaglutide viene assorbita lentamente dopo l’iniezione sottocutanea. In uno studio farmacocinetico condotto su 20 adulti sani, la Cmax si è verificata entro 24-48 ore dalla somministrazione. La biodisponibilità assoluta media di Dulaglutide dopo iniezioni sottocutanee di dosi singole da 0,75mg e 1,5mg è stata rispettivamente del 65% e del 47%. L’emivita media della Dulaglutide somministrato a varie dosi è stata di circa 3,75 giorni (89,9 ore). Questa emivita prolungata consente la somministrazione una volta alla settimana. Le informazioni di prescrizione indicano un’emivita di circa 5 giorni.
Gli effetti collaterali più comuni includono disturbi gastrointestinali, come dispepsia, inappetenza, nausea, vomito, dolore addominale, diarrea.[92] Alcuni pazienti possono manifestare reazioni avverse gravi: pancreatite acuta (i sintomi includono dolore addominale persistente e grave, che talvolta si irradia alla schiena ed è accompagnato da vomito), ipoglicemia, insufficienza renale (che talvolta può richiedere l’emodialisi). Il rischio di ipoglicemia aumenta se il farmaco è usato in combinazione con Sulfoniluree o Insulina.[93][94] Esiste anche un rischio potenziale di carcinoma midollare della tiroide associato all’uso del farmaco.[87]
- Lixisenatide [approvato nel 2016]
La Lixisenatide (nome commerciale Lyxumia nell’Unione Europea e Adlyxin negli Stati Uniti e prodotto da Sanofi) è un agonista del recettore GLP-1 iniettabile una volta al giorno per il trattamento del diabete di tipo II.
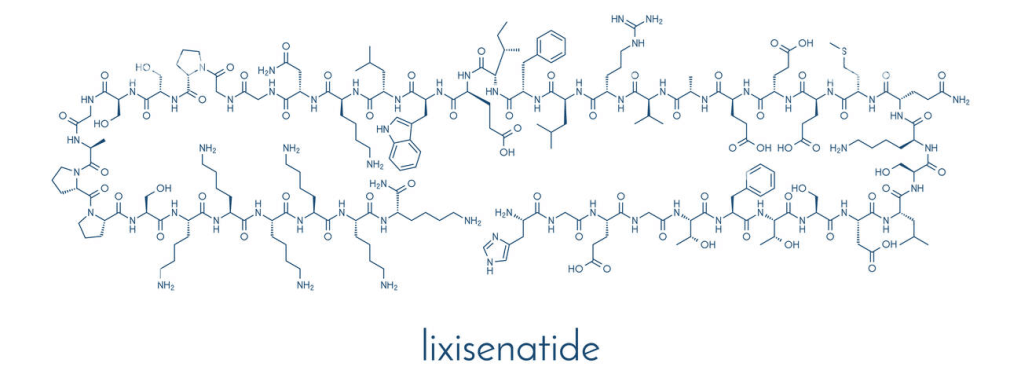
È stato sintetizzato dalla danese Zealand Pharma A/S;[95] nel 2003 Zealand lo ha concesso in licenza a Sanofi, che ha sviluppato il farmaco.[96] La Lixisenatide è stata approvata dalla Commissione europea nel febbraio 2013.
La Lixisenatide è un peptide composto da 44 aminoacidi, con un gruppo amidico sul suo terminale C.[97]
E’ stata descritta come “des-38-prolina-exendin-4 (Heloderma suspectum)-(1-39)-peptidilpenta-L-lisil-L-lisinamide”, ovvero è derivata dai primi 39 aminoacidi della sequenza del peptide exendin-4, isolato dal veleno del “mostro di Gila”, omettendo la Prolina in posizione 38 e aggiungendo sei residui di Lisina. La sua sequenza completa è:
H–His–Gly–Glu–Gly–Thr–Phe–Thr–Ser–Asp–Leu–Ser–Lys–Gln–Met–Glu–Glu–Glu–Ala–Val–Arg–Leu–Phe–Ile–Glu–Trp–Leu–Lys–Asn–Gly–Gly–Pro–Ser–Ser–Gly–Ala–Pro–Pro–Ser–Lys–Lys–Lys–Lys–Lys–Lys–NH2
La Lixisenatide, appartenendo alla classe dei farmaci agonisti del GLP-1, come per i precedentemente trattati composti agisce rallentando lo svuotamento gastrico e aumentando la secrezione di Insulina da parte delle cellule β pancreatiche.
I risultati di una ricerca condotta da McClean PL et al. hanno dimostrato che la Liraglutide e la Lixisenatide sono promettenti come potenziali trattamenti farmacologici della malattia di Alzheimer AD. La Lixisenatide è risultata ugualmente efficace a una dose inferiore rispetto alla Liraglutide in alcuni dei parametri misurati dopo dieci settimane di iniezioni intraperitoneali giornaliere di Liraglutide (2,5 o 25 nmol/kg) o Lixisenatide (1 o 10 nmol/kg) o soluzione fisiologica in topi APP/PS1 a un’età in cui le placche amiloidi si erano già formate. Analizzando la plasticità sinaptica nell’ippocampo, l’LTP è stato fortemente aumentato nei topi APP/PS1 da entrambi i farmaci, con maggiore efficacia con la Lixisenatide. La riduzione del numero di sinapsi osservata nei topi APP/PS1 è stata evitata dai due farmaci. Il carico di placche amiloidi e il carico di placche Congo rosso positivo a nucleo denso nella corteccia sono stati ridotti da entrambi i farmaci a tutte le dosi. Anche la risposta infiammatoria cronica (attivazione microgliale) è stata ridotta da tutti i trattamenti.[98]
Cai HY et al. hanno dimostrato in uno studio che la lixisenatide è in grado di ridurre le placche amiloidi, i grovigli neurofibrillari e la neuroinfiammazione negli ippocampi di topi femmina APP/PS1/tau di 12 mesi; l’attivazione della via di segnalazione PKA-CREB e l’inibizione della p38-MAPK potrebbero essere i meccanismi importanti nella funzione neuroprotettiva della lixisenatide. Pertanto, la lixisenatide potrebbe avere il potenziale per essere sviluppata come nuova terapia per l’AD. [99] Liu Wet al hanno trovato risultati interessanti confrontando exendin-4 (10 nmol/kg), liraglutide (25 nmol/kg) e lixisenatide (10 nmol/kg): è emerso che exendin-4 non ha mostrato effetti protettivi alla dose scelta, mentre sia liraglutide che lixisenatide hanno mostrato effetti nel prevenire la compromissione motoria indotta da MPTP (Rotarod, locomozione in campo aperto, test di catalessi), la riduzione dei livelli di tirosina idrossilasi (TH) (sintesi di dopamina) nella substantia nigra e nei gangli della base, una riduzione della molecola di segnalazione pro-apoptotica BAX e un aumento della molecola di segnalazione anti-apoptotica B-cell lymphoma-2. I risultati precedenti dimostrano che sia la liraglutide che la lixisenatide sono superiori all’exendin-4 ed entrambi i farmaci sono promettenti come nuovo trattamento della malattia di Parkinson.[100]
Un altro studio condotto da Kerry Hunter et al. ha analizzato gli agonisti del recettore GLP-1 liraglutide e lixisenatide. Sono state valutate le cinetiche di attraversamento della barriera ematoencefalica (BBB), l’attivazione del GLP-1R attraverso la misurazione dei livelli di cAMP e gli effetti fisiologici nel cervello sulla proliferazione delle cellule staminali neuronali e sulla neurogenesi. Entrambi i farmaci sono stati in grado di attraversare la BBB. La lixisenatide ha attraversato la BBB a tutte le dosi testate (2,5, 25 o 250 nmol/kg ip.) quando misurate 30 minuti dopo l’iniezione e a 2,5-25 nmol/kg ip. 3 ore dopo l’iniezione. La lixisenatide ha anche aumentato la neurogenesi nel cervello. La liraglutide ha attraversato la BBB a 25 e 250 nmol/kg ip. ma nessun aumento è stato rilevato a 2,5 nmol/kg ip. 30 minuti dopo l’iniezione, e a 250 nmol/kg ip. a 3 ore dopo l’iniezione. Liraglutide e lixisenatide hanno aumentato i livelli di cAMP nel cervello, con lixisenatide più efficace. I risultati precedenti suggeriscono che questi nuovi analoghi dell’incretina attraversano la BBB mostrando attività fisiologica e neurogenesi nel cervello, il che li rende buoni candidati per essere utilizzati come trattamento delle malattie neurodegenerative.[101]
Anche la Lixisenatide è utilizzata come coadiuvante della dieta e dell’esercizio fisico per il trattamento del diabete di tipo II.[97] Nell’Unione Europea il suo uso è limitato all’integrazione della terapia Insulinica.[102][103] Al 2017 non è chiaro se influisca sul rischio di morte di una persona.[104]
Viene fornito in un autoiniettore contenente quattordici dosi e viene iniettato per via sottocutanea.[97]
La Lixisenatide non deve essere utilizzata da persone che hanno problemi di svuotamento gastrico.[97] La Lixisenatide ritarda lo svuotamento gastrico, il che può modificare la velocità con cui altri farmaci assunti oralmente esplicano la loro efficacia.[97]
Dopo la somministrazione sottocutanea nell’uomo, la Lixisenatide mostra una farmacocinetica lineare e un’emivita di eliminazione dipendente dall’assorbimento di 2-3 ore.
La dose iniziale di Lixisenatide è di 10mcg una volta al giorno, per 14 giorni. La dose di mantenimento è successivamente di 20mcg una volta al giorno nell’ora che precede il primo pasto della giornata o il pasto serale.
In circa lo 0,1% dei casi le persone hanno avuto reazioni anafilattiche alla lixisenatide e in circa lo 0,2% dei casi il farmaco ha causato pancreatite.[97] L’uso con insulina o sulfonilurea può causare ipoglicemia.[97] In alcuni casi, persone senza malattie renali hanno avuto lesioni renali acute e in alcune persone con malattie renali esistenti la condizione è peggiorata. Poiché la Lixisenatide è un peptide, le persone possono sviluppare una risposta immunitaria nei suoi confronti che finirà per rendere il farmaco inefficace; le persone che hanno sviluppato anticorpi contro la Lixisenatide tendono ad avere una maggiore infiammazione nel sito di iniezione.[97]
Almeno il 5% delle persone ha avuto nausea, vomito, diarrea, mal di testa o vertigini dopo l’assunzione di Lixisenatide.[97]
- Semaglutide [approvata nel 2017]

La Semaglutide è chimicamente simile al GLP-1 umano.[105-41] Mancano i primi sei aminoacidi del GLP-1.[105] Le sostituzioni sono effettuate nelle posizioni 8 e 34 del GLP-1 (posizioni 2 e 28 della Semaglutide), dove l’Alanina e la Lisina sono sostituite rispettivamente dall’acido 2-aminoisobutirrico e dall’Arginina. La sostituzione dell’Alanina impedisce la degradazione chimica da parte della dipeptidil peptidasi-4.[106] La Lisina in posizione 26 del GLP-1 (posizione 20 del Semaglutide) ha una lunga catena attaccata, che termina con una catena di 17 atomi di carbonio e un gruppo carbossilico.[106] Ciò aumenta il legame del farmaco con le proteine trasportatrici nel sangue (albumina), consentendo una più lunga presenza nella circolazione sanguigna.[106]
L’emivita del Semaglutide nel sangue è di circa sette giorni (165-184 ore).
Come per gli altri incretino-mimetici, la Semaglutide è un agonista del recettore del GLP -1.[107][108][109] Il farmaco riduce i livelli di glucosio nel sangue. Sembra inoltre che aumenti la crescita delle cellule β pancreatiche, responsabili della produzione e del rilascio di Insulina.[110][111] Inoltre, inibisce la produzione di Glucagone, l’ormone che aumenta la glicogenolisi (rilascio dei carboidrati immagazzinati dal fegato) e la Gluconeogenesi (sintesi di nuovo glucosio). Riduce l’assunzione di cibo abbassando l’appetito e rallentando la digestione nello stomaco e suo svuotamento,[112] contribuendo a ridurre il peso corporeo.[113][114]
Nel giugno 2008 è stato avviato uno studio clinico di fase II al fine di esaminare la Semaglutide come terapia per il diabete da somministrare una volta alla settimana, come alternativa ad azione prolungata alla Liraglutide .[115][116] Gli studi clinici sono iniziati nel gennaio 2016 e si sono conclusi nel maggio 2017.[117][118]
Nel giugno 2021, una versione iniettabile a dosaggio più elevato, venduta con il marchio Wegovy, è stata approvata dalla Food and Drug Administration (FDA) statunitense come farmaco anti-obesità per la gestione del peso a lungo termine negli adulti.[119-15] Nel novembre 2021, il Comitato per i Medicinali per Uso Umano (CHMP) dell’Agenzia Europea per i Medicinali (EMA) ha raccomandato di concedere a Novo Nordisk A/S l’autorizzazione all’immissione in commercio di Wegovy[120]. Nel gennaio 2022, Wegovy è stato approvato per uso medico nell’Unione Europea.[121]
Nel gennaio 2023, l’etichetta di Rybelsus è stata aggiornata per indicare che può essere utilizzato come trattamento di prima linea per gli adulti con diabete di tipo 2.[122]
Nel marzo 2021, in uno studio di fase III randomizzato, in doppio cieco, 1.961 adulti con un indice di massa corporea pari o superiore a 30 sono stati assegnati, in un rapporto 2:1, a un trattamento con Semaglutide sottocutaneo una volta alla settimana o placebo, più un intervento sullo stile di vita. Gli studi si sono svolti in 129 siti in 16 Paesi di Asia, Europa, Nord America e Sud America. La variazione percentuale media del peso corporeo alla settimana 68 è stata di -14,9% nel gruppo Semaglutide contro -2,4% con placebo, per una differenza di trattamento stimata di -12,4 punti percentuali (95% CI, da -13,4 a -11,5).[123][124][125][126]
Una revisione dei trattamenti anti-obesità del 2022 ha rilevato che il Semaglutide e la Tirzepatide (che ha un meccanismo d’azione sovrapponibile) erano più promettenti dei precedenti farmaci anti-obesità, anche se meno efficaci della chirurgia bariatrica.[127]
Nel marzo 2023, un funzionario di Novo Nordisk ha dichiarato che i pazienti che utilizzano la Semaglutide per perdere peso possono riacquistare il peso originario entro 5 anni dall’interruzione del trattamento.[128]
Nel marzo 2024, l’FDA ha esteso l’indicazione di Semaglutide (Wegovy) per ridurre il rischio di morte cardiovascolare, infarto e ictus in adulti con malattie cardiovascolari e obesità o sovrappeso. L’efficacia e la sicurezza di questa nuova indicazione sono state studiate in uno studio multinazionale, multicentrico, in doppio cieco, controllato con placebo, che ha assegnato in modo casuale oltre 17.600 partecipanti a ricevere Semaglutide (Wegovy) o placebo.[129] I partecipanti di entrambi i gruppi hanno ricevuto anche un trattamento medico standard (ad es, Semaglutide (Wegovy) ha ridotto significativamente il rischio di eventi cardiovascolari avversi maggiori (morte cardiovascolare, infarto e ictus), che si sono verificati nel 6,5% dei partecipanti che hanno ricevuto Semaglutide (Wegovy) rispetto all’8% dei partecipanti che hanno ricevuto placebo.[129]
Una meta-analisi del 2014 ha rilevato che la Semaglutide può essere efficace nell’abbassare gli enzimi epatici (transaminite) e nel migliorare alcune caratteristiche radiologicamente osservate della malattia epatica steatotica associata a disfunzione metabolica.[130]
Nel luglio 2023, l’Agenzia islandese per i medicinali ha segnalato due casi di pensieri suicidi e un caso di autolesionismo tra i consumatori del farmaco, inducendo a valutare la sicurezza di Ozempic,[131] Wegovy, Saxenda e altri farmaci simili.[132] Nel gennaio 2024, una revisione preliminare condotta dalla FDA ha confermato che non sono state trovate prove che suggeriscano che il farmaco causi pensieri o azioni suicide.[133][134]
La Semaglutide ha dimostrato di poter ridurre l’interesse per il consumo di alcol tra gli utilizzatori. Gli scienziati ipotizzano che il Semaglutide possa influenzare le regioni cerebrali coinvolte nella dipendenza e nella regolazione dell’appetito, sebbene i meccanismi esatti siano ancora in fase di studio. La ricerca sugli animali ha indicato che farmaci simili alla Semaglutide possono ridurre l’assunzione di alcolici.[135]
La Semaglutide e farmaci simili, come la Dulaglutide e la Liraglutide, sono stati utilizzati per trattare il disturbo da alimentazione incontrollata (BED), in quanto possono minimizzare i pensieri ossessivi sul cibo e gli impulsi ad abbuffarsi.[136][137] Alcuni utilizzatori di questi farmaci hanno riferito di aver ridotto in modo significativo quello che è colloquialmente noto come “food noise” (pensieri costanti e inarrestabili di mangiare nonostante non si abbia fisicamente fame), che può essere un fattore di BED.[138][139]
Attualmente, la Semaglutide indicata come coadiuvante della dieta e dell’esercizio fisico per migliorare il controllo glicemico negli adulti con diabete di tipo II.[140][141]
La formulazione a dosi più elevate di Semaglutide è indicata come coadiuvante della dieta e dell’esercizio fisico per la gestione del peso a lungo termine negli adulti con obesità (indice di massa corporea (IMC) iniziale ≥ 30 kg/m2) o in sovrappeso (IMC iniziale ≥ 27 kg/m2) e con almeno una comorbidità correlata al peso.[142]
Nel marzo 2024, la Food and Drug Administration (FDA) statunitense ha ampliato l’indicazione di Semaglutide (Wegovy), in combinazione con una dieta a ridotto contenuto calorico e un aumento dell’attività fisica, per ridurre il rischio di morte cardiovascolare, infarto e ictus in adulti obesi o in sovrappeso con malattie cardiovascolari.[143]
La dose iniziale è di 0,25mg di Semaglutide una volta alla settimana. Dopo 4 settimane, la dose deve essere aumentata a 0,5 mg una volta alla settimana. Dopo almeno 4 settimane con una dose da 0,5 mg una volta alla settimana, la dose può essere aumentata a 1 mg una volta alla settimana per migliorare ulteriormente il controllo glicemico. Dopo almeno 4 settimane con una dose da 1 mg una volta alla settimana, la dose può essere aumentata a 2 mg una volta alla settimana per migliorare ulteriormente il controllo glicemico.
Semaglutide 0,25mg non è una dose di mantenimento. Non sono raccomandate dosi superiori a 2 mg alla settimana.
Quando Ozempic viene aggiunto alla terapia in atto a base di Metformina e/o Tiazolidinedione o dell’ inibitore del cotrasportatore sodio-glucosio (SGLT2), la dose di Metformina e/o Tiazolidinedione o dell’inibitore SGLT2 può essere mantenuta senza variazioni.
Quando Ozempic viene aggiunto alla terapia in atto con Sulfanilurea o con un’insulina, è necessario considerare una riduzione della dose di Sulfanilurea o di insulina per ridurre il rischio di ipoglicemia (vedere paragrafi 4.4 e 4.8).
Non è necessario automonitorare la glicemia per aggiustare la dose di Ozempic. L’auto-monitoraggio della glicemia è necessario per correggere la dose di Sulfanilurea e insulina, in particolare quando si inizia Ozempic e si riduce l’insulina. Si raccomanda un approccio graduale alla riduzione dell’insulina.
Similmente agli altri incretino-mimetici, possibili effetti avversi con l’uso di questo peptide includono nausea, diarrea, vomito, costipazione, dolore addominale, cefalea, affaticamento, indigestione/bruciore di stomaco, vertigini, distensione addominale, eruttazioni, ipoglicemia (basso livello di glucosio nel sangue) nelle persone con diabete di tipo II (ma non limitato ad esse), flatulenza, gastroenterite e malattia da reflusso gastroesofageo (GERD). In passato è stato sospettato di causare pancreatite e può causare gastroparesi e ostruzione intestinale.[144]Tra le persone a cui è stato prescritto un agonista del recettore del GLP-1, lo 0,1% ha ricevuto una diagnosi di gastroparesi. L’1% ha ricevuto una diagnosi di gastroparesi almeno sei mesi dopo, il che equivale a un aumento del 52% del rischio di diagnosi di gastroparesi durante l’assunzione di un farmaco di questa classe.[145] Una meta-analisi del 2019 non ha indicato un rischio significativamente elevato di pancreatite acuta.[146]Secondo il sistema di segnalazione degli eventi avversi dell’FDA (FAERS), più di 150 pazienti che assumevano Ozempic hanno riportato ileo o ostruzioni intestinali dopo l’assunzione del farmaco.[147]
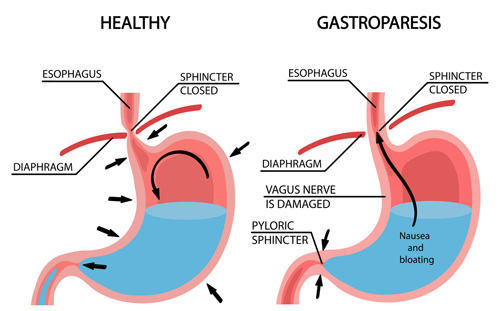
L’etichetta dell’FDA statunitense per il Semaglutide contiene un boxed warning per i tumori della tiroide a cellule C nei roditori.[148] Non è noto se il Semaglutide causi tumori della tiroide a cellule C, incluso il carcinoma midollare della tiroide, nell’uomo.[149]
- Tirzepatide [approvato nel 2022]
La Tirzepatide è un farmaco antidiabetico utilizzato per il trattamento del diabete di tipo II [150][151][152][153] e per la perdita di peso.[154][155] La Tirzepatide viene somministrata tramite iniezioni sottocutanee.[150][151] Viene venduta con i marchi Mounjaro per il trattamento del diabete,[150] e Zepbound per la perdita di peso.[154] La Tirzepatide è un agonista del recettore del GIP e del GLP-1.[154]
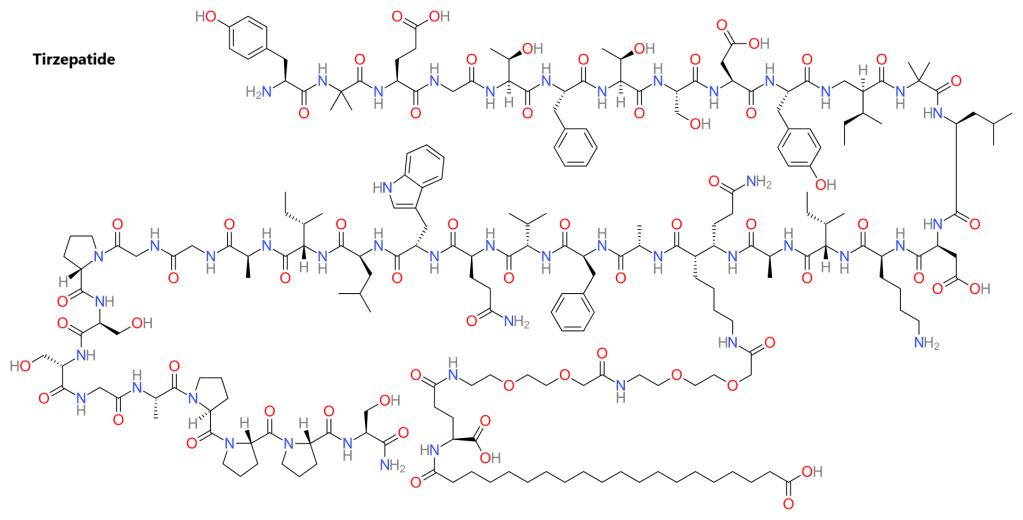
La sintesi della Tirzepatide è stata divulgata per la prima volta nei brevetti depositati da Eli Lilly and Company.[156] Questa utilizza la sintesi standard di peptidi in fase solida, con un gruppo protettivo allilossicarbonilico sulla Lisina in posizione 20 della catena lineare degli amminoacidi, consentendo una serie finale di trasformazioni chimiche in cui l’ammina della catena laterale di tale Lisina viene derivatizzata con il frammento contenente lipidi.
Per questo composto sono stati riportati processi di produzione su larga scala.[157]
La Tirzepatide è un analogo dell’ormone GIP umano con una porzione diacidica grassa C20, utilizzata per ottimizzare l’assorbimento e il metabolismo del composto.[158] La sezione diacidica grassa (acido eicosanedioico) è legata tramite un acido glutammico e due unità di acido (2-(2-aminoetossi)etossico)acetico alla catena laterale del residuo di Lisina. Questa disposizione consente un’emivita molto più lunga, prolungando il tempo tra una dose e l’altra, grazie alla sua elevata affinità con l’albumina.[159]
Quindi, la Tirzepatide è un polipeptide lineare di 39 aminoacidi che è stato modificato chimicamente mediante lipidazione per migliorarne l’assorbimento nelle cellule e la stabilità al metabolismo.[158] Ha completato la sperimentazione di fase III a livello globale nel 2021.[160][161]
La Tirzepatide ha un’affinità maggiore per i recettori GIP rispetto ai recettori GLP-1 e questo comportamento da doppio agonista ha dimostrato di produrre una maggiore riduzione dell’iperglicemia rispetto a un agonista selettivo dei recettori GLP-1.[162] Studi di segnalazione hanno riportato che la Tirzepatide imita le azioni del GIP naturale sul recettore GIP. [Studi di segnalazione hanno riportato che la Tirzepatide imita le azioni del GIP naturale sul recettore del GIP.[163] Tuttavia, sul recettore del GLP-1, la Tirzepatide mostra una predilezione per la generazione di cAMP (un messaggero associato alla regolazione del metabolismo del glicogeno, degli zuccheri e dei lipidi), piuttosto che per il reclutamento della β-arrestina. Questa combinazione di preferenza verso il recettore GIP e di proprietà di segnalazione distinte del GLP-1 suggerisce che questo agonismo distorto aumenta la secrezione di Insulina.[163] È stato riportato che la Tirzepatide aumenta i livelli di adiponectina, un’adipochina coinvolta nella regolazione del metabolismo del glucosio e dei lipidi, con un aumento massimo del 26% rispetto al basale dopo 26 settimane, al dosaggio di 10mg.[162]
Negli studi preliminari finanziati dall’industria che hanno confrontato la Tirzepatide con la Semaglutide, la Tirzepatide ha mostrato un miglioramento minore delle riduzioni (2,01%-2,30% a seconda del dosaggio) nei test dell’emoglobina glicata rispetto alla Semaglutide (1,86%). [164] Una dose di 10mg si è dimostrata efficace anche nel ridurre l’insulino-resistenza, con una riduzione di circa l’8% rispetto al basale, misurata utilizzando l’HOMA2-IR (calcolato con l’Insulina a digiuno).[162] I livelli a digiuno delle proteine che legano l’IGF, come IGFBP1 e IGFBP2, sono aumentati in seguito al trattamento con Tirzepatide, aumentando la sensibilità all’Insulina.[162]
Una meta-analisi del 2021 ha mostrato che, nell’arco di un anno di utilizzo clinico, la Tirzepatide è risultata superiore a Dulaglutide, Semaglutide, Degludec e Insulina glargine per quanto riguarda l’efficacia glicemica e la riduzione dell’obesità.[165]
In uno studio di fase III, in doppio cieco, randomizzato e controllato, sostenuto da Eli Lilly, adulti non diabetici con un indice di massa corporea pari o superiore a 30, o pari o superiore a 27 e almeno una complicazione correlata al peso, escluso il diabete, sono stati randomizzati a ricevere Tirzepatide sottocutanea una volta alla settimana (5mg, 10mg o 15mg) o placebo. La variazione percentuale media del peso alla settimana 72 è stata di -15,0% (intervallo di confidenza [IC] al 95%, da -15,9 a -14,2) con dosi settimanali di Tirzepatide di 5mg, -19,5% (IC al 95%, da -20,4 a -18,5) con dosi di 10mg e -20,9% (IC al 95%, da -21,8 a -19,9) con dosi di 15mg. La variazione di peso nel gruppo placebo è stata del -3,1% (95% CI, da -4,3 a -1,9).[166][167][168]
La Tirzepatide è stata approvata per uso medico nell’Unione Europea nel settembre 2022.[169][170]
La dose iniziale di Tirzepatide è 2,5mg una volta a settimana. Dopo 4 settimane, la dose deve essere aumentata a 5mg una volta a settimana. Se necessario, è possibile aumentare la dose con incrementi di 2,5mg dopo un minimo di 4 settimane con la dose in uso.
Le dosi di mantenimento raccomandate sono 5mg, 10mg e 15mg.
La dose massima è 15mg una volta a settimana.
Quando Tirzepatide viene aggiunto alla terapia esistente con Metformina e/o inibitore del co- trasportatore di sodio-glucosio 2 (SGLT2i), può essere mantenuta la dose in uso di Metformina e/o SGLT2i.
Quando Tirzepatide viene aggiunto alla terapia esistente con una sulfonilurea e/o Insulina, si può considerare una riduzione della dose di sulfonilurea o Insulina per ridurre il rischio di ipoglicemia. L’automonitoraggio della glicemia è necessario per aggiustare la dose di sulfonilurea e Insulina. Si raccomanda un approccio graduale per la riduzione dell’Insulina.
Gli studi preclinici, di fase I e clinici di fase II hanno indicato che la Tirzepatide presenta effetti avversi simili a quelli di altri agonisti del recettore GLP-1, come visto in precedenza. Questi effetti si verificano in gran parte a livello del tratto gastrointestinale.[171] I più frequentemente osservati sono nausea, diarrea e vomito, la cui incidenza è aumentata con l’entità del dosaggio (cioè la probabilità è maggiore quanto più alta è la dose). Anche il numero di pazienti che hanno interrotto l’assunzione di Tirzepatide è aumentato con l’aumentare del dosaggio: i pazienti che assumevano 15mg avevano un tasso di interruzione del 25% rispetto al 5,1% dei pazienti che assumevano 5mg e all’11,1% di quelli che assumevano Dulaglutide.[172] In misura leggermente minore, i pazienti hanno anche riferito una riduzione dell’appetito.[171] Altri effetti collaterali segnalati sono stati dispepsia, costipazione, dolore addominale, vertigini e ipoglicemia.[173][174]
Uso off-label e “ricreativo”:
Oltre ai loro usi medici, gli agonisti del GLP-1 hanno visto una massiva diffusione in ambito della perdita di peso a fini “estetici” nel Fitness e in parte nel BodyBuilding, resa popolare da influencer e celebrità.[175] I venditori del mercato nero offrono online prodotti non autorizzati che si spacciano per agonisti del GLP-1. Questa pratica è illegale sia negli Stati Uniti che in Europa, ma alcuni acquirenti si rivolgono a rivenditori non autorizzati perché non hanno la possibilità di farsi prescrivere legalmente il farmaco.[176][177][178][179][180] Gli acquirenti, ovviamente, corrono rischi dovuti a farmaci contraffatti o di qualità inferiore venduti da soggetti non autorizzati.[181]
L’uso, le modalità di applicazione e le limitazioni degli incretino-mimetici in campo “cosmetico” saranno riportate nella seconda parte…
Gabriel Bellizzi [CEO BioGenTech]
Riferimenti:
- Reynolds M. “What the Scientists Who Pioneered Weight-Loss Drugs Want You to Know”. Wired. ISSN 1059-1028. Archived from the original on 15 May 2024. Retrieved 15 May 2024.
- Müller MU, Preker A (4 January 2024). “Interview with Weight Loss Drugs Inventor Lotte Bjerre Knudsen: “I’m Experimenting with Periodic Fasting””. Der Spiegel. ISSN 2195-1349. Archived from the original on 25 August 2024. Retrieved 15 May 2024.
- Holst JJ. The physiology of glucagon-like peptide 1. Physiol Rev. 2007;87:1409–1439. [PubMed] [Google Scholar]
- Nauck MA, Homberger E, Siegel EG, et al. Incretin effects of increasing glucose loads in man calculated from venous insulin and C-peptide responses. J Clin Endocrinol Metab. 1986;63:492–498. [PubMed] [Google Scholar]
- Brown JC, Mutt V, Pederson RA. Further purification of a polypeptide demonstrating enterogastrone activity. J Physiol. 1970;209:57–64. [PMC free article] [PubMed] [Google Scholar]
- Deacon CF, Johnsen AH, Holst JJ. Degradation of glucagon-like peptide-1 by human plasma in vitro yields an N-terminally truncated peptide that is a major endogenous metabolite in vivo. J Clin Endocrinol Metab. 1995;80:952–957. [PubMed] [Google Scholar]
- Vilsboll T, Agerso H, Lauritsen T, et al. The elimination rates of intact GIP as well as its primary metabolite, GIP 3–42, are similar in type 2 diabetic patients and healthy subjects. Regul Pept. 2006;137:168–172. [PubMed] [Google Scholar]
- Drucker DJ. The biology of incretin hormones. Cell Metab. 2006;3:153–165. [PubMed] [Google Scholar]
- Orskov C, Holst JJ, Poulsen SS, Kirkegaard P. Pancreatic and intestinal processing of proglucagon in man. Diabetologia. 1987;30:874–881. [PubMed] [Google Scholar]
- Orci L, Bordi C, Unger RH, Perrelet A. Glucagon- and glicentin-producing cells. In: Lefebvre PJ, editor. Glucagon. Berlin: Springer Verlag; 1983. pp. 57–79. [Google Scholar]
- Goke R, Larsen PJ, Mikkelsen JD, Sheikh SP. Distribution of GLP-1 binding sites in the rat brain: evidence that exendin-4 is a ligand of brain GLP-1 binding sites. Eur J Neurosci. 1995;7:2294–2300. [PubMed] [Google Scholar]
- Flint A, Raben A, Astrup A, Holst JJ. Glucagon-like peptide 1 promotes satiety and suppresses energy intake in humans. J Clin Invest. 1998;101:515–520. [PMC free article] [PubMed] [Google Scholar]
- Gros R, You X, Baggio LL, et al. Cardiac function in mice lacking the glucagon- like peptide-1 receptor. Endocrinology. 2003;144:2242–2252. [PubMed] [Google Scholar]
- Meier JJ, Gethmann A, Gotze O, et al. Glucagon-like peptide 1 abolishes the postprandial rise in triglyceride concentrations and lowers levels of non-esterified fatty acids in humans. Diabetologia. 2006;49:452–458. [PubMed] [Google Scholar]
- Carraro-Lacroix LR, Malnic G, Girardi AC. Regulation of Na+/H+ exchanger NHE3 by glucagon-like peptide 1 receptor agonist exendin-4 in renal proximal tubule cells. Am J Physiol Renal Physiol. 2009;297:F1647–F1655. [PubMed] [Google Scholar]
- Gault VA, O’Harte FP, Flatt PR. Glucose-dependent insulinotropic polypeptide (GIP): anti-diabetic and anti-obesity potential? Neuropeptides. 2003;37:253–263. [PubMed] [Google Scholar]
- Tsukiyama K, Yamada Y, Yamada C, et al. Gastric inhibitory polypeptide as an endogenous factor promoting new bone formation after food ingestion. Mol Endocrinol. 2006;20:1644–1651. [PubMed] [Google Scholar]
- Knop FK, Vilsboll T, Hojberg PV, et al. Reduced incretin effect in type 2 diabetes: cause or consequence of the diabetic state? Diabetes. 2007;56:1951–1959. [PubMed] [Google Scholar]
- Nauck M, Stockmann F, Ebert R, Creutzfeldt W. Reduced incretin effect in type 2 (non-insulin-dependent) diabetes. Diabetologia. 1986;29:46–52. [PubMed] [Google Scholar]
- Bagger JO, Knop FK, Lund A, Vestergaard H, Holst JJ, Vilsboll T. Impaired Regulation of the Incretin Effect in Patients with Type 2 Diabetes Mellitus. Diabetes. 2010;58 (Suppl 1):A369. [PubMed] [Google Scholar]
- Vilsboll T, Krarup T, Deacon CF, Madsbad S, Holst JJ. Reduced postprandial concentrations of intact biologically active glucagon-like peptide 1 in type 2 diabetic patients. Diabetes. 2001;50:609–613. [PubMed] [Google Scholar]
- Kjems LL, Holst JJ, Volund A, Madsbad S. The influence of GLP-1 on glucose-stimulated insulin secretion: effects on beta-cell sensitivity in type 2 and nondiabetic subjects. Diabetes. 2003;52:380–386. [PubMed] [Google Scholar]
- Nauck MA, Heimesaat MM, Orskov C, Holst JJ, Ebert R, Creutzfeldt W. Preserved incretin activity of glucagon-like peptide 1 [7–36 amide] but not of synthetic human gastric inhibitory polypeptide in patients with type-2 diabetes mellitus. J Clin Invest. 1993;91:301–307. [PMC free article] [PubMed] [Google Scholar]
- Nauck MA, Kleine N, Orskov C, Holst JJ, Willms B, Creutzfeldt W. Normalization of fasting hyperglycaemia by exogenous glucagon-like peptide 1 (7–36 amide) in type 2 (non-insulin-dependent) diabetic patients. Diabetologia. 1993;36:741–744. [PubMed] [Google Scholar]
- Raufman JP (January 1996). “Bioactive peptides from lizard venoms”. Regulatory Peptides. 61 (1): 1–18. doi:10.1016/0167-0115(96)00135-8. PMID 8701022. S2CID 5293453.
- Koole C, Reynolds CA, Mobarec JC, Hick C, Sexton PM, Sakmar TP (April 2017). “Genetically encoded photocross-linkers determine the biological binding site of exendin-4 peptide in the N-terminal domain of the intact human glucagon-like peptide-1 receptor (GLP-1R)”. The Journal of Biological Chemistry. 292 (17): 7131–7144. doi:10.1074/jbc.M117.779496. PMC 5409479. PMID 28283573.
- Bunck MC, Diamant M, Cornér A, Eliasson B, Malloy JL, Shaginian RM, et al. (May 2009). “One-year treatment with exenatide improves beta-cell function, compared with insulin glargine, in metformin-treated type 2 diabetic patients: a randomized, controlled trial”. Diabetes Care. 32 (5): 762–768. doi:10.2337/dc08-1797. PMC 2671094. PMID 19196887.
- Ding X, Saxena NK, Lin S, Gupta NA, Gupta N, Anania FA (January 2006). “Exendin-4, a glucagon-like protein-1 (GLP-1) receptor agonist, reverses hepatic steatosis in ob/ob mice”. Hepatology. 43 (1): 173–181. doi:10.1002/hep.21006. PMC 2925424. PMID 16374859.
- Ali ES, Hua J, Wilson CH, Tallis GA, Zhou FH, Rychkov GY, et al. (September 2016). “The glucagon-like peptide-1 analogue exendin-4 reverses impaired intracellular Ca(2+) signalling in steatotic hepatocytes”. Biochimica et Biophysica Acta (BBA) – Molecular Cell Research. 1863 (9): 2135–2146. doi:10.1016/j.bbamcr.2016.05.006. PMID 27178543.
- Tushuizen ME, Bunck MC, Pouwels PJ, van Waesberghe JH, Diamant M, Heine RJ (October 2006). “Incretin mimetics as a novel therapeutic option for hepatic steatosis”. Liver International. 26 (8): 1015–1017. doi:10.1111/j.1478-3231.2006.01315.x. PMID 16953843. S2CID 32332119.
- European medicines Agency. European Public Assessment Report Byetta. 2006. EMEA/H/C/698. [Google Scholar]
- Amori RE, Lau J, Pittas AG. Efficacy and safety of incretin therapy in type 2 diabetes: systematic review and meta-analysis. JAMA. 2007;298:194–206. [PubMed] [Google Scholar]
- Heine RJ, Van Gaal LF, Johns D, Mihm MJ, Widel MH, Brodows RG. Exenatide versus insulin glargine in patients with suboptimally controlled type 2 diabetes: a randomized trial. Ann Intern Med. 2005;143:559–569. [PubMed] [Google Scholar]
- 65. US Food and Drug Administration. Information for Healthcare Professionals Exenatide (marketed as Byetta) 2009. [press release] http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm124713.htm.
- European medicines Agency. European Public Assessment Report Victoza. 2009. EMEA/H/C/1026. [Google Scholar]
- “FDA investigating reports of possible increased risk of pancreatitis and pre-cancerous findings of the pancreas from incretin mimetic drugs for type 2 diabetes”. FDA. U.S. Food and Drug Administration. 3 March 2013. Retrieved 14 March 2013.
- “European Medicines Agency investigates findings on pancreatic risks with GLP-1-based therapies for type-2 diabetes”. EMA. European Medicines Agency Sciences Medicines Health. 26 March 2013. Archived from the original on 28 August 2021. Retrieved 26 March 2013.
- Moylan T (11 November 2015). “Preemption Summary Judgment Granted In Incretin-Mimetic Multidistrict Litigation”. Lexisnexis.
- Ali ES, Hua J, Wilson CH, Tallis GA, Zhou FH, Rychkov GY, et al. (September 2016). “The glucagon-like peptide-1 analogue exendin-4 reverses impaired intracellular Ca(2+) signalling in steatotic hepatocytes”. Biochimica et Biophysica Acta (BBA) – Molecular Cell Research. 1863 (9): 2135–2146.
- Kim DS, Choi HI, Wang Y, Luo Y, Hoffer BJ, Greig NH (September 2017). “A New Treatment Strategy for Parkinson’s Disease through the Gut-Brain Axis: The Glucagon-Like Peptide-1 Receptor Pathway”. Cell Transplantation. 26 (9): 1560–1571. doi:10.1177/0963689717721234. PMC 5680957. PMID 29113464.
- Bailey S (30 November 2021). “The Bydureon (exenatide) phase 3 trial”. Cure Parkinson’s. Retrieved 11 September 2022.
- Cvetkovic RS, Plosker GL. Exenatide: a review of its use in patients with type 2 diabetes mellitus (as an adjunct to metformin and/or a sulfonylurea) Drugs. 2007;67:935–954. [PubMed] [Google Scholar]
- Knudsen LB, Nielsen PF, Huusfeldt PO, et al. Potent derivatives of glucagon-like peptide-1 with pharmacokinetic properties suitable for once daily administration. J Med Chem. 2000;43:1664–1669. [PubMed] [Google Scholar]
- Elbrond B, Jakobsen G, Larsen S, et al. Pharmacokinetics, pharmacodynamics, safety, and tolerability of a single-dose of NN2211, a long-acting glucagon-like peptide 1 derivative, in healthy male subjects. Diabetes Care. 2002;25:1398–1404. [PubMed] [Google Scholar]
- Damholt B, Golor G, Wierich W, Pedersen P, Ekblom M, Zdravkovic M. An open-label, parallel group study investigating the effects of age and gender on the pharmacokinetics of the once-daily glucagon-like peptide-1 analogue liraglutide. J Clin Pharmacol. 2006;46:635–641. [PubMed] [Google Scholar]
- “Liraglutide Monograph for Professionals”. Drugs.com. American Society of Health-System Pharmacists. Archived from the original on 23 March 2019. Retrieved 23 March 2019.
- “FDA approves weight management drug”. U.S. Food and Drug Administration (FDA). 4 December 2020. Archived from the original on 14 June 2021. Retrieved 5 June 2021.
- Shyangdan D, Cummins E, Royle P, Waugh N (May 2011). “Liraglutide for the treatment of type 2 diabetes”. Health Technology Assessment. 15 (Suppl 1): 77–86. doi:10.3310/hta15Suppl1-09. PMID 21609656. Archived from the original on 14 March 2023. Retrieved 14 May 2023.
- British National formulary: BNF 76 (76 ed.). Pharmaceutical Press. 2018. p. 685. ISBN 9780857113382.
- “Victoza EPAR”. European Medicines Agency. 17 September 2018. Archived from the original on 23 March 2019. Retrieved 23 March 2019.
- “Liraglutide injection”. DailyMed. U.S. National Library of Medicine. Archived from the original on 27 March 2021. Retrieved 23 March 2019.
- “The Top 300 of 2022”. ClinCalc. Archived from the original on 30 August 2024. Retrieved 30 August 2024.
- “Liraglutide Drug Usage Statistics, United States, 2013 – 2022”. ClinCalc. Retrieved 30 August 2024.
- Goldstein BJ, Mueller-Wieland D (14 November 2007). Type 2 Diabetes: Principles and Practice (2nd ed.). CRC Press. ISBN 978-0-8493-7958-1. Archived from the original on 18 January 2015. Retrieved 17 January 2015.
- Beglinger C, Degen L (November 2006). “Gastrointestinal satiety signals in humans–physiologic roles for GLP-1 and PYY?”. Physiology & Behavior. 89 (4): 460–464. doi:10.1016/j.physbeh.2006.05.048. PMID 16828127. S2CID 32598231.
- “Victoza (liraglutide)”. Drugs.com. May 2008. Archived from the original on 15 December 2017. Retrieved 23 January 2018.
- Marso SP, Daniels GH, Brown-Frandsen K, Kristensen P, Mann JF, Nauck MA, et al. (July 2016). “Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes”. The New England Journal of Medicine. 375 (4): 311–322. doi:10.1056/nejmoa1603827. PMC 4985288. PMID 27295427.
- American Diabetes Association (January 2022). “Introduction: Standards of Medical Care in Diabetes-2022”. Diabetes Care. 45 (Suppl 1): S1–S2. doi:10.2337/dc22-Sint. PMID 34964812. S2CID 245454068.
- Nathan DM, Lachin JM, Balasubramanyam A, Burch HB, Buse JB, Butera NM, et al. (September 2022). “Glycemia Reduction in Type 2 Diabetes – Glycemic Outcomes”. The New England Journal of Medicine. 387 (12): 1063–1074. doi:10.1056/NEJMoa2200433. PMC 9829320. PMID 36129996. S2CID 252437415.
- Shyangdan DS, Royle P, Clar C, Sharma P, Waugh N, Snaith A (October 2011). “Glucagon-like peptide analogues for type 2 diabetes mellitus”. The Cochrane Database of Systematic Reviews. 2011 (10): CD006423.
- Xie Z, Yang S, Deng W, Li J, Chen J (6 December 2022). “Efficacy and Safety of Liraglutide and Semaglutide on Weight Loss in People with Obesity or Overweight: A Systematic Review”. Clinical Epidemiology. 14: 1463–1476. doi:10.2147/CLEP.S391819. PMC 9738168. PMID 36510488.
- O’Neil PM, Birkenfeld AL, McGowan B, Mosenzon O, Pedersen SD, Wharton S, et al. (August 2018). “Efficacy and safety of semaglutide compared with liraglutide and placebo for weight loss in patients with obesity: a randomised, double-blind, placebo and active controlled, dose-ranging, phase 2 trial”. Lancet. 392 (10148): 637–649. doi:10.1016/S0140-6736(18)31773-2. PMID 30122305. S2CID 52041320.
- Chen E, Cooney E (10 September 2024). “Obesity drug worked in children ages 6 to 12, study says, raising hopes and concerns”. STAT. Retrieved 12 September 2024.
- Fox CK, Barrientos-Pérez M, Bomberg EM, Dcruz J, Gies I, Harder-Lauridsen NM, et al. (September 2024). “Liraglutide for Children 6 to <12 Years of Age with Obesity – A Randomized Trial”. The New England Journal of Medicine. doi:10.1056/NEJMoa2407379. PMID 39258838.
- “News details”. Novo Nordisk. Retrieved 12 September 2024.
- Garber A, Henry R, Ratner R, et al. Liraglutide versus glimepiride monotherapy for type 2 diabetes (LEAD-3 Mono): a randomised, 52-week, phase III, double-blind, parallel-treatment trial. Lancet. 2009;373:473–481. [PubMed] [Google Scholar]
- Marre M, Shaw J, Brandle M, et al. Liraglutide, a once-daily human GLP-1 analogue, added to a sulphonylurea over 26 weeks produces greater improvements in glycaemic and weight control compared with adding rosiglitazone or placebo in subjects with Type 2 diabetes (LEAD-1 SU) Diabet Med. 2009;26:268–278. [PMC free article] [PubMed] [Google Scholar]
- Buse JB, Rosenstock J, Sesti G, et al. Liraglutide once a day versus exenatide twice a day for type 2 diabetes: a 26-week randomised, parallel-group, multinational, open-label trial (LEAD-6) Lancet. 2009;374:39–47. [PubMed] [Google Scholar]
- “Victoza- liraglutide injection”. DailyMed. U.S. National Library of Medicine. Archived from the original on 27 March 2021. Retrieved 5 June 2021.
- Parks M, Rosebraugh C (March 2010). “Weighing risks and benefits of liraglutide–the FDA’s review of a new antidiabetic therapy”. The New England Journal of Medicine. 362 (9): 774–7. doi:10.1056/NEJMp1001578. PMID 20164475.
- Singh S, Chang HY, Richards TM, Weiner JP, Clark JM, Segal JB (April 2013). “Glucagonlike peptide 1-based therapies and risk of hospitalization for acute pancreatitis in type 2 diabetes mellitus: a population-based matched case-control study”. JAMA Internal Medicine. 173 (7): 534–539. doi:10.1001/jamainternmed.2013.2720. PMID 23440284. S2CID 425632.
- Egan AG, Blind E, Dunder K, de Graeff PA, Hummer BT, Bourcier T, Rosebraugh C (February 2014). “Pancreatic safety of incretin-based drugs–FDA and EMA assessment”. The New England Journal of Medicine. 370 (9): 794–797. doi:10.1056/NEJMp1314078. PMID 24571751.
- “Tanzeum”. Drugs.com.
- “Eperzan: EPAR — Product Information” (PDF). European Medicines Agency. 2017-08-04. Archived from the original (PDF) on 2017-09-02. Retrieved 2017-09-02.
- Matthew Herper for Forbes. 16 July 2012. Three Lessons From GlaxoSmithKline’s Purchase Of Human Genome Sciences
- Gallivan R, Plumridge H (26 March 2014). “Glaxo Gets EU Marketing Approval for Diabetes Drug Eperzan”. Wall Street Journal.
- Busko M (15 April 2014). “FDA Approves Weekly Injectable Diabetes Drug: Albiglutide”. Medscape.
- “Typ-2-Diabetes: Albiglutid geht weltweit vom Markt” [Type 2 diabetes: Albiglutide is being withdrawn from the market worldwide]. Pharmazeutische Zeitung Online (in German). 2017-08-02.
- Madsbad S (April 2016). “Review of head-to-head comparisons of glucagon-like peptide-1 receptor agonists”. Diabetes, Obesity & Metabolism. 18 (4): 317–332. doi:10.1111/dom.12596. PMC 5064617. PMID 26511102.
- Matthews JE, Stewart MW, De Boever EH, Dobbins RL, Hodge RJ, Walker SE, et al. (December 2008). “Pharmacodynamics, pharmacokinetics, safety, and tolerability of albiglutide, a long-acting glucagon-like peptide-1 mimetic, in patients with type 2 diabetes”. The Journal of Clinical Endocrinology and Metabolism. 93 (12): 4810–4817. doi:10.1210/jc.2008-1518. PMID 18812476.[permanent dead link]
- Baggio LL, Drucker DJ (2008). “Glucagon-like Peptide-1 Analogs Other Than Exenatide”.
- Yu M, Benjamin MM, Srinivasan S, Morin EE, Shishatskaya EI, Schwendeman SP, Schwendeman A (May 2018). “Battle of GLP-1 delivery technologies”. Advanced Drug Delivery Reviews. 130: 113–130. doi:10.1016/j.addr.2018.07.009. PMC 6843995. PMID 30009885.
- Tibble CA, Cavaiola TS, Henry RR (May 2013). “Longer acting GLP-1 receptor agonists and the potential for improved cardiovascular outcomes: a review of current literature”. Expert Review of Endocrinology & Metabolism. 8 (3): 247–259. doi:10.1586/eem.13.20. PMID 30780817. S2CID 73313508.
- “Lilly’s Once-Weekly Dulaglutide Shows Non-Inferiority to Liraglutide in Head-to-Head Phase III Trial for Type 2 Diabetes” (Press release). Eli Lilly. 25 February 2014.
- “Trulicity (dulaglutide) is the first and only type 2 diabetes medicine approved to reduce cardiovascular events in adults with and without established cardiovascular disease”. Eli Lilly and Company (Press release). 21 February 2020. Retrieved 23 February 2020.
- “FDA approves Trulicity to treat type 2 diabetes” (Press release). U.S. Food and Drug Administration (FDA). 18 September 2014. Archived from the original on 20 April 2016. Retrieved 4 February 2020.
 This article incorporates text from this source, which is in the public domain.
This article incorporates text from this source, which is in the public domain. - “Risk Evaluation and Mitigation Strategy (REMS)”. United States Food and Drug Administration. September 2014. Retrieved 24 March 2020.
- Frias JP, Bonora E, Nevarez Ruiz L, Li YG, Yu Z, Milicevic Z, et al. (March 2021). “Efficacy and Safety of Dulaglutide 3.0 mg and 4.5 mg Versus Dulaglutide 1.5 mg in Metformin-Treated Patients With Type 2 Diabetes in a Randomized Controlled Trial (AWARD-11)”. Diabetes Care. 44 (3): 765–773. doi:10.2337/dc20-1473. PMC 7896253. PMID 33397768.
- Terauchi Y, Satoi Y, Takeuchi M, Imaoka T (July 2014). “Monotherapy with the once weekly GLP-1 receptor agonist dulaglutide for 12 weeks in Japanese patients with type 2 diabetes: dose-dependent effects on glycaemic control in a randomised, double-blind, placebo-controlled study”. Endocrine Journal. 61 (10): 949–959. doi:10.1507/endocrj.ej14-0147. PMID 25029955.
- “Drug Approval Package: Trulicity (dulaglutide) NDA #125469”. U.S. Food and Drug Administration (FDA). 27 October 2014. Retrieved 4 February 2020.
- Liu J, Li L, Deng K, Xu C, Busse JW, Vandvik PO, et al. (June 2017). “Incretin based treatments and mortality in patients with type 2 diabetes: systematic review and meta-analysis”. BMJ. 357: j2499. doi:10.1136/bmj.j2499. PMC 5463186. PMID 28596247.
- Nauck M, Weinstock RS, Umpierrez GE, Guerci B, Skrivanek Z, Milicevic Z (August 2014). “Efficacy and safety of dulaglutide versus sitagliptin after 52 weeks in type 2 diabetes in a randomized controlled trial (AWARD-5)”. Diabetes Care. 37 (8): 2149–2158. doi:10.2337/dc13-2761. PMC 4113177. PMID 24742660.
- Amblee A (April 2014). “Dulaglutide for the treatment of type 2 diabetes”. Drugs of Today. 50 (4): 277–289. doi:10.1358/dot.2014.50.4.2132740. PMID 24918645.
- Monami M, Dicembrini I, Nardini C, Fiordelli I, Mannucci E (February 2014). “Glucagon-like peptide-1 receptor agonists and pancreatitis: a meta-analysis of randomized clinical trials”. Diabetes Research and Clinical Practice. 103 (2): 269–275. doi:10.1016/j.diabres.2014.01.010. PMID 24485345. S2CID 33922845.
- Christensen M, Knop FK, Holst JJ, Vilsboll T (August 2009). “Lixisenatide, a novel GLP-1 receptor agonist for the treatment of type 2 diabetes mellitus”. IDrugs. 12 (8): 503–13. PMID 19629885.
- Terry M (November 5, 2015). “In Attempt to Bolster Sagging Diabetes Revenue Sanofi Inks Deal with Hanmi Pharma Worth 4 2 Billion”. Biospace.
- “Adlyxin- lixisenatide kit Adlyxin- lixisenatide injection, solution”. DailyMed. January 11, 2019. Retrieved September 7, 2020.
- McClean PL, Hölscher C (November 2014). “Lixisenatide, a drug developed to treat type 2 diabetes, shows neuroprotective effects in a mouse model of Alzheimer’s disease”. Neuropharmacology. 86: 241–58. doi:10.1016/j.neuropharm.2014.07.015. PMID 25107586. S2CID 24550291.
- Cai HY, Yang JT, Wang ZJ, Zhang J, Yang W, Wu MN, Qi JS (January 2018). “Lixisenatide reduces amyloid plaques, neurofibrillary tangles and neuroinflammation in an APP/PS1/tau mouse model of Alzheimer’s disease”. Biochemical and Biophysical Research Communications. 495 (1): 1034–1040. doi:10.1016/j.bbrc.2017.11.114. PMID 29175324.
- Liu W, Jalewa J, Sharma M, Li G, Li L, Hölscher C (September 2015). “Neuroprotective effects of lixisenatide and liraglutide in the 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine mouse model of Parkinson’s disease” (PDF). Neuroscience. 303: 42–50. doi:10.1016/j.neuroscience.2015.06.054. PMID 26141845. S2CID 35297066.
- Hunter K, Hölscher C (March 2012). “Drugs developed to treat diabetes, liraglutide and lixisenatide, cross the blood brain barrier and enhance neurogenesis”. BMC Neuroscience. 13 (1): 33. doi:10.1186/1471-2202-13-33. PMC 3352246. PMID 22443187.
- “Lyxumia 10 micrograms solution for injection – Summary of Product Characteristics (SPC)”. UK Electronic Medicines Compendium. May 2, 2016. Archived from the original on September 23, 2016. Retrieved September 21, 2016.
- “Lyxumia EPAR”. European Medicines Agency (EMA). September 17, 2018. Retrieved September 7, 2020.
- Liu J, Li L, Deng K, Xu C, Busse JW, Vandvik PO, et al. (June 2017). “Incretin based treatments and mortality in patients with type 2 diabetes: systematic review and meta-analysis”. BMJ. 357: j2499. doi:10.1136/bmj.j2499. PMC 5463186. PMID 28596247.
- Lau J, Bloch P, Schäffer L, Pettersson I, Spetzler J, Kofoed J, et al. (September 2015). “Discovery of the Once-Weekly Glucagon-Like Peptide-1 (GLP-1) Analogue Semaglutide”. Journal of Medicinal Chemistry. 58 (18): 7370–80. doi:10.1021/acs.jmedchem.5b00726. PMID 26308095. S2CID 20228358.
- Gotfredsen CF, Mølck AM, Thorup I, Nyborg NC, Salanti Z, Knudsen LB, et al. (July 2014). “The human GLP-1 analogs liraglutide and semaglutide: absence of histopathological effects on the pancreas in nonhuman primates”. Diabetes. 63 (7): 2486–97. doi:10.2337/db13-1087. PMID 24608440. S2CID 35102048.
- “Ozempic- semaglutide injection, solution”. DailyMed. Archived from the original on 5 June 2021. Retrieved 5 June 2021.
- “Rybelsus- oral semaglutide tablet”. DailyMed. Archived from the original on 5 June 2021. Retrieved 5 June 2021.
- “Wegovy- semaglutide injection, solution”. DailyMed. 4 June 2021. Archived from the original on 14 December 2021. Retrieved 11 March 2022.
- Goldenberg RM, Steen O (March 2019). “Semaglutide: Review and Place in Therapy for Adults With Type 2 Diabetes”. Canadian Journal of Diabetes. 43 (2): 136–145.
- Li Y, Hansotia T, Yusta B, Ris F, Halban P, Drucker D (2003). “Glucagon-like Peptide-1 Receptor Signaling Modulates β Cell Apoptosis”. The Journal of Biological Chemistry. 278 (1): 471–478. doi:10.1074/jbc.M209423200. PMID 12409292.
- Doggrell SA (March 2018). “Semaglutide in type 2 diabetes – is it the best glucagon-like peptide 1 receptor agonist (GLP-1R agonist)?” (PDF). Expert Opinion on Drug Metabolism & Toxicology. 14 (3): 371–377. doi:10.1080/17425255.2018.1441286. PMID 29439603. S2CID 3421553. Archived (PDF) from the original on 5 May 2020. Retrieved 12 December 2019.
- Dhillon S (February 2018). “Semaglutide: First Global Approval”. Drugs. 78 (2): 275–284. doi:10.1007/s40265-018-0871-0. PMID 29363040. S2CID 46851453.
- Blundell J, Finlayson G, Axelsen M, Flint A, Gibbons C, Kvist T, et al. (September 2017). “Effects of once-weekly semaglutide on appetite, energy intake, control of eating, food preference and body weight in subjects with obesity”. Diabetes, Obesity & Metabolism. 19 (9): 1242–1251. doi:10.1111/dom.12932. PMC 5573908. PMID 28266779.
- Clinical trial number NCT00696657 for “A Randomised Controlled Clinical Trial in Type 2 Diabetes Comparing Semaglutide to Placebo and Liraglutide” at ClinicalTrials.gov
- Kalra S, Gupta Y (July 2015). “Once-weekly glucagon-like peptide 1 receptor agonists”. The Journal of the Pakistan Medical Association. 65 (7): 796–8. PMID 26160096. Archived from the original on 30 September 2022. Retrieved 10 April 2022.
- Singh G, Krauthamer M, Bjalme-Evans M (January 2022). “Wegovy (semaglutide): a new weight loss drug for chronic weight management”. Journal of Investigative Medicine. 70 (1): 5–13. doi:10.1136/jim-2021-001952. PMC 8717485. PMID 34706925.
- “Efficacy and Safety of Semaglutide Versus Dulaglutide as add-on to Metformin in Subjects With Type 2 Diabetes”. ClinicalTrials.gov. October 2019. Archived from the original on 31 July 2018. Retrieved 3 March 2023.
- “Wegovy- semaglutide injection, solution”. DailyMed. 4 June 2021. Archived from the original on 14 December 2021. Retrieved 11 March 2022.
- “FDA approves first oral GLP-1 treatment for type 2 diabetes” (Press release). U.S. Food and Drug Administration (FDA). 20 September 2019. Archived from the original on 23 September 2019. Retrieved 20 September 2019.
- “Wegovy : Pending EC decision”. European Medicines Agency. 11 November 2021. Archived from the original on 13 November 2021. Retrieved 13 November 2021. Text was copied from this source which is copyright European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- “Wegovy Product information”. Union Register of medicinal products. Archived from the original on 30 October 2022. Retrieved 3 March 2023.
- Wilding JP, Batterham RL, Calanna S, Davies M, Van Gaal LF, Lingvay I, et al. (March 2021). “Once-Weekly Semaglutide in Adults with Overweight or Obesity”. The New England Journal of Medicine. 384 (11): 989–1002. doi:10.1056/NEJMoa2032183. PMID 33567185. S2CID 231883214.
- Blum D (22 November 2022). “What Is Ozempic and Why Is It Getting So Much Attention?”. The New York Times. ISSN 0362-4331. Archived from the original on 29 March 2023. Retrieved 30 March 2023.
- Garvey WT, Batterham RL, Bhatta M, Buscemi S, Christensen LN, Frias JP, et al. (October 2022). “Two-year effects of semaglutide in adults with overweight or obesity: the STEP 5 trial”. Nature Medicine. 28 (10): 2083–2091. doi:10.1038/s41591-022-02026-4. PMC 9556320. PMID 36216945.
- Dillinger K (29 March 2023). “WHO advisers to consider whether obesity medication should be added to Essential Medicines List”. CNN. Archived from the original on 30 March 2023. Retrieved 30 March 2023.
- Müller TD, Blüher M, Tschöp MH, DiMarchi RD (March 2022). “Anti-obesity drug discovery: advances and challenges”. Nature Reviews. Drug Discovery. 21 (3): 201–223. doi:10.1038/s41573-021-00337-8. PMC 8609996. PMID 34815532.
- “Novo Nordisk says stopping obesity drug may cause full weight regain in 5 years”. Reuters. 30 March 2023. Archived from the original on 10 June 2023. Retrieved 12 February 2024.
- “FDA Approves First Treatment to Reduce Risk of Serious Heart Problems Specifically in Adults with Obesity or Overweight”. U.S. Food and Drug Administration (FDA) (Press release). 8 March 2024. Archived from the original on 12 March 2024. Retrieved 12 March 2024.
 This article incorporates text from this source, which is in the public domain.
This article incorporates text from this source, which is in the public domain. - “Medications Containing Semaglutide Marketed for Type 2 Diabetes or Weight Loss”. U.S. Food and Drug Administration (FDA). 21 December 2023. Archived from the original on 29 December 2023. Retrieved 29 December 2023.
- Nagendra L, Bg H, Sharma M, Dutta D (July 2023). “Semaglutide and cancer: A systematic review and meta-analysis.”. Diabetes Metab Syndr. 17 (9): 102834. doi:10.1016/j.dsx.2023.102834. PMID 37531876. S2CID 260261877.
- Blanchet B (27 July 2023). “Ozempic, Drugs for Weight Loss Being Reviewed for Links to Suicide Risk”. People. Archived from the original on 28 July 2023. Retrieved 28 July 2023.
- “Weight-loss jabs investigated for suicide risk”. BBC News. 10 July 2023. Archived from the original on 10 July 2023. Retrieved 10 July 2023.
- “FDA reports no link between weight-loss drugs and suicidal thoughts”. The Washington Post. Archived from the original on 14 January 2024. Retrieved 19 January 2024.
- “Update on FDA’s ongoing evaluation of reports of suicidal thoughts or actions in patients taking a certain type of medicines approved for type 2 diabetes and obesity”. U.S. Food and Drug Administration (FDA). 11 January 2024. Archived from the original on 19 January 2024. Retrieved 19 January 2024.
- Blum D (24 February 2023). “Some People on Ozempic Lose the Desire to Drink. Scientists Are Asking Why”. The New York Times. Archived from the original on 20 July 2024. Retrieved 20 July 2024.
- Hayashi D, Edwards C, Emond JA, Gilbert-Diamond D, Butt M, Rigby A, et al. (November 2023). Trakada G (ed.). “What Is Food Noise? A Conceptual Model of Food Cue Reactivity”. Nutrients. 15 (22): 4809. doi:10.3390/nu15224809. PMC 10674813. PMID 38004203.
- Järvinen A, Laine MK, Tikkanen R, Castrén ML (2019). “Beneficial Effects of GLP-1 Agonist in a Male With Compulsive Food-Related Behavior Associated With Autism”. Frontiers in Psychiatry. 10: 97. doi:10.3389/fpsyt.2019.00097. PMC 6405420. PMID 30881319.
- Kuhn C (25 September 2023). “Patients say drugs like Ozempic help with ‘food noise.’ Here’s what that means”. PBS. Archived from the original on 13 January 2024. Retrieved 13 January 2024.
- “Ozempic- semaglutide injection, solution”. DailyMed. Archived from the original on 5 June 2021. Retrieved 5 June 2021.
- “Rybelsus- oral semaglutide tablet”. DailyMed. Archived from the original on 5 June 2021. Retrieved 5 June 2021.
- “FDA Approves New Drug Treatment for Chronic Weight Management, First Since 2014”. U.S. Food and Drug Administration (FDA) (Press release). 4 June 2021. Archived from the original on 4 June 2021. Retrieved 5 June 2021.
- ^ Jump up to:a b c d e “FDA Approves First Treatment to Reduce Risk of Serious Heart Problems Specifically in Adults with Obesity or Overweight”. U.S. Food and Drug Administration (FDA) (Press release). 8 March 2024. Archived from the original on 12 March 2024. Retrieved 12 March 2024.
 This article incorporates text from this source, which is in the public domain.
This article incorporates text from this source, which is in the public domain. - ^ Sodhi M, Rezaeianzadeh R, Kezouh A, Etminan M (November 2023). “Risk of Gastrointestinal Adverse Events Associated With Glucagon-Like Peptide-1 Receptor Agonists for Weight Loss”. Jama. 330 (18): 1795–1797. doi:10.1001/jama.2023.19574. PMC 10557026. PMID 37796527.
- ^ Goodman B (20 May 2024). “People using popular drugs for weight loss, diabetes are more likely to be diagnosed with stomach paralysis, studies confirm”. CNN. Retrieved 29 September 2024.
- ^ Abd El Aziz M, Cahyadi O, Meier JJ, Schmidt WE, Nauck MA (April 2020). “Incretin-based glucose-lowering medications and the risk of acute pancreatitis and malignancies: a meta-analysis based on cardiovascular outcomes trials”. Diabetes, Obesity & Metabolism. 22 (4): 699–704. doi:10.1111/dom.13924. PMID 31750601.
- ^ “Ozempic Bowel Obstruction | Causes & Side Effects”. Motley Rice. Retrieved 29 September 2024.
- “Ozempic Drug Trial Snapshot”. U.S. Food and Drug Administration (FDA). 5 December 2017. Archived from the original on 31 December 2023. Retrieved 31 December 2023.
 This article incorporates text from this source, which is in the public domain.
This article incorporates text from this source, which is in the public domain. - Sande CM, Tondi Resta I, Livolsi VA (March 2023). “The Thyroid Pathologist Meets Therapeutic Pharmacology”. Endocrine Pathology. 34 (1): 48–56. doi:10.1007/s12022-023-09749-1. PMC 9890439. PMID 36723855.
- “Mounjaro- tirzepatide injection, solution”. DailyMed. 13 May 2022. Archived from the original on 3 July 2022. Retrieved 27 May 2022.
- “FDA Approves Novel, Dual-Targeted Treatment for Type 2 Diabetes”. U.S. Food and Drug Administration (FDA) (Press release). 13 May 2022. Archived from the original on 13 May 2022. Retrieved 13 May 2022.
 This article incorporates text from this source, which is in the public domain.
This article incorporates text from this source, which is in the public domain. - Thomas MK, Nikooienejad A, Bray R, Cui X, Wilson J, Duffin K, et al. (January 2021). “Dual GIP and GLP-1 Receptor Agonist Tirzepatide Improves Beta-cell Function and Insulin Sensitivity in Type 2 Diabetes”. The Journal of Clinical Endocrinology and Metabolism. 106 (2): 388–396. doi:10.1210/clinem/dgaa863. PMC 7823251. PMID 33236115.
- Coskun T, Sloop KW, Loghin C, Alsina-Fernandez J, Urva S, Bokvist KB, et al. (December 2018). “LY3298176, a novel dual GIP and GLP-1 receptor agonist for the treatment of type 2 diabetes mellitus: From discovery to clinical proof of concept”. Molecular Metabolism. 18: 3–14. doi:10.1016/j.molmet.2018.09.009. PMC 6308032. PMID 30473097.
- “Zepbound- tirzepatide injection, solution”. DailyMed. 9 November 2023. Archived from the original on 20 November 2023. Retrieved 20 November 2023.
- “FDA Approves New Medication for Chronic Weight Management”. U.S. Food and Drug Administration (FDA) (Press release). 8 November 2023. Archived from the original on 8 November 2023. Retrieved 9 November 2023.
 This article incorporates text from this source, which is in the public domain.
This article incorporates text from this source, which is in the public domain. - US patent 9474780, Bokvist BK, Coskun T, Cummins RC, Alsina-Fernandez J, “GIP and GLP-1 co-agonist compounds”, issued 2016-10-25, assigned to Eli Lilly and Co
- Frederick MO, Boyse RA, Braden TM, Calvin JR, Campbell BM, Changi SM, et al. (2021). “Kilogram-Scale GMP Manufacture of Tirzepatide Using a Hybrid SPPS/LPPS Approach with Continuous Manufacturing”. Organic Process Research & Development. 25 (7): 1628–1636. doi:10.1021/acs.oprd.1c00108. S2CID 237690232.
- Ahangarpour M, Kavianinia I, Harris PW, Brimble MA (January 2021). “Photo-induced radical thiol-ene chemistry: a versatile toolbox for peptide-based drug design”. Chemical Society Reviews. 50 (2). Royal Society of Chemistry: 898–944. doi:10.1039/d0cs00354a. PMID 33404559. S2CID 230783854.
- Østergaard S, Paulsson JF, Kofoed J, Zosel F, Olsen J, Jeppesen CB, et al. (October 2021). “The effect of fatty diacid acylation of human PYY3-36 on Y2 receptor potency and half-life in minipigs”. Scientific Reports. 11 (1): 21179. Bibcode:2021NatSR..1121179O. doi:10.1038/s41598-021-00654-3. PMC 8551270. PMID 34707178.
- “Tirzepatide significantly reduced A1C and body weight in people with type 2 diabetes in two phase 3 trials from Lilly’s SURPASS program” (Press release). Eli Lilly and Company. 17 February 2021. Archived from the original on 28 October 2021. Retrieved 28 October 2021 – via PR Newswire.
- “Lilly : Phase 3 Tirzepatide Results Show Superior A1C And Body Weight Reductions In Type 2 Diabetes”. Business Insider. RTTNews. 19 October 2021. Archived from the original on 28 October 2021. Retrieved 28 October 2021.
- Thomas MK, Nikooienejad A, Bray R, Cui X, Wilson J, Duffin K, et al. (January 2021). “Dual GIP and GLP-1 Receptor Agonist Tirzepatide Improves Beta-cell Function and Insulin Sensitivity in Type 2 Diabetes”. The Journal of Clinical Endocrinology and Metabolism. 106 (2): 388–396. doi:10.1210/clinem/dgaa863. PMC 7823251. PMID 33236115.
- Willard FS, Douros JD, Gabe MB, Showalter AD, Wainscott DB, Suter TM, et al. (September 2020). “Tirzepatide is an imbalanced and biased dual GIP and GLP-1 receptor agonist”. JCI Insight. 5 (17). doi:10.1172/jci.insight.140532. PMC 7526454. PMID 32730231.
- Frías JP, Davies MJ, Rosenstock J, Pérez Manghi FC, Fernández Landó L, Bergman BK, et al. (August 2021). “Tirzepatide versus Semaglutide Once Weekly in Patients with Type 2 Diabetes”. The New England Journal of Medicine. 385 (6): 503–515. doi:10.1056/NEJMoa2107519. PMID 34170647. S2CID 235635529.
- Dutta D, Surana V, Singla R, Aggarwal S, Sharma M (November–December 2021). “Efficacy and safety of novel twincretin tirzepatide a dual GIP and GLP-1 receptor agonist in the management of type-2 diabetes: A Cochrane meta-analysis”. Indian Journal of Endocrinology and Metabolism. 25 (6): 475–489. doi:10.4103/ijem.ijem_423_21. PMC 8959203. PMID 35355921.
- Jastreboff AM, Aronne LJ, Ahmad NN, Wharton S, Connery L, Alves B, et al. (4 June 2022). “Tirzepatide Once Weekly for the Treatment of Obesity”. NEJM. 387 (3): 205–216. doi:10.1056/NEJMoa2206038. PMID 35658024. S2CID 249385412.
- ^ Dee JE (6 June 2022). “More Than 20% Weight Reduction in Individuals With Obesity”. Yale Department of Internal Medicine. Archived from the original on 10 June 2022. Retrieved 12 June 2022.
- ^ Davis N (5 June 2022). “Diabetes drug leads to notable weight loss in people with obesity – study”. The Guardian. Archived from the original on 11 June 2022. Retrieved 12 June 2022.
- “Mounjaro EPAR”. European Medicines Agency (EMA). 18 July 2022. Archived from the original on 12 December 2022. Retrieved 2 January 2023.
Text was copied from this source which is copyright European Medicines Agency. Reproduction is authorized provided the source is acknowledged. - “Mounjaro Product information”. Union Register of medicinal products. Archived from the original on 8 February 2023. Retrieved 3 March 2023.
- Min T, Bain SC (January 2021). “The Role of Tirzepatide, Dual GIP and GLP-1 Receptor Agonist, in the Management of Type 2 Diabetes: The SURPASS Clinical Trials”. Diabetes Therapy. 12 (1): 143–157. doi:10.1007/s13300-020-00981-0. PMC 7843845. PMID 33325008.
- Frias JP, Nauck MA, Van J, Kutner ME, Cui X, Benson C, et al. (November 2018). “Efficacy and safety of LY3298176, a novel dual GIP and GLP-1 receptor agonist, in patients with type 2 diabetes: a randomised, placebo-controlled and active comparator-controlled phase 2 trial”. The Lancet. 392 (10160): 2180–2193. doi:10.1016/S0140-6736(18)32260-8. PMID 30293770.
- Frias JP, Nauck MA, Van J, Benson C, Bray R, Cui X, et al. (June 2020). “Efficacy and tolerability of tirzepatide, a dual glucose-dependent insulinotropic peptide and glucagon-like peptide-1 receptor agonist in patients with type 2 diabetes: A 12-week, randomized, double-blind, placebo-controlled study to evaluate different dose-escalation regimens”. Diabetes, Obesity & Metabolism. 22 (6): 938–946. doi:10.1111/dom.13979. PMC 7318331. PMID 31984598.
- Dahl D, Onishi Y, Norwood P, Huh R, Bray R, Patel H, et al. (February 2022). “Effect of Subcutaneous Tirzepatide vs Placebo Added to Titrated Insulin Glargine on Glycemic Control in Patients With Type 2 Diabetes: The SURPASS-5 Randomized Clinical Trial”. JAMA. 327 (6): 534–545. doi:10.1001/jama.2022.0078. PMC 8826179. PMID 35133415.
- Han, Sabrina H; Safeek, Rachel; Ockerman, Kyle; et al. (2023). “Public Interest in the Off-Label Use of Glucagon-like Peptide 1 Agonists (Ozempic) for Cosmetic Weight Loss: A Google Trends Analysis”. Aesthetic Surgery Journal. doi:10.1093/asj/sjad211. PMID 37402640.
- Messer, Sarah; Kindelan, Katie (May 18, 2023). “Woman says she got less expensive drug for weight loss after being denied by insurance”. abcnews.go.com. ABC News. Retrieved 31 July 2024.
- Lovelace, Berkeley Jr. (May 3, 2023). “Safety worries over copycat versions of Ozempic and Wegovy prompt state crackdowns”. nbcnews.com. NBC News. Retrieved 26 September 2023.
- Jones, C. T. (8 June 2023). “The FDA Warned Ozempic Users. They Don’t Give a F-ck”. Rolling Stone. Retrieved 26 September 2023.
- Gilbert, Daniel (19 September 2023). “Inside the gold rush to sell cheaper imitations of Ozempic”. Washington Post. Retrieved 31 July 2024.
- Lovelace, Berkeley Jr.; Lewis, Reynolds; Kopf, Marina (19 March 2023). “The high price of Ozempic is pushing many to unregulated, copycat drugs for weight loss”. nbcnews.com. NBC News. Retrieved 31 July 2024.
- Chiappini, Stefania; Papanti Pelletier, G. Duccio; Vickers-Smith, Rachel; et al. (19 October 2023). “Exploring the nexus of binge eating disorder (BED), New Psychoactive Substances (NPS), and misuse of pharmaceuticals: charting a path forward”. Expert Opinion on Pharmacotherapy: 1–4. doi:10.1080/14656566.2023.2271389. PMID 37853742. S2CID 264303916.
