Introduzione:

Nel comune pensare dell’uomo (e dell’atleta) medio, il Dihydrotestosterone (DHT) è, al pari degli Estrogeni, visto come un ormone tendenzialmente negativo, da ridurre il più possibile. Ovviamente questa visione è a dir poco ristretta dal momento che valuta l’attività del suddetto metabolita del Testosterone solamente in quelle circostanze dove un suo consistente livello può causare, specie nei soggetti predisposti o in determinate circostanze multifattoriali, acne, perdita accelerata dei capelli e ipertrofia prostatica (ovviamente parliamo di soggetti di sesso maschile). Inoltre, il DHT è considerato un metabolita pressoché insignificante nel miglioramento delle prestazioni, soprattutto per quanto concerne l’ipertrofia muscolare. Ma è veramente così limitato il suo impatto per un atleta? ..
Per rispondere a questo quesito nel presente articolo, in modo simile a quanto già feci nell’articolo dedicato agli Estrogeni, esporrò una panoramica dettagliata di tutto ciò che concerne il Dihydrotestosterone e le sue caratteristiche anche alla luce di recenti ed interessanti studi.
Cos’è il DHT?

Il Dihydrotestosterone (DHT, 5α-dihydrotestosterone, 5α-DHT, Androstanolone o Stanolone) è uno steroide con caratteristiche fortemente androgene, principalmente ottenuto dalla 5α-riduzione del Testosterone. Infatti, l’enzima 5α-reduttasi catalizza la formazione di DHT dal Testosterone in alcuni tessuti tra cui la ghiandola prostatica, le vescicole seminali, le epididimidi, la pelle, i follicoli piliferi, il fegato e il cervello. Questo enzima media la riduzione del doppio legame C4-5 del Testosterone. Rispetto al Testosterone, il DHT è considerevolmente più potente come agonista del recettore degli androgeni (AR), seppure limitato da percorsi enzimatici.
Oltre al suo ruolo di ormone naturale, il DHT è stato usato come farmaco, ad esempio nel trattamento di bassi livelli di Androgeni negli uomini (vedi Androstanolone).
Il DHT nella Storia

Il DHT fu sintetizzato per la prima volta da Adolf Butenandt e dai suoi colleghi nel 1935. [1][2] Venne ottenuto mediante idrogenazione del Testosterone [3], che era stato scoperto all’inizio di quell’anno.[4] Il DHT è stato introdotto per uso medico come AAS nel 1953 ed è stato inizialmente notato per essere più potente del Testosterone ma con maggiore androgenicità.[5][6][7] Ma il suo potenziale androgeno non fu chiaro fino al 1956, quando venne dimostrato che veniva sintetizzato dal Testosterone negli omogenati di fegato di ratto.[2][8] Inoltre, l’importanza biologica del DHT non è stata realizzata fino agli inizi degli anni ’60, quando si è scoperto che era prodotto dalla 5α-riduzione del Testosterone circolante nei tessuti bersaglio come la ghiandola prostatica e le vescicole seminali risultando più potente del Testosterone in test biologici.[9][10][11][12] Le funzioni biologiche del DHT nell’uomo sono state definite in modo molto più chiaro alla scoperta e alla caratterizzazione del deficit di 5α-reduttasi di tipo II nel 1974.[13] Il DHT è stato l’ultimo importante ormone sessuale, gli altri sono Testosterone, Estradiolo e Progesterone, ad essere scoperto, ed è unico in quanto risulta essere il solo ormone sessuale principale che agisce fondamentalmente come ormone intracrino e paracrino piuttosto che come ormone endocrino.[12]
Biosintesi e distribuzione
Il DHT, noto anche come 5α-androstan-17β-ol-3-one, è uno steroide androstano presente in natura con un gruppo chetonico nella posizione C3 e un gruppo idrossile nella posizione C17β. È il derivato del Testosterone in cui il doppio legame tra le posizioni C4 e C5 è stato ridotto o idrogenato.
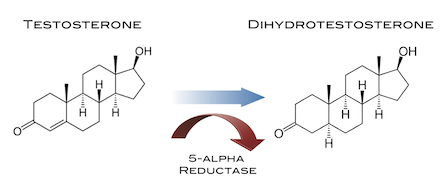
Il DHT è sintetizzato irreversibilmente dal Testosterone dall’enzima 5α-reduttasi. [14] [15] Ciò si verifica in vari tessuti tra cui i genitali (pene, scroto, clitoride, grandi labbra), [16] prostata, pelle, follicoli piliferi, fegato e cervello. [14] Circa il 5-7% del Testosterone subisce una 5α-riduzione in DHT [17] [18], e circa 200-300μg di DHT vengono sintetizzati giornalmente nel corpo. La maggior parte del DHT è prodotta nei tessuti periferici come la pelle e il fegato, mentre la maggior parte del DHT circolante proviene specificamente dal fegato. I testicoli e la ghiandola prostatica contribuiscono relativamente poco alle concentrazioni di DHT nel circolo ematico.[14]

Esistono due isoforme principali di 5α-reduttasi, la SRD5A1 (tipo I) e la SRD5A2 (tipo II), quest’ultimo isoenzima ha una maggiore importanza biologica.[14] Esiste anche una terza forma di 5α-reduttasi: SRD5A3. [19] L’SRD5A2 è maggiormente espressa nei genitali, nella ghiandola prostatica, nelle epididimidi, nelle vescicole seminali, nella pelle genitale, nei follicoli piliferi del viso, del torace [20][21] e nel fegato, mentre si osserva un’espressione più bassa in alcune aree del cervello, pelle non genitale / follicoli piliferi, testicoli e reni. L’SRD5A1 è maggiormente espressa nei follicoli non genitali della pelle / dei capelli, nel fegato e in alcune aree del cervello, mentre sono presenti livelli più bassi nella prostata, nelle epididimidi, nelle vescicole seminali, nella pelle genitale, nei testicoli, nelle ghiandole surrenali e nei reni.[14] Nella pelle, la 5α-reduttasi è espressa in ghiandole sebacee, ghiandole sudoripare, cellule epidermiche e follicoli piliferi.[20][21] Entrambi gli isoenzimi sono espressi nei follicoli piliferi del cuoio capelluto [22], sebbene l’SRD5A2 predomina in queste cellule.[21] Il sottotipo SRD5A2 è l’isoforma quasi esclusivamente espressa nella ghiandola prostatica.[23][24]

Il legame del DHT con le proteine plasmatiche è superiore al 99%. Negli uomini, circa lo 0,88% del DHT non è legato e quindi libero, mentre nelle donne in premenopausa, circa lo 0,47-0,48% non è legato. Negli uomini, il DHT è legato per il 49,7% alla globulina legante gli ormoni sessuali (SHBG), il 39,2% per l’albumina e lo 0,22% per la globulina legante i corticosteroidi (CBG), mentre nelle donne in premenopausa il DHT è legato per il 78,1-78,4% alle SHBG, 21,0-21,3% all’albumina e lo 0,12% al CBG. Nella tarda gravidanza, solo lo 0,07% del DHT non è legato nelle donne; Il 97,8% è legato alle SHBG mentre il 2,15% è legato all’albumina e lo 0,04% è legato al CBG. [25][26] Il DHT ha un’affinità maggiore per le SHBG rispetto al Testosterone, all’Estradiolo o qualsiasi altro ormone steroideo.[27][26]
Funzioni e attività biologiche del DHT
Il DHT è biologicamente importante per la differenziazione sessuale dei genitali maschili durante l’embriogenesi, la maturazione del pene e dello scroto durante la pubertà, la crescita dei peli nel viso, nel corpo e dei peli pubici e lo sviluppo e il mantenimento della ghiandola prostatica e delle vescicole seminali. Come già accennato, è principalmente sintetizzato per via della 5α-riduzione del Testosterone in alcuni tessuti ed è il principale androgeno nei genitali, nella ghiandola prostatica, nelle vescicole seminali, nella pelle e nei follicoli piliferi. [28]

Il DHT esplica una segnalazione principalmente in maniera intracrina e paracrina nei tessuti in cui viene sintetizzato, svolgendo un ruolo secondario, sebbene non trascurabile, come ormone endocrino circolante.[29][30][31] I livelli circolanti di DHT sono 1/10 e 1/20 di quelli del Testosterone in termini di concentrazioni totali e libere, rispettivamente [32], mentre i livelli locali di DHT possono essere fino a 10 volte quelli del Testosterone nei tessuti con alta espressione del 5α-reduttasi come la prostata.[33] Inoltre, a differenza del Testosterone, il DHT viene inattivato dalla 3α-idrossisteroide deidrogenasi (3α-HSD) nell’androgeno 3α-androstanediolo molto debole in vari tessuti come quello muscolare, adiposo e epatico, tra gli altri [31][34][35], e in relazione a questo, è generalmente stato riportato che il DHT è un agente anabolico molto scarso quando somministrato esogenamente come farmaco. [36] Ma su questo ci torneremo più avanti.

Oltre alle funzioni biologiche di base, il DHT svolge anche un importante ruolo causale in una serie di condizioni dipendenti dagli androgeni, tra cui le condizioni inerenti alla crescita della peluria come l’irsutismo (eccessiva crescita dei peli sul viso / corpo) e anche la perdita di capelli (alopecia androgenetica o calvizie) e malattie della prostata come l’iperplasia prostatica benigna (IPB) e il carcinoma prostatico.[28] Gli inibitori della 5α-reduttasi, che impediscono la sintesi di DHT, sono efficaci nella prevenzione e nel trattamento di queste condizioni, sebbene siano accompagnati da pesanti effetti collaterali.[37][38][39][40] Inoltre, il DHT può svolgere una funzione nel reclutamento e nella funzione del trasportatore di aminoacidi nel muscolo scheletrico.[41] Ed anche su questo punto torneremo tra poco.

È stato scoperto che i metaboliti del DHT agiscono come neurosteroidi con la propria attività biologica indipendente dall’AR.[42] Il 3α-Androstanediol è un potente modulatore allosterico positivo del recettore GABAA, mentre il 3β-androstanediol è un potente e selettivo agonista del sottotipo ERβ del Recettore degli Estrogeni (ER).[42] Questi metaboliti possono svolgere un ruolo importante negli effetti centrali del DHT e per estensione del Testosterone, inclusi i loro effetti antidepressivi, ansiolitici, gratificanti / edonici, antistress e pro-cognitivi.[42][43] Ed è soprattutto grazie all’azione neurosteroidea dei metaboliti del DHT a conferire a questa molecola i suoi benefici sull’aumento della forza muscolare e del focus mentale, entrambe caratteristiche ricercate negli sport di potenza e propedeutiche ad un migliore stimolo ipertrofico indotto dall’allenamento contro-resistenza.
Il DHT è un potente agonista dell’AR ed è in effetti il ligando endogeno più potente conosciuto per questo recettore. Ha un’affinità (Kd) compresa tra 0,25 e 0,5 nM per la RA umana, che è circa 2-3 volte superiore a quella del Testosterone (Kd = 0,4 a 1,0 nM) [44] e 15-30 volte superiore a quella degli androgeni surrenali.[45] Inoltre, il tasso di dissociazione del DHT dall’AR è 5 volte più lento di quello del Testosterone.[46 L’EC50 del DHT per l’attivazione dell’AR è 0,13 nM, che è circa 5 volte più forte di quello del Testosterone (EC50 = 0,66 nM).[47] Nei biotest, il DHT è risultato essere da 2,5 a 10 volte più potente del Testosterone.[44]
L’emivita di eliminazione del DHT nel corpo (53 minuti) è più lunga di quella del Testosterone (34 minuti), e ciò potrebbe spiegare alcune delle differenze nella loro potenza.[48] Uno studio sul trattamento transdermico con DHT e Testosterone ha riportato emivite terminali rispettivamente di 2,83 ore e 1,29 ore.[49]
A differenza di altri androgeni come il Testosterone, il DHT non può essere convertito dall’enzima aromatasi in estrogeno come l’Estradiolo. Pertanto, viene spesso utilizzato in contesti di ricerca per distinguere tra gli effetti del testosterone causati dal legame con l’AR e quelli causati dalla conversione del Testosterone in Estradiolo e il successivo legame e attivazione del ER.[50] Sebbene il DHT non possa essere aromatizzato, viene comunque trasformato in metaboliti con significativa affinità e attività ER. Questi sono 3α-androstanediolo e 3β-androstanediolo, che sono agonisti predominanti dell’ERβ.[51] Determinano l’effetto anti-estrogenico attribuito al DHT.
I livelli sierici di DHT sono circa il 10% di quelli del Testosterone, ma i livelli nella ghiandola prostatica sono da 5 a 10 volte superiori a quelli del Testosterone a causa di una conversione di oltre il 90% di quest’ultimo in DHT da parte della 5α-reduttasi espressa localmente.[33] Per questo motivo, e oltre al fatto che il DHT è molto più potente come agonista dell’AR rispetto al Testosterone [44], il DHT è considerato il principale androgeno della ghiandola prostatica.[33]

Il DHT è inattivato nel fegato e nei tessuti extraepatici come la pelle in 3α-androstanediol dall’enzima 3α-idrossistoidea deidrogenasi, e in 3β-androstanediol dall’enzimi 3β-idrossisteroidide deidrogenasi.[34][52]Questi metaboliti vengono a loro volta convertiti, rispettivamente, in Androsterone ed Epiandrosterone, quindi coniugati (tramite glucuronidazione e/o solfatazione), rilasciati in circolazione ed escreti nelle urine.[34]
Come già detto, a differenza del Testosterone, il DHT non può essere aromatizzato in estrogeno come l’Estradiolo e, per questo motivo, non ha propensione ad esercitare effetti estrogenici.[53] Quindi, il DHT viene escreto nelle urine sotto forma di metaboliti, come i coniugati di 3α-androstanediol e Androsterone.[54][34]
Uso del DHT in medicina

Il DHT è disponibile in formulazioni farmaceutiche per uso medico come steroide anabolizzante androgeno (AAS) con finalità prettamente androgene.[55] È usato come ancillare principalmente nel trattamento dell’ipogonadismo maschile.[56] Quando usato come farmaco, il DHT viene chiamato Androstanolone (INN) o Stanolone (BAN) [55] [57] [58], e viene venduto sotto nomi commerciali differenti come Andractim. [55] [57] [58] [56] [59] La disponibilità di DHT farmaceutica è limitata; non è disponibile negli Stati Uniti o in Canada, [60] [61] ma è disponibile in alcuni paesi europei. [58] [56] Le formulazioni disponibili di DHT includono compresse orali o sublinguali, gel topici e, come esteri in olio, iniettabili come Androstanolone propionato e Androstanolone Valerato.[55] [56] [59]
L’Androstanolone è disponibile in formulazioni farmaceutiche per uso medico come androgeno.[4] È usato principalmente come forma ancillare nella terapia sostitutiva degli androgeni nel trattamento dell’ipogonadismo maschile ed è specificamente approvato per questa indicazione in alcuni paesi.[62] [13] [63] [64] [65] [66] [67] Non è più raccomandato come solo farmaco nelle terapie sostitutive degli androgeni a causa delle differenze biologiche con il Testosterone come la mancanza di effetti Estrogenici e effetti androgeni parziali.[68] L’Androstanolone topico è utile nel trattamento della ginecomastia.[69] Allo stesso modo, l’Androstanolone Enantato tramite iniezione intramuscolare è risultato efficace nel trattamento della ginecomastia puberale persistente.[70] Il farmaco è stato anche usato come gel topico per il trattamento del pene piccolo nei ragazzi pre e peripubertali con sindrome da insensibilità agli androgeni lieve o parziale.[71] [72] [73]

L’Androstanolone è risultato efficace nel trattamento del carcinoma mammario in fase avanzata nelle donne negli anni ’50, sebbene fosse utilizzato in dosi molto elevate e causasse una grave virilizzazione.[74] [75] [76] È stato usato in sospensione acquosa microcristallina mediante iniezione intramuscolare.[77] [78] [79] Poco dopo, il Drostanolone Propionato (2α-Methylandrostanolone Propionato) fu sviluppato per questo uso al fine di sostituire l’Androstanolone a causa della sua superiore farmacodinamica e fu introdotto per questa indicazione negli Stati Uniti e in Europa nei primi anni ’60.[80] [81] [82] [83]
L’Androstanolone è stato usato alla dose di 25mg per via sublinguale da due a tre volte al giorno nella terapia sostitutiva con androgeni per gli uomini.[84] Questo è anche il dosaggio di Androstanolone comunemente utilizzato nel trattamento di individui si sesso maschile.[84]
La questione DHT e ipertrofia muscolare

La sarcopenia, caratterizzata da una perdita di massa muscolare, ossea, forza e resistenza, si verifica con l’invecchiamento e disturbi medici cronici come l’infezione da virus dell’immunodeficienza umana (HIV) e la terapia a lungo termine con glucocorticoidi sistemici (Gcc). D’altra parte, la somministrazione di Testosterone negli uomini più anziani e negli uomini con infezione da HIV con perdita di peso che hanno basse concentrazioni di Testosterone (Bhasin et al. 2001), nonché gli uomini che richiedono un trattamento sistemico a lungo termine di Gcc (Truhan e Ahmed 1989) aumentano il grasso corporeo- massa magra e forza muscolare.

Il muscolo scheletrico è uno dei tessuti bersaglio per l’azione anabolica degli androgeni. Recettori degli Androgeni (AR), localizzati nelle cellule muscolari e adipose, cellule nervose e pluripotenti mesenchimali che risiedono nel tessuto muscolare, probabilmente mediano gli effetti degli androgeni aumentando la massa muscolare, la sintesi proteica, il contenuto ribosomiale, le aree mitocondriali, il numero mioonucleare, il numero di cellule satellite e la miogenesi delle cellule mesenchimali pluripotenti riducendo la degradazione delle proteine e l’adipogenesi delle cellule mesenchimali pluripotenti (Herbst & Bhasin 2004). Sul ligando che si lega all’AR intracellulare, il complesso androgeno-AR viene traslocato nel nucleo e si lega a sequenze specifiche di DNA, elementi di risposta agli androgeni, con conseguente trascrizione di geni specifici (Michel & Baulieu 1980, Simental et al. 1991). Gli androgeni hanno anche azioni rapide non genomiche nel muscolo (Estrada et al. 2000, 2003), tra cui il recettore di membrana accoppiato alla proteina G, il recettore dell’inositolo 1,4,5-trisfosfato (IP3), lo ione calcio (Ca2 +) e la cascata della fosforilazione della proteina chinasi mitogeno-attivata (MAPK) / proteina chinasi regolata da segnali extracellulari (ERK). Oltre al suo ruolo nella contrazione muscolare, si ritiene che Ca2+ intracellulare regola l’espressione genica nel muscolo scheletrico (Estrada et al. 2001, Araya et al. 2003). Pertanto, le azioni genomiche e non genomiche degli androgeni sono responsabili della trascrizione dei geni sensibili agli androgeni (ARG).
Tuttavia, i meccanismi molecolari dell’effetto anabolico degli androgeni nel muscolo scheletrico sono mal compresi. Con l’avvento dell’analisi seriale dell’espressione genica (SAGE) (Velculescu et al. 1995), sono sorte nuove possibilità per l’analisi del trascrittoma su larga scala. Usando questo metodo, si sono precedentemente studiati i meccanismi molecolari responsabili dell’atrofia muscolare causata dall’immobilizzazione nei ratti (St-Amand et al. 2001), nonché il profilo di espressione genica degli uomini allenati per la resistenza (Yoshioka et al. 2003). In un interessante studio del 2006 [85], si sono studiati gli effetti della castrazione (GDX) e del DHT sull’espressione genica globale nel muscolo scheletrico dei topi maschi usando la strategia SAGE. Le trascrizioni modulate DHT sono coinvolte nel rilascio di Ca2 +, nella segnalazione cellulare, nella proliferazione cellulare, nella sintesi di mRNA e proteine e nel metabolismo energetico. Questi risultati costituiscono un primo passo verso una comprensione precisa dei meccanismi molecolari coinvolti negli effetti fisiologici degli androgeni nel muscolo scheletrico.

Nello studio, è stato asportato il muscolo gastrocnemio destro dai topi C57BL6 di età compresa tra 12 e 14 settimane. Gli animali sono stati tenuti con luci accese da 0715 a 1915h, e hanno avuto accesso all’acqua ad libitum. Nessun trattamento è stato eseguito su 26 topi intatti. Il GDX è stato eseguito 7 giorni prima della raccolta di organi in ciascuno dei 14 topi dai gruppi GDX e DHT. I topi del gruppo GDX hanno ricevuto un i.p. della soluzione del veicolo (0,4% (p / v) Methocel A15 LV Premium / 5% etanolo; Dow Chemicals Co, Laval, Quebec, Canada) 24 ore prima della morte, mentre una dose fisiologica di DHT (0,1 mg / topo) è stato iniettato 1, 3, 6 e 24 ore prima della loro uccisione (gruppi DHT 1 h, DHT 3 h, DHT 6 he DHT 24 h). Il muscolo gastrocnemio destro è stato campionato da ciascun topo e messo insieme per l’analisi dello stesso gruppo per eliminare le variazioni inter-individuali ed estrarre quantità sufficienti di mRNA. I tessuti sono stati conservati a -80 ° C fino all’estrazione dell’RNA.

Gli ormoni anabolizzanti stimolano la crescita muscolare principalmente aumentando la sintesi proteica (Rooyackers & Nair 1997). In questo studio, la condizione GDX ha represso l’espressione del membro della famiglia delle proteine da shock termico 7 (Hspb7), mentre l’iniezione di DHT ha regolato verso l’alto cinque geni che codificano proteine ribosomiali e chaperoni (Mrpl51, Rpl34, Rps20, Cct8 e Cabc1) entro 3 ore e modulando altre tre trascrizioni (Fxr2h, Rps24 e Rps27) a 24 h. Oltre alla sintesi proteica, Rpl34 e Rps20 sono implicati nella biosintesi delle poliammine (Panagiotidis et al. 1995). La proteina Cct8 la cui espressione è fortemente dipendente dalla crescita cellulare (Yokota et al. 1999) piega le proteine appena sintetizzate, compresi i componenti cellulari necessari per la crescita cellulare (Thulasiraman et al. 1999), oltre a comportarsi come proteina associata ai microtubuli (Roobol et al. 1999). Mrpl51 è codificato dal DNA mitocondriale e Cabc1 codifica una proteina mitocondriale essenziale per la corretta conformazione e funzionamento dei complessi proteici nella catena respiratoria (Iiizumi et al. 2002). In effetti, le espressioni di 18 trascrizioni relative alla produzione di OxPhos e ATP sono state sovra-regolate dal DHT in questo studio. Questi dati suggeriscono che il DHT aumenta la sintesi proteica e la stabilizzazione in parallelo con la crescita cellulare entro 3 ore nei topi in vivo.
Le trascrizioni modulate 24h dopo il trattamento con DHT nel presente studio suggeriscono quanto segue:
- l’aumento del trasporto di mRNA tra citoplasma e nucleolo da parte delle proteine fragili correlate all’X (FMRP) (Tamanini et al. 1999);
- la soppressione della degradazione dell’mRNA da parte della proteina ribosomiale S27 (Revenkova et al. 1999);
- la diminuzione della sintesi proteica poiché la proteina ribosomiale S24 è strettamente coinvolta sia nei processi di iniziazione che di allungamento durante la sintesi proteica (Bommer et al. 1988).
Il fatto che il tasso di sintesi proteica diminuisca drasticamente durante la mitosi nelle cellule di mammifero potrebbe spiegare i dati.
La degradazione delle proteine da parte del proteasoma 26S è essenziale per la progressione del ciclo cellulare, il metabolismo delle poliammine e la presentazione della catena pesante di classe I del maggiore complesso di istocompatibilità (MHC) sulla superficie cellulare. Il DHT ha indotto Psmc3 e Psmc5 le cui proteine sono i componenti integrali della subunità normativa 19S del proteasoma 26S, che potrebbe riflettere l’induzione della proliferazione cellulare e la modulazione dell’immunità da DHT.
La regolazione trascrizionale è un punto di controllo essenziale per diverse funzioni cellulari come la proliferazione cellulare, la differenziazione, la trasformazione e l’apoptosi. Il DHT ha sovra-regolato cinque fattori trascrizionali (Ogt, Pttg1, Psmc3, Psmc5 e Smyd2) entro 3 ore dopo il trattamento e il Fxr2h a 24h. L’attivazione della cascata MAPK provoca la traslocazione della proteina citoplasmatica Pttg1 nel nucleo (Pei 2000) dove la proteina Pttg1 transattiva i geni bersaglio che promuovono la proliferazione cellulare (Pei 2001). Le proteine di Psmc3 e Psmc5 suggeriscono ruoli nella transattivazione del recettore dell’ormone tiroideo (Ishizuka et al. 2001). La condizione GDX ha anche ridotto il livello di espressione del Ttr, il cui prodotto è una proteina plasmatica omotetramericana che trasporta tiroxina e retinolo. Sebbene gli ormoni tiroidei siano essenziali durante la crescita, sia un eccesso che una carenza causano un degrado muscolare da meccanismi sconosciuti (Rooyackers & Nair 1997). La proteina Fxr2h mostra una forte attivazione della trascrizione (Hillman & Gecz 2001). La glicosilazione delle proteine nucleari e citoplasmatiche è una modifica post-traduzionale diffusa e reversibile nelle cellule eucariotiche. La glicosilazione intracellulare dei residui di serina e treonina è catalizzata dalla proteina di Ogt, che regola un numero di funzioni cellulari tra cui l’attivazione trascrizionale (geni bersaglio p53) / repressione (RNA polimerasi II) e l’attivazione traslazionale (Wells et al. 2003). La presenza nel gene Smyd2 di domini SET e MYND sarebbe in accordo con gli effetti rispettivamente sulla deacetilazione e metilazione dell’istone (Sims et al. 2002). Pertanto, i risultati suggeriscono che almeno alcune delle azioni del DHT si verificano attraverso l’attivazione o la repressione dei regolatori trascrizionali.
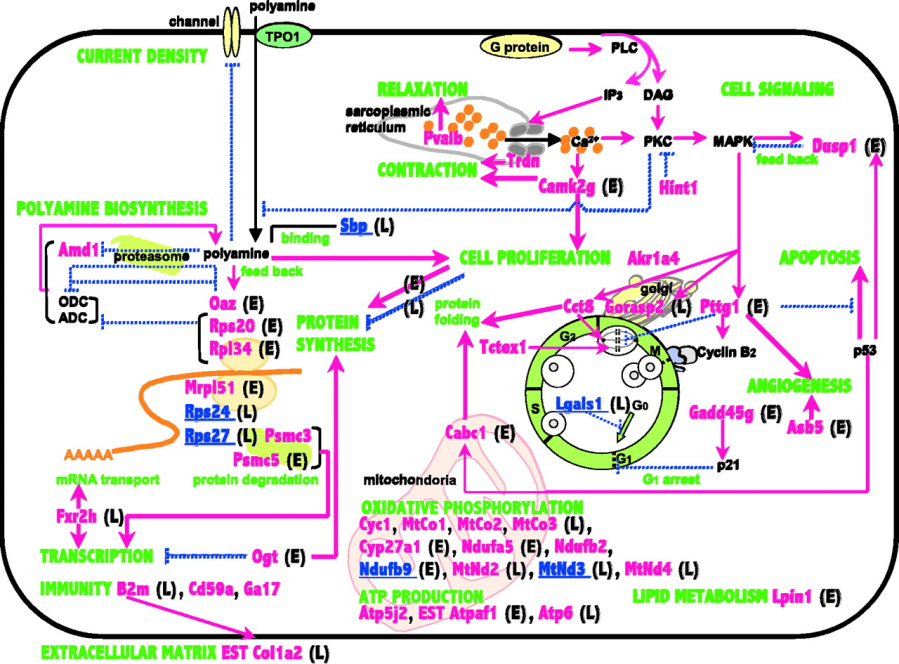
Nel muscolo scheletrico, il Ca2+ svolge un ruolo chiave nella contrazione e nel rilassamento. Il presente studio ha dimostrato che il trattamento con DHT ha aumentato l’espressione della Pvalb, una proteina di legame Ca2+ ad alta affinità che agisce come fattore di rilassamento muscolare dopo la contrazione, e Trdn che forma un complesso quaternario con il recettore della ryanodina, junctina e calsequestrina nel lume del reticolo sarcoplasmatico ( SR) per il buffering passivo di Ca2+ luminale SR, nonché un rilascio Ca2+ attivo dal processo SR durante l’accoppiamento eccitazione-contrazione. Topi transgenici che sovraesprimono Trdn1 nel cuore mostrano ipertrofia cardiaca con rilassamento alterato e contrattilità attenuata (Kirchhefer et al. 2001). Pertanto, l’induzione di entrambi i fattori di rilassamento muscolare e di contrazione potrebbe contribuire a una generazione di energia generalmente osservata negli atleti che assumono steroidi anabolizzanti.

La depolarizzazione delle cellule muscolari provoca anche un rilascio transitorio lento di Ca2 +, che è mediato dalla fosfolipasi C (PLC) e IP3 tramite i recettori IP3 (Estrada et al. 2001, Powell et al. 2001) e porta alla fosforilazione di ERK1 / 2 (Powell et al. 2001). Negli osteoblasti, il DHT attiva la proteina Gβ4 accoppiata al PLC-β2 che aumenta la formazione di IP3 e diacilglicerolo (DAG) e innesca il rilascio di Ca2 + intracellulare dal reticolo endoplasmatico (Zagar et al. 2004). Gli aumenti dei livelli di DAG e Ca2 + regolano l’attività della proteina chinasi C (PKC) che stimola ERK1 / 2 attraverso l’attivazione di MAPK chinasi 1/2 (Zagar et al. 2004). I risultati hanno mostrato le induzioni di Camk2g, Dusp1 e Hint1 entro 3 ore dall’iniezione di DHT. Ca2 + multifunzionale / proteinodinasi dipendente dalla calmodulina (CaMKII) media le risposte cellulari alla Ca2 + intracellulare ed è implicato nel controllo di funzioni essenziali quali trasmissione sinaptica, canali ionici, trascrizione genica e progressione del ciclo cellulare (Santella 1998, Anderson 2005). Le cellule proliferanti (Tombes & Krystal 1997) e il cuore ipertrofico con maggiore contrattilità (Colomer et al. 2003) esprimono l’isoforma CaMKIIγ codificata da Camk2g. Dusp1 (chiamato anche CL100 o MAPK fosfatasi 1) è stato originariamente identificato come un gene precoce immediato indotto da mitogeni (Charles et al. 1992, Keyse & Emslie 1992), e il suo livello di trascrizione riflette l’attivazione di ERK1 / 2 (Camps et al. 2000).

La Hint1, una proteina che interagisce con la PKC che originariamente si pensava inibisse quest’ultima, può svolgere un ruolo di soppressore del tumore (Su et al. 2003). Abbiamo osservato la sovra-regolazione di Mpp6, Oaz, Psmc3 e Psmc5 entro 3 ore dal trattamento con DHT. La funzione di Mpp6, un membro della sottofamiglia guanilato chinasi (MAGUK) associata alla membrana p55, non è ancora nota. Tuttavia, il MAGUK interagisce con i recettori del glutammato e vari canali ionici (Godreau et al. 2004). Le poliammine (spermine, spermidina e putrescina) interagiscono anche con alcuni canali ionici e controllano i livelli intracellulari di Ca2 + (Williams 1997). La biosintesi della poliammina nelle cellule di mammifero inizia con una produzione di putrescina da parte dell’ornitina decarbossilasi (ODC). Quando i livelli di poliammina intracellulare aumentano, l’antizima ODC, codificato da Oaz, si lega all’OCD e facilita il suo rapido degrado da parte del proteosoma 26S (Thomas & Thomas 2003). Pertanto, le induzioni di Oaz così come Psmc3 e Psmc5, che sono componenti integranti del proteasoma 26S, possono riflettere il livello aumentato di poliammine intracellulari. Inoltre, le modulazioni di queste trascrizioni e di Mpp6 entro 3 ore, lo stesso decorso di Camk2g, suggeriscono la loro partecipazione al controllo di Ca2 + intracellulare. Inoltre, il percorso Ras / MAPK controlla la trascrizione di Cct8 (Yamazaki et al. 2003) che è stata indotta a 1 ora dopo il trattamento con DHT nel presente studio. Nel loro insieme, il secondo messaggero, ovvero Ca2 + intracellulare, e le sue cascate a valle tra cui PKC e MAPK, che sono essenziali per la regolazione della crescita cellulare, sembrano essere modulati dal DHT.
Le cellule satellite / mioblasti all’interno del tessuto muscolo-scheletrico proliferano in seguito all’esposizione a fattori di crescita e a seguito di lesioni muscolari, ma smettono di dividersi quando si fondono con fibre muscolari preesistenti. La fusione è generalmente accoppiata con l’inizio della proliferazione cellulare. Nel presente studio, la trascrizioni sovra-regolate da parte del DHT e correlate all’entrata in fase S (Pttg1) (Nasmyth et al. 2000), assemblaggio di microtubuli (Cct8) (Roobol et al. 1999), formazione del fuso bipolare (Tctex1) (Vaisberg et al 1993), uguale segregazione cromosomica (Pttg1) (Nasmyth et al. 2000), accatastamento di Golgi cisternae (Gorasp2) (Shorter et al. 1999) e disintossicazione dei metaboliti reattivi prodotti durante la proliferazione cellulare (Akr1a4) (Barski et al. 2004 ), suggeriscono un’induzione della proliferazione cellulare da parte del DHT. D’altra parte, il DHT ha sotto-regola un fattore cistostatico, Lgals1, che mantiene G0 e controlla la traversata G2 (Wells & Mallucci 1991). Il fuso mitotico richiede il montaggio / smontaggio di icrotubuli e l’azione di complessi motori come il dynein (Vaisberg et al. 1993). La proteina Tctex1 è una catena leggera del complesso motorio dynein (Tai et al. 1998). Il Cct8 aumenta durante la transizione G1 / S attraverso la prima fase S (Yokota et al. 1999). Pttg1, protezione umana, si accumula all’inizio della fase S con picchi nelle fasi G2 – M, e previene l’attivazione prematura delle separine durante la mitosi (Nasmyth et al. 2000).
Il DHT sovra-regola Psmc3, Dusp1, Gadd45g e Pttg1 nelle presenti condizioni. La sovraespressione di Psmc3 aumenta le proteine p53 e p21 (Pollice et al. 2004). In risposta al danno al DNA e ad altri stress, il soppressore del tumore p53 induce l’arresto del ciclo cellulare o l’apoptosi a seconda dei contesti cellulari specifici (Yu & Zhang 2005). In risposta al danno al DNA, p53 promuove la riparazione del DNA influenzando il percorso di riparazione dell’escissione del DNA e arrestando le cellule in G1 attraverso l’induzione di p21 che contribuiscono a fornire più tempo per la riparazione (Smith & Seo 2002), mentre anche l’arresto G1 mediato da p53 si verifica per induzione di Dusp1 in assenza di danni al DNA (Li et al. 2003). Le proteine codificate da Gadd45g interagiscono con p21 e sopprimono la crescita cellulare senza alcuna evidenza di apoptosi (Nakayama et al. 1999). L’arresto della crescita mediato dagli inibitori del ciclo cellulare p21 e Gadd45 inibisce la risposta apoptotica indotta da bersagli apoptotici di p53 (Yu & Zhang 2005). Inoltre, la protezione codificata da Pttg1 inibisce la capacità di p53 di indurre la morte cellulare (Bernal et al. 2002). Nel loro insieme, il DHT potrebbe promuovere l’arresto di G1 senza indurre l’apoptosi, almeno secondo ciò che è emerso dal presente studio.

Il presente studio riporta l’induzione di Amd1 che codifica per la S-adenosilmetionina decarbossilasi (SAMDC), Oaz, Rps20 e Rpl34, nonché Psmc3 e Psmc5 dopo l’iniezione di DHT. D’altra parte, il DHT sotto-regolato Sbp il cui prodotto è correlato all’accumulo di spermatozoi (Moruzzi et al. 1982). I composti policristici sintetizzati dagli enzimi che limitano la velocità, ODC e SAMDC, sono cruciali per la crescita e la proliferazione delle cellule di mammifero. L’antizima ODC codificato da Oaz, così come le proteine ribosomiali L34 e S20, inibiscono le decarbossilasi di arginina e ODC (Panagiotidis et al. 1995). ODC e SAMDC sono degradati dal proteasoma 26S (Yerlikaya e Stanley 2004) che è codificato da Psmc3 e Psmc5. L’antizima ODC inibisce anche l’assorbimento della poliammina e stimola l’escrezione (Sakata et al. 2000). Inoltre, l’assorbimento della poliammina è inibito dal PKC ed è stimolato dalla sua inibizione (Dot et al. 2000). Per coincidenza, Hint1, che inibisce la PKC, aveva un modello di modulazione simile a quello di Oaz con il trattamento a base di DHT. Nel loro insieme, le modulazioni di Pttg1, Cct8, Tctex1, Gorasp2, Akr1a4, Lgals1, Amd1, Oaz, Rpl34, Rps20, Psmc3, Psmc5 e Sbp mediante dal DHT nel presente studio potrebbero riflettere la proliferazione di cellule satelliti / mioblasti nel muscolo scheletrico .
Inoltre, la proteina Pttg1 induce angiogenesi sia in vitro che in vivo (Ishikawa et al. 2001). Nel presente studio, il DHT ha sovra-regolato Pttg1 e Asb5, che è una nuova proteina implicata nell’inizio dell’arteriogenesi (Boengler et al. 2003). La vascolarizzazione è un importante fattore determinante dell’approvvigionamento energetico e della rimozione dei rifiuti durante la contrazione muscolare e la sua stimolazione da parte del DHT in questo studio è quindi in accordo con altri dati presentati.

Nel metabolismo lipidico, la condizione GDX ha spento la Apina2 e il DHT a sovra-regolato la Lpin1. L’apolipoproteina A-II codificata da Apoa2, la seconda proteina più abbondante delle particelle di lipoproteine ad alta densità (HDL), esercita un marcato effetto sul legame HDL e sull’assorbimento selettivo dei lipidi da parte dei recettori scavenger di classe B. Nel topo, l’espressione migliorata di Lpin1 nel muscolo scheletrico promuove l’obesità diminuendo il dispendio energetico dell’intero corpo e l’utilizzo dei grassi, nonché inducendo resistenza all’insulina (Phan & Reue 2005). Contrariamente a quanto accade nel muscolo, la sovraespressione di Lpin1 nel tessuto adiposo provoca obesità senza insulino-resistenza (Phan & Reue 2005). Ho precedentemente riportato che il livello di espressione di Lpin1 nel tessuto adiposo rimane inalterato con il trattamento a base di DHT (Bolduc et al. 2004). L’induzione di Lpin1 solo nel muscolo potrebbe suggerire che il carboidrato fosse usato per aumentare la produzione di OxPhos e ATP. Ulteriori studi sono necessari per chiarire questo intrigante meccanismo.
Le prime risposte all’iniezione di DHT (DHT 1, 3 e 6 h) sono l’induzione sia dei fattori di rilassamento muscolare (Pvalb) che di contrazione (Trdn) che modulano i livelli intracellulari di Ca2+ . Il DHT ha anche indotto le trascrizioni relative alla segnalazione cellulare come Ca2 + (Camk2g), PKC (Hint1) e percorsi MAPK (Dusp1) nonché la biosintesi della poliammina (Amd1, Oaz, Psmc3, Rps20 e Rpl34), proliferazione cellulare (Akr1a4, Cct8 Pttg1 e Tctex1), arresto del ciclo cellulare (Gadd45g), p53 (Cabc1, Dusp1 e Pttg1) e angiogenesi (Asb5 e Pttg1). L’induzione di mRNA correlati alla trascrizione (Ogt, Psmc3 e Psmc5), sintesi proteica (Mrpl51, Ogt, Rps20 e Rpl34), modifica (Cabc1, Cct8 e Ogt) e degradazione (Psmc3 e Psmc5), fosforilazione ossidativa (Cyc1, MtCo1, in questi punti sono stati osservati anche MtCo2, Cyp27a1, Ndufa5 e Ndufb2), produzione di ATP (Atp5j2 e EST Atpaf1), metabolismo lipidico (Lpin1) e immunità (Cd59a e Ga17). Tuttavia, l’induzione di trascrizioni relative alla segnalazione di Ca2+, MAPK, arresto del ciclo cellulare, p53, sintesi proteica e angiogenesi non è più significativa dopo 24 ore dall’iniezione di DHT mentre le trascrizioni relative alla progressione del ciclo cellulare sono ancora sovraregolate. Inoltre, le trascrizioni relative alla sintesi proteica (Rps24 e Rps27) erano sotto-regolate. Questi risultati indicano che l’iniezione di DHT induce la generazione di energia, la sintesi proteica, la funzione mitocondriale e la proliferazione di cellule satellite / mioblasti a livello trascrizionale in vivo, supportando precedenti risultati di un’azione anabolica del composto in questione.
Un altro studio interessante del 2011 e pubblicato sul “The Journal of Physiology” [86] ci offre ulteriori indizzi sul potenziale del DHT nell’ipertrofia muscolare.
Il gruppo di ricerca che ha svolto questo studio ne aveva in precedenza condotto un altro attraverso il quale avevano dimostrato che il Dihydrotestosterone (DHT), ma non il Testosterone, aumenta la produzione di forza nei muscoli a contrazione rapida e la diminuisce in quelli a contrazione lenta. Questi risultati hanno loro suggerito che il DHT poteva essere un androgeno con capacità ben superiori a quelle comunemente attribuiteli. Nel presente studio, i ricercatori hanno esaminato gli effetti di questi ormoni sul trasporto degli aminoacidi nei fasci muscolari dell’apparato muscolo-scheletrico a rapida contrazione del topo. I risultati mostrano che il DHT aumenta la sintesi proteica e l’aumento delle proteine che trasportano aminoacidi essenziali in fasci muscolari a contrazione rapida. Questo non è stato osservato con il Testosterone.

E’ stato osservato che il DHT esercita azioni acute/non genomiche nel muscolo-scheletrico di mammiferi adulti le cui funzioni fisiologiche sono state capite di recente, pertanto l’obiettivo primario di questo studio era di osservare gli effetti acuti / non genomici del DHT sul uptacke di aminoacidi e sugli eventi di trasduzione del segnale cellulare alla base di queste azioni in fasci muscolari scheletrici a contrazione rapida e lenta di topo. Gli aminoacidi marcati con 14C sono stati usati per studiare gli effetti del DHT e del Testosterone (T) sull’assorbimento degli aminoacidi e sono stati usati interventi farmacologici per determinare gli eventi di trasduzione del segnale cellulare che mediano queste azioni. Mentre il T non ha avuto alcun effetto sull’assorbimento di isoleucina (Ile) e acido α-metilamminoisobutirrico (MeAIB) in entrambi i tipi di fibre, il DHT ha aumentato il loro assorbimento nei fasci di fibre a contrazione rapida. Questo effetto è stato invertito dagli inibitori della traslazione proteica, del recettore del prodotto per la crescita epidemica (EGFR), del sistema A, del sistema L, del mTOR e del MEK. Tuttavia, è stato relativamente correlato agli inibitori della trascrizione, dei recettori degli androgeni e dell’IP3K / Akt. In aggiunta, il trattamento con DHT ha aumentato l’espressione della LAT2 e l’insufflazione fosforilata del GRFR, mentre il miscuglio rapido-twitch si mescola e in entrambi i tipi di ERK1 / 2, RSK1 / 2 e ATF2. Inoltre, ha diminuito la fosforilazione di eEF2 e ha aumentato l’incorporazione di proteine di ferro in entrambi i tipi di fibre. La maggior parte di questi effetti è stata superata dagli inibitori di EGFR e MEK. Da questi risultati si ipotizza che un’altra funzione fisiologica delle azioni acute/non genomiche del DHT nelle fibre muscolari isolate dei mammiferi è quella di stimolare l’assorbimento di aminoacidi. Questo effetto è mediato dall’EGFR e comporta l’attivazione della via MAPK e un aumento dell’espressione LAT2.

Un risultato chiave nel presente studio è stato l’osservazione che il trattamento di piccoli fasci di fibre muscolari scheletriche isolati dall’EDL e dal soleo di topi femmine adulti con concentrazioni fisiologiche (630pgml − 1) di DHT, per 1 ora, significativamente (P = 0,001) ha aumentato l’assorbimento di Ile e MeAiB nei fasci di fibre isolati dall’EDL ma non in quelli isolati dal soleo. Sebbene la somministrazione acuta di ormoni come l’insulina (Biolo et al. 1995), il fattore di crescita insulino-simile 1 (IGF-1) (Fryburg et al. 1995) e l’ormone della crescita (Fryburg et al. 1995) hanno dimostrato di aumentare la sintesi proteica e per promuovere l’assorbimento di aminoacidi nel muscolo scheletrico umano, è la prima volta che è stato dimostrato un aumento dell’assorbimento di aminoacidi in risposta alla somministrazione acuta di uno steroide anabolizzante-androgeno nel muscolo scheletrico dei mammiferi adulti. Solo altri due studi hanno precedentemente osservato gli effetti dell’assorbimento di aminoacidi. Entrambi gli studi hanno utilizzato soggetti umani e non sono stati in grado di dimostrare alcun cambiamento nell’assorbimento degli aminoacidi in gruppi muscolari interi (Bhasin et al. 1997; Ferrando et al. 1998). Sebbene nel presente studio siano state utilizzate piccole fibre muscolari e il T sia stata applicato direttamente ai fasci di fibre, è importante notare che questo ormone non ha avuto alcun effetto sull’assorbimento degli aminoacidi in entrambi i tipi di fibre. Al contrario, il trattamento dei fasci di fibre con DHT ha comportato un marcato aumento dell’assorbimento di Ile e MeAIB solo nei fasci di fibre a contrazione rapida (Fig. 1). In precedenza, abbiamo anche dimostrato che il T non ha effetti acuti sulla produzione di forza in fasci muscolari di topo isolati intatti, mentre il DHT ha aumentato la produzione di forza nei fasci di fibre a contrazione rapida, ma l’ha diminuita in quelli a contrazione lenta (Hamdi & Mutungi, 2010). Nel loro insieme, questi risultati suggeriscono che il T potrebbe non avere effetti acuti / non genomici nelle fasce muscolari scheletriche dei mammiferi adulti.
Come già detto, nella maggior parte dei tessuti il T viene convertito in DHT dall’enzima 5 α-reduttasi. Pertanto, è probabile che tutti gli effetti acuti del T osservati in precedenza nei miociti in coltura (Estrada et al. 2003) potrebbero essere stati esercitati dal DHT. In effetti, è stato precedentemente suggerito che gli effetti anabolici del T nei muscoli scheletrici umani possano essere indiretti o secondari al rilascio di un altro ormone come IGF-1 (Ferrando et al. 1998). Con la presente si precisa che oltre all’IGF-1, gli effetti del T nel muscolo scheletrico dei mammiferi possono anche essere esercitati attraverso il rilascio di DHT. I ricercatori suggeriscono anche che il DHT è il principale steroide anabolizzante-androgeno nei muscoli scheletrici dei mammiferi adulti.
Nonostante la maggior parte degli studi è stata effettuata su fasci muscolari di topi femmina, in precedenza era già stato dimostrato che il DHT ha effetti simili sulla produzione di forza nei fasci muscolari scheletrici di topi maschi e femmine (Hamdi & Mutungi, 2010).
I risultati riportati in questo studio (vedi figura seguente) mostrano che sebbene il DHT aumenti l’attività del SNAT2, ciò non influisce sulla sua espressione. Al contrario, aumenta l’attività e l’espressione del LAT2 (vedi Fig. 3). Inoltre, il trattamemto del fascio di fibre muscolari con il classico sistema di inibitori A e L-typeaminoacid ha portato a una marcata riduzione dell’assorbimento basale di L- [U-14C] Ile in entrambi i tipi di fibre e ha completamente soppresso l’aumento indotto da DHT nell’assorbimento di Ile.
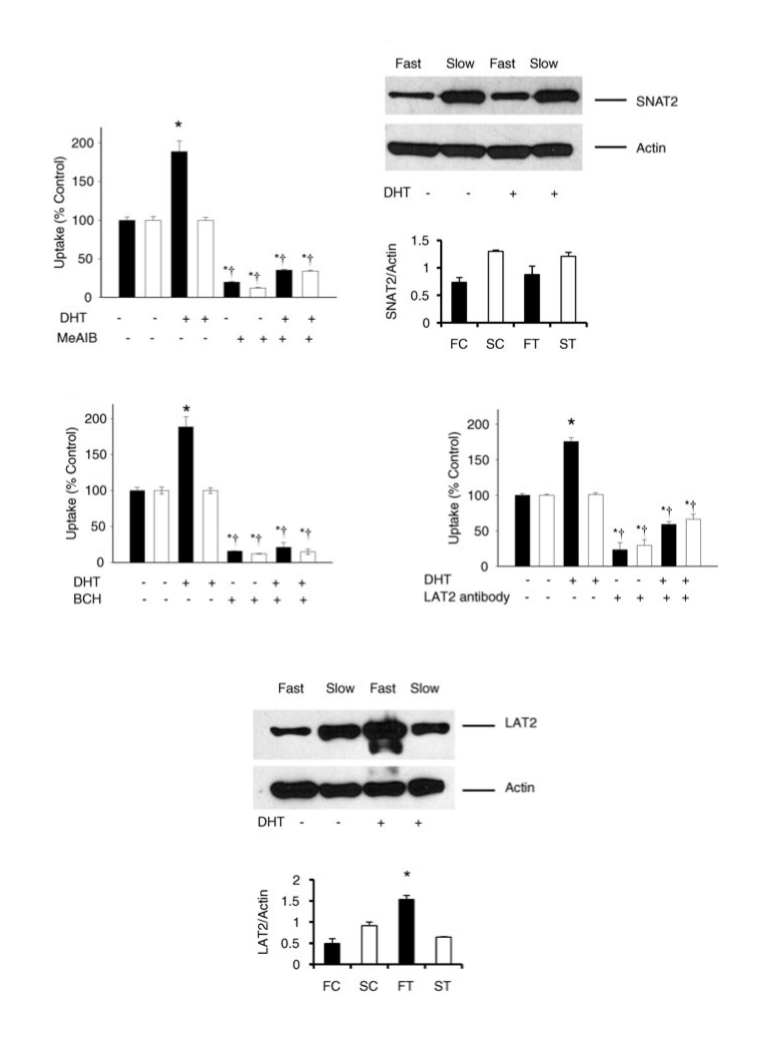
Effetti simili sono stati osservati anche quando i fasci di fibre sono stati trattati con la soluzione di Ringer contenente anticorpi contro il LAT2, suggerendo che gli effetti del DHT sull’Ile sono mediati attraverso questo trasportatore. Da queste osservazioni si ipotizza che i due trasportatori (LAT2, SNAT2) siano in qualche modo collegati. Pertanto, modulando l’espressione e l’attività di LAT2, anche il DHT sembra regolare indirettamente l’attività di SNAT2.

In precedenza, era stato dimostrato che le azioni acute/ non genomiche del DHT sulla produzione di forza nei fasci muscolo-scheletrici di topi adulti sono mediate attraverso il Recettore del Fattore di Crescita dell’Epidermide (EGFR) e comportano l’attivazione di ERK1 / 2 (Hamdi & Mutungi, 2010). È interessante notare che i risultati qui riportati suggeriscono che le azioni acute/non genomiche del DHT sull’assorbimento di aminoacidi nelle fibre muscolari dei mammiferi adulti sono mediate attraverso lo stesso recettore e lo stesso percorso. Inoltre, il pretrattamento dei fasci di fibre con Ciproterone o Flutamide in modo significativo (P <0,05) ha attenuato gli effetti del DHT sull’assorbimento dell’Ile senza sopprimerlo completamente. In precedenza, è stato suggerito che il Testosterone può attivare la via MAPK tramite un recettore degli androgeni accoppiato con proteina G (Estrada et al. 2003). Tuttavia, se questo meccanismo, comunemente indicato come transattivazione, è quello che media gli effetti acuti/non genomici del DHT nelle fibre muscolari dei mammiferi adulti è incerto e sono necessarie ulteriori ricerche per chiarirlo.

Dopo l’attivazione, ERK1 / 2 può rimanere nel citosol o traslare nel nucleo dove svolge un ruolo critico nella regolazione dell’espressione genica e della replicazione del DNA (Brunet et al. 1999). Nel nucleo, ERK1 / 2 fosforila una serie di target, inclusi molti fattori di trascrizione e una famiglia di chinasi correlate a RSK, le chinasi proteiche attivate dallo stress e dal mitogeno (MSK) (Deaketal.1998). Anche se nel presente studio è stato esaminato un gran numero di target a valle di ERK1 / 2, il trattamento con DHT ha aumentato soltanto la fosforilazione di RSK1 / 2 e ATF2 . Inoltre, il DHT non ha avuto alcun effetto sulla fosforilazione degli altri modulatori MAPK. Per i ricercatori, questi risultati suggeriscono che le azioni acute / non genomiche del DHT nei muscoli scheletrici dei mammiferi adulti sono esercitate principalmente attraverso l’EGFR e comportano l’attivazione della modulazione ERK1 / 2 del percorso MAPK. L’ipotesi è che il DHT, direttamente o indirettamente, attivi l’EGFR che a sua volta attiva la via MAPK che porta ad un aumento del trasporto di aminoacidi nelle fibre aumentando anche la sintesi proteica in esse. Inoltre, il DHT sembra avere un attività principale sulle fibre a contrazione rapida.
Negli animali adulti, un aumento della massa muscolo scheletrica (ipertrofia) si verifica principalmente a causa di un aumento delle dimensioni piuttosto che del numero di fibre muscolari ed è generalmente ritenuto che sia regolata dal percorso Akt / mTOR (Glass, 2003). Il percorso Akt / mTOR è attivato da molti stimoli tra cui fattori di crescita, altri ormoni e sostanze nutritive. Inoltre, la sua attivazione culmina nel blocco del apoptosi, induzione della sintesi proteica, trascrizione genica e proliferazione cellulare (Dann etal.2007). Pertanto, è stato stimato che il DHT e il T potessero attivare questo percorso. L’assorbimento di amminoacidi indotto dal DHT nelle fibre a contrazione rapida senza la sua completa soppressione, suggerisce che le azioni acute / non genomiche del DHT non sono mediate attraverso Akt. Invece, i risultati che vengono presentati nel presente studio suggeriscono che il DHT aumenta la sintesi proteica regolando la traduzione dell’mRNA già presente nelle cellule. In effetti, il trattamento dei fasci di fibre muscolari con DHT ha portato a una marcata riduzione della fosforilazione di eEF2 e ad un moderato aumento (∼50%) della sintesi proteica nei fasci di fibre a contrazione rapida.
È anche degno di nota il fatto che il pretrattamento dei fasci di fibre con l’inibitore specifico del mTOR non solo ha ridotto l’assorbimento basale di Ile, ma ha anche soppresso completamente l’aumento indotto dal DHT dell’assorbimento di Ile nei gruppi di fibre a contrazione rapida. Per i ricercatori questi risultati suggeriscono che alcuni degli effetti acuti / non genomici del DHT sono probabilmente mediati attraverso mTOR. In effetti, numerosi studi hanno suggerito che mTOR è il legame tra la disponibilità di aminoacidi e una maggiore sintesi proteica (Beugnet et al. 2003; Avruch et al. 2009). Tuttavia, la rapamicina può anche indurre l’autofagia (Ravikumar et al. 2004). Pertanto, un’altra possibilità è che i suoi effetti siano dovuti all’accumulo di aminoacidi nelle fibre muscolari.
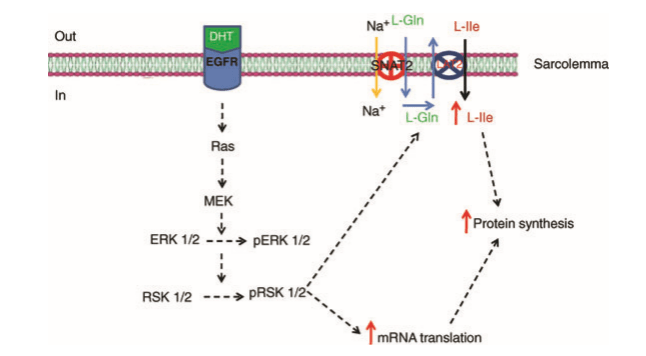
In conclusione, ci sono state prove che dimostrano che un’altra funzione fisiologica delle azioni acute / non genomiche del DHT nelle fibre muscolari dei mammiferi adulti è quella di aumentare l’assorbimento di aminoacidi essenziali. Sebbene non si possa escludere completamente il coinvolgimento del recettore degli androgeni, i principali risultati suggeriscono che l’aumento dell’assorbimento di aminoacidi e la sintesi proteica sono mediati attraverso l’EGFR e comportano l’attivazione del modulo ERK1 / 2 del pathway MAPK che a sua volta attiva RSK1 / 2 portando ad un aumento dell’espressione del trasportatore di aminoacidi di tipo L LAT2.
Piccola parentesi sul Mesterolone
Arrivati a questo punto, prima di trattare le conclusioni sul DHT, vorrei riportarvi due interessanti studi nei quali si è osservata l’azione di una forma di DHT metilata in C-1, il noto Mesterolone, sulla massa muscolare.

Senza dilungarsi troppo in preamboli, come ben sappiamo, il Mesterolone (nome commerciale Proviron) [1 alpha-methyl-17 beta- hydroxy-5 alpha-androstan-3-one] è un AAS derivato dal Dihydrotestosterone (DHT). A differenza del DHT il Mesterolone presenta l’aggiunta di un gruppo metilico in C1 (similmente al Metenolone) cosa che ne aumenta discretamente la biodisponibilità orale, senza però apportare eccessivo stress epatico. Questa alterazione però non aumenta la stabilità del C3 chetogruppo, essenziale per l’attività anabolizzante a livello muscolare mediata dal legame recettoriale, come il suo precursore.
Ora, sappiamo anche che ci sono frequenti segnalazioni di abuso di Mesterolone negli sport umani ed equini per il miglioramento della prestazione. Tuttavia, sono disponibili informazioni limitate su come questo farmaco esercita i suoi effetti sul muscolo scheletrico.
Le cellule satellite (SC) sono cellule staminali miogeniche mononucleari che contribuiscono alla crescita e alla riparazione dei muscoli postnatali. Poiché l’attivazione delle SC e la successiva differenziazione nei nuovi myonuclei sono un evento importante durante l’ipertrofia muscolare. In uno studio pubblicato nel maggio del 2012 [87], si è osservata l’influenza del Mesterolone sulla distribuzione delle SC all’interno del muscolo pettorale dei polli (Gallus gallus ). Nello specifico, questo studio ha testato le ipotesi secondo cui che il Mesterolone induca l’ipertrofia del muscolo scheletrico aviario e che aumenti anche il numero di SC nel muscolo scheletrico aviario. Sono state utilizzate solide tecniche immunocitochimiche e analisi morfometriche per calcolare il numero di SC e myonuclei. Inoltre, sono stati misurati i livelli di concentrazione di DNA e proteine Pax7 per confermare i risultati immunocitochimici. Il Mesterolone ha aumentato significativamente la massa pettorale e le dimensioni delle fibre. Tutti gli indici delle SC e il numero di myonuclei sono aumentati significativamente con la somministrazione di Mesterolone. Inoltre, negli uccelli trattati con Mesterolone sono state riscontrate una maggiore concentrazione di DNA ed espressione della proteina Pax7. Questo studio indica che il Mesterolone può indurre ipertrofia del muscolo scheletrico aviario e che questo è correlato con un aumento del numero di SC. I ricercatori suggeriscono che le SC siano intermediari cellulari chiave per l’ipertrofia muscolare indotta da Mesterolone. L’ipotesi, che necessità di ulteriori ricerche, è che tale effetto possa riscontrarsi anche in altre specie compreso l’uomo.
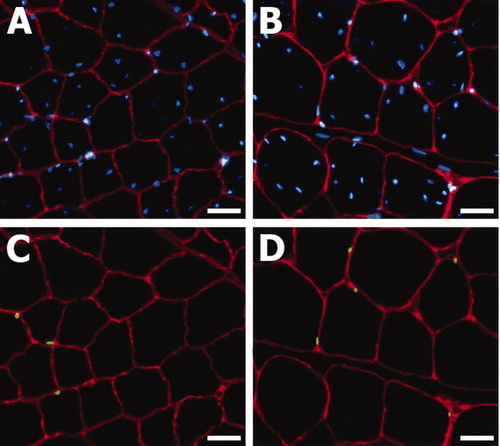

In un altro studio pubblicato nel 2010 [88], la microscopia ottica ed elettronica e la morfometria quantitativa sono state utilizzate per determinare gli effetti dell’esercizio e del Mesterolone sul muscolo soleo dei topi. Sia l’esercizio fisico che il Mesterolone hanno causato una significativa ipertrofia delle fibre muscolari extrafusali. L’ipertrofia delle fibre di tipo I era maggiore di quella delle fibre di tipo II. Non c’era iperplasia. I mitocondri erano più numerosi e più grandi rispetto a quanto osservato nei muscoli degli animali sedentari. La capillarità è aumentata e sono comparse piccole fibre muscolari nucleate centralmente, di solito in piccoli gruppi e molto spesso nei muscoli degli animali esposti al Mesterolone. Una piccola percentuale di cellule satelliti mostrava segni di attivazione ma nei muscoli degli animali trattati con Mesterolone c’era una massa muscolare maggiore dopo l’esercizio. I muscoli di animali che erano stati entrambi fatti esercitati e trattati con Mesterolone presentavano i maggiori cambiamenti: la massa muscolare e l’ipertrofia delle fibre muscolari erano maggiori rispetto a tutti gli altri gruppi di animali, la capillarità era maggiore e> il 30% di tutte le cellule satellitari riconosciute mostrava segni di attivazione. Gruppi di piccole fibre muscolari nucleate centralmente sono state comunemente osservate in questi muscoli. Sembravano essere il risultato di lacerazioni rigenerate in fibre muscolari esistenti. Sia con l’esercizio fisico sia con il Mesterolone, da solo o in combinazione, si è verificato un aumento della percentuale di fibre muscolari di tipo I e una diminuzione della proporzione di tipo II.
Entrambi gli studi esposti, sebbene non siano di grande impatto, fanno sicuramente nascere il dubbio in coloro i quali hanno sempre valutato le possibili azioni di una molecola in modo ristretto, sia per mancanza di una conoscenza sufficienza in materia sia per limitatezza nel formulare ipotesi estrapolate dall’osservazione.
Ora, non sto sicuramente dicendo che un culturista trattato con solo Mesterolone possa ambire a grandi cambiamenti nella composizione corporea. Sto semplicemente ipotizzando, che le nozioni in merito alle attività degli AAS sono datate e parziali, anche perchè si basano per lo più, tanto quanto gli studi esposti, sulla capacità di legame degli AAS testati osservata nella prostata e nel levator ani dei topi. Inoltre, il Mesterolone ha visto una riscoperta come farmaco ancillare nella TRT o come anti-depressivo funzionale in alcune tipologie di depressione.
In fondo, il peggior difetto del Mesterolone è dipeso dalla sua consuetudinaria via di somministrazione…
Nota: la biodisponibilità orale del Mesterolone è stata stimata al 3%.
Tiriamo le somme…con possibili critiche…
Già sento i soliti limitati in intelletto e pazienza, sempre pronti a parlare senza cognizione di causa, urlare al “esiste lo studio X che afferma che l’aggiunta di Dutasteride con dosi sovrafisiologiche di Testosterone non cambia il risultato!” … Lo conosco anche io capre!… A proposito, vediamo di cosa si tratta…

Il principale studio è quello pubblicato su JAMA nel 2012.[89] Si tratta di uno studio in doppio cieco, randomizzato, controllato con placebo. Lo studio è stato diretto dal dott. Bhasin e colleghi, i quali hanno reclutato 139 uomini sani, di età compresa tra 18 e 50 anni, con livelli normali di Testosterone.
Ai pazienti è stata assegnata 1 su 4 dosi di Testosterone Enantato (50, 125, 300 o 600 mg / settimana) più 2,5mg/die di Dutasteride o sono stati assegnati a 1 su 4 gruppi a cui è stato somministrato 1 di 4 dosi di Testosterone Enantato (50, 125, 300 o 600 mg / settimana) più placebo per 20 settimane.

Il cambiamento nella massa magra rispetto al basale, misurata dall’assorbtiometria a raggi X a doppia energia, è stato il risultato primario. I ricercatori hanno anche misurato i livelli di Testosterone, la forza muscolare, la funzione sessuale, la produzione di sebo e l’acne.
La forza nel Leg Press e del petto sono state misurate con il metodo 1 ripetizione massimale con l’uso di macchine Keizer.
La funzione sessuale è stata valutata con l’indice internazionale della funzione erettile e il questionario sulla salute sessuale maschile per una valutazione più completa del desiderio sessuale.
Il volume della prostata è stato misurato con la risonanza magnetica 1.5-Tesla.
La produzione di sebo è stata misurata con l’uso di nastri di sebo. La scala Palatzi è stata utilizzata per valutare l’acne.
139 uomini furono assegnati in modo casuale; 102 (54 nei gruppi placebo e 48 nei gruppi dutasteride) hanno completato l’intervento di 20 settimane.
Gli uomini assegnati alla Dutasteride erano simili al basale degli uomini assegnati al placebo. Inoltre, i livelli di Testosterone totale e libero non differivano tra i due gruppi.
L’aumento della massa magra ottenuta dai gruppi Dutasteride+Testosterone era di 0,6 kg (IC 95%, da -0,1 a 1,2 kg) quando ricevevano 50 mg/settimana di Testosterone Enantato, 2,6 kg (IC 95%, 0,9 – 4,3 kg) per 125mg/settimana, 5,8 kg (IC 95%, 4,8 – 6,9 kg) per 300mg/settimana e 7,1kg (IC 95%, 6,0 – 8,2 kg) per 600 mg/settimana.
La massa magra ottenuta dai gruppi placebo+Testosterone era di 0,8 kg (IC 95%, da -0,1 a 1,7 kg) quando ricevevano 50mg/settimana di Testosterone Enantato, 3,5 kg (IC 95%, 2,1-4,8 kg) per 125 mg/settimana, 5,7 kg (IC 95%, 4,8 – 6,5 kg) per 300mg/settimana e 8,1 kg (IC 95%, 6,7 – 9,5 kg) per 600mg/settimana.
Le differenze dose-dipendente tra i gruppi Dutasteride e placebo per la massa magra non erano significative (P = .18).
I cambiamenti nella massa grassa, nella forza muscolare, nella funzione sessuale, nel volume della prostata, nella produzione di sebo e nei livelli di ematocrito e lipidi non differivano tra i gruppi.
La frequenza complessiva di eventi avversi, inclusa la frequenza di disfunzione sessuale, acne, vampate di calore e dolorabilità mammaria era simile nei gruppi placebo e dutasteride.
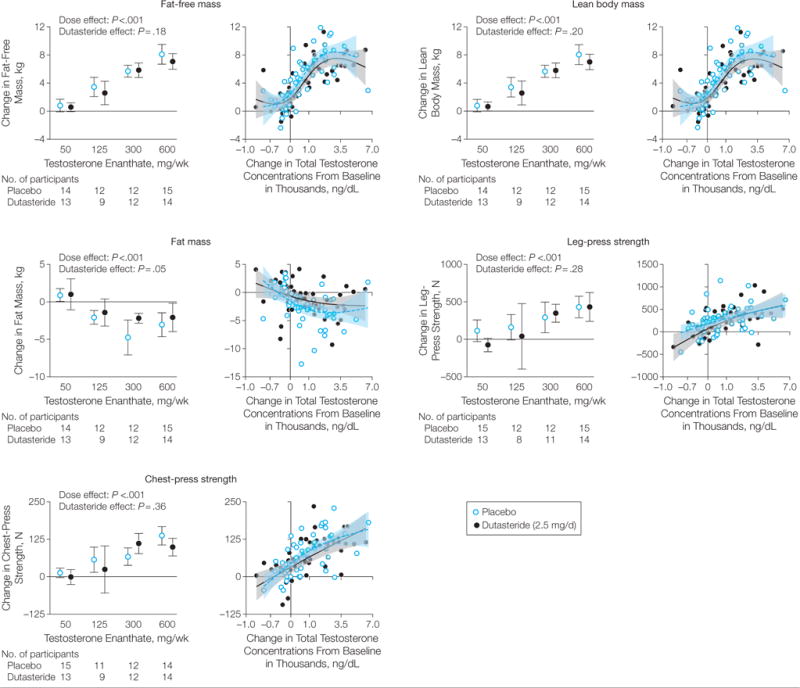
Nei grafici a sinistra, i marker indicati hanno un margine di errore con intervalli di confidenza al 95%. Nei grafici a destra (variazione dei livelli di Testosterone), le scale dell’asse orizzontale sono state spostate (offset) di 1000ng/dL e quindi è stata applicata una trasformazione della radice quadrata. Il livellamento semiparametrico è stato ottenuto utilizzando modelli di additivi generalizzati. Le aree ombreggiate indicano intervalli di confidenza al 95%.
Bene…possiamo cestinare tutto quanto ipotizzato in precedenza? Visto anche il tipo di studio esposto? Non esattamente …
Ora, da notare la tipologia di soggetti arruolati e il loro grado di “maturità sportiva”, più specificatamente negli allenamenti contro resistenza. Essa non è chiaramente specificata e la misurazione dell’espressione della forza in soggetti poco o per nulla allenati non è un grande parametro sebbene lo scopo dello studio fosse quello di constatare l’impatto nella forza e ipertrofia dato da un protocollo a dosaggio differenziato di Testosterone Enantato con o senza un inibitore della 5α-reduttasi (Dutasteride).
Secondo punto da notare, la mancanza di misurazione specifica della massa muscolare. Infatti, la composizione corporea dei partecipanti è stata valutata per i parametri di massa grassa e massa magra. Come risaputo, quando si parla di massa magra si prende anche in considerazione l’acqua. Sebbene la differenza sia bassa, probabilmente essa è da ricollegare anche al fatto che le dosi di Testosterone utilizzate erano differenti e con limite a 600mg di Testosterone Enantato a settimana (pari a 432mg di Testosterone), e che tale dosaggio non sempre crea iperestrogenemia marcata (considerando anche un lasso di tempo contenuto) tale da causare accumuli sensibili di acqua extracellulare. Considerando poi che uno degli effetti collaterali collegati all’uso di inibitore della 5α-reduttasi sia proprio un aumento degli estrogeni circolanti (per aumento del substrato di sintesi) con ripercussioni a carico di (e non solo limitate a) ritenzione idrica, accumulo di grasso con modello ginoide e ginecomastia, i dubbi sulle metodiche di analisi dei partecipanti allo studio diventano senz’altro dubbie.
Da notare che il Dutasteride è stato osservato ridurre il DHT sierico del >90% e quello intraprostatico del 94% alla dose di 0.5mg/die.[90] Nello studio presentato, i partecipanti assegnati ai gruppi Dutasteride e Dutasteride+Testosterone erano trattati con una dose di Dutasteride pari a 2,5mg/die.
I ricercatori volevano condurre uno studio meticolosamente progettato ed eseguito per rispondere a una domanda vecchia di quasi 5 decenni: il Testosterone, il DHT o entrambi a livelli fisiologici e soprafisiologici sono importanti per il guadagno della massa magra? Purtroppo sembra che non siano stati sufficientemente meticolosi…
Non è di certo mia intenzione far valere di più uno studio svolto in vitro o su animali rispetto ad uno svolto su esseri umani. E’ invece mia intenzione far riflettere il lettore sul design di uno studio, ed in base al livello di questo poter valutare quanto in esso riportato.
Un altra critica riduttiva che potrebbe essere mossa contro le nuove ipotesi di attività del DHT potrebbe essere riferita all’enzima 3α-Hydroxysteroide dehydrogenasi (3α-HSD). Si dimentica però che tale enzima è un “limitatore” dell’attività del DHT a livello di tessuti come quello muscolare e adiposo. Infatti, la sua azione non esclude assolutamente la potenziale attività in acuto e non genomica del DHT nei tessuti dove l’enzima 3α-HSD viene espresso. E’ possibile che la cooperatività del DHT con il Testosterone sia di tipo sequenziale: attività prettamente recettoriale e in cronico (sebbene sotto regolazione organica) data dal Testosterone preceduta e seguita da una attività acuta e non genomica data dal DHT.
Inoltre, ed è una cosa molto importante da tenere in considerazione, la ricerca è tutt’ora in essere. Esistono ipotesi diverse con il loro bagaglio di ricerca. Ciò che il lettore preparato può fare è semplicemente soppesare le informazioni raccolte al fine di farsi un idea il più concreta possibile della questione.
Sebbene la ricerca scientifica abbia fatto enormi passi avanti nell’ultimo secolo, siamo ancora lungi dal conoscere tutto… anche quando si parla di ormoni e la loro attività diretta e indiretta…
Nota conclusiva: è ovvio che non si mette in dubbio l’utilità del controllo terapeutico del DHT in condizioni patologiche (vedi iperplasia prostatica maligna) o preventive in particolari soggetti. Negli individui in fisiologia e senza particolari predisposizioni, l’uso di inibitori della 5α-reduttasi potrebbe risultare una scelta controproducente sotto molteplici aspetti.
Gabriel Bellizzi
Riferimenti:
- Schnitzer R (1 January 1967). Experimental Chemotherapy. Elsevier Science. pp. 156–. ISBN 978-0-323-14611-1.
- Krüskemper H (22 October 2013). Anabolic Steroids. Elsevier. pp. 12–. ISBN 978-1-4832-6504-9.
- Taylor WN (16 January 2002). Anabolic Steroids and the Athlete, 2d ed. McFarland. pp. 178–. ISBN 978-0-7864-1128-3.
- William Andrew Publishing (2007). Pharmaceutical Manufacturing Encyclopedia. William Andrew Pub. ISBN 978-0-8155-1526-5.
- Newsweek. Newsweek. 1953.
- New and Nonofficial Drugs. Lippincott. 1958.
- Rubin BL, Dorfman RI (1956). “In vitro conversion of testosterone to 17beta-hydroxyandrostan-3-one”. Proc. Soc. Exp. Biol. Med. 91 (4): 585–6. doi:10.3181/00379727-91-22337. PMID 13323010.
- Agmo A (18 April 2011). Functional and Dysfunctional Sexual Behavior: A Synthesis of Neuroscience and Comparative Psychology. Academic Press. pp. 196–. ISBN 978-0-08-054938-5.
- Oreopoulos DG, Michelis M, Herschorn S (6 December 2012). Nephrology and Urology in the Aged Patient. Springer Science & Business Media. pp. 495–. ISBN 978-94-011-1822-4.
- Webster GF, Rawlings AV (17 May 2007). Acne and Its Therapy. CRC Press. pp. 168–. ISBN 978-1-4200-1841-7.
- Smith LB, Mitchell RT, McEwan IJ (1 October 2013). Testosterone: From Basic Research to Clinical Applications. Springer Science & Business Media. pp. 5–. ISBN 978-1-4614-8978-8.
- Anawalt BD (2017). “Is Dihydrotestosterone a Classic Hormone?”. Endocr. Rev. 38 (3): 170–172. doi:10.1210/er.2017-00091. PMID 28582536.
- Azzouni F, Mohler J (2012). “Role of 5α-reductase inhibitors in benign prostatic diseases”. Prostate Cancer Prostatic Dis. 15 (3): 222–30.
- Melmed S (2016). Williams Textbook of Endocrinology. Elsevier Health Sciences. pp. 621, 711.
- Blume-Peytavi U, Whiting DA, Trüeb RM (26 June 2008). Hair Growth and Disorders. Springer Science & Business Media. pp. 161–162.
- Rhoades RA, Bell DR (18 January 2012). Medical Phisiology: Principles for Clinical Medicine. Lippincott Williams & Wilkins. pp. 690–.
- Rakel D (12 April 2012). Integrative Medicine E-Book. Elsevier Health Sciences. pp. 321–.
- Morrison MF (4 May 2000). Hormones, Gender and the Aging Brain: The Endocrine Basis of Geriatric Psychiatry. Cambridge University Press. pp. 17–.
- Azzouni F, Godoy A, Li Y, Mohler J (2012). “The 5 alpha-reductase isozyme family: a review of basic biology and their role in human diseases”. Advances in Urology. 2012: 1–18.
- Zouboulis CC, Chen WC, Thornton MJ, Qin K, Rosenfield R (2007). “Sexual hormones in human skin”. Horm. Metab. Res. 39 (2): 85–95.
- Bolognia JL, Jorizzo JL, Schaffer JV (8 June 2012). Dermatology E-Book. Elsevier Health Sciences. pp. 1094–. ISBN 978-0-7020-5182-1.
- Murphy MJ (24 March 2011). Molecular Diagnostics in Dermatology and Dermatopathology. Springer Science & Business Media. pp. 373–.
- eam SJ, Scott LJ (2008). “Dutasteride: a review of its use in the management of prostate disorders”. Drugs. 68 (4): 463–85.
- Heesakkers J, Chapple C, Ridder DD, Farag F (24 February 2016). Practical Functional Urology. Springer. pp. 280–.
- Nieschlag E, Behre HM, Nieschlag S (26 July 2012). Testosterone: Action, Deficiency, Substitution. Cambridge University Press. pp. 61–.
- Dunn JF, Nisula BC, Rodbard D (July 1981). “Transport of steroid hormones: binding of 21 endogenous steroids to both testosterone-binding globulin and corticosteroid-binding globulin in human plasma”. J. Clin. Endocrinol. Metab. 53 (1): 58–68.
- Williams DA, Foye WO, Lemke TL (2002). Foye’s Principles of Medicinal Chemistry. Lippincott Williams & Wilkins. pp. 707–.
- Coutts, S. B.; Kicman, A. T.; Hurst, D. T.; Cowan, D. A. (1997-11-01). “Intramuscular administration of 5α-dihydrotestosterone heptanoate: changes in urinary hormone profile”. Clinical Chemistry. 43 (11): 2091–2098.
- Marks LS (2004). “5α-reductase: history and clinical importance”. Rev Urol. 6 Suppl 9: S11–21.
- Horton R (1992). “Dihydrotestosterone is a peripheral paracrine hormone”. J. Androl. 13 (1): 23–7. doi:10.1002/j.1939-4640.1992.tb01621.x (inactive 2020-03-09).
- Wilson JD (1996). “Role of dihydrotestosterone in androgen action”. Prostate Suppl. 6: 88–92.
- Swerdloff RS, Dudley RE, Page ST, Wang C, Salameh WA (2017). “Dihydrotestosterone: Biochemistry, Physiology, and Clinical Implications of Elevated Blood Levels”. Endocr. Rev. 38 (3): 220–254.
- Bhasin S (13 February 1996). Pharmacology, Biology, and Clinical Applications of Androgens: Current Status and Future Prospects. John Wiley & Sons. pp. 72–.
- Hay ID, Wass JA (26 January 2009). Clinical Endocrine Oncology. John Wiley & Sons. pp. 37–.
- Melmed S (2016). Williams Textbook of Endocrinology. Elsevier Health Sciences. pp. 621, 711.
- Jin Y, Penning TM (2001). “Steroid 5alpha-reductases and 3alpha-hydroxysteroid dehydrogenases: key enzymes in androgen metabolism”. Best Pract. Res. Clin. Endocrinol. Metab. 15 (1): 79–94.
- Llewellyn W (2009). Anabolics. Molecular Nutrition Llc. pp. 19, 163.
- Blume-Peytavi U, Whiting DA, Trüeb RM (26 June 2008). Hair Growth and Disorders. Springer Science & Business Media. pp. 161–162.
- Azzouni F, Mohler J (2012). “Role of 5α-reductase inhibitors in benign prostatic diseases”. Prostate Cancer Prostatic Dis. 15 (3): 222–30.
- Azzouni F, Mohler J (2012). “Role of 5α-reductase inhibitors in prostate cancer prevention and treatment”. Urology. 79 (6): 1197–205.
- Lotti F, Maggi M (28 April 2015). “Hormonal Treatment for Skin Androgen-Related Disorders”. In Katsambas A, Lotti T, Dessinioti C, D’Erme AM (eds.). European Handbook of Dermatological Treatments. Springer. pp. 1451–1464.
- Wendowski, Oskar; Redshaw, Zoe; Mutungi, Gabriel (February 2017). “Dihydrotestosterone treatment rescues the decline in protein synthesis as a result of sarcopenia in isolated mouse skeletal muscle fibres”. Journal of Cachexia, Sarcopenia and Muscle. 8 (1): 48–56.
- Kohtz AS, Frye CA (2012). Dissociating behavioral, autonomic, and neuroendocrine effects of androgen steroids in animal models. Methods Mol. Biol. Methods in Molecular Biology. 829. pp. 397–431.
- Mozayani A, Raymon L (18 September 2011). Handbook of Drug Interactions: A Clinical and Forensic Guide. Springer Science & Business Media. pp. 656–.
- Hemat RA (2004). Principles Of Orthomolecularism. Urotext. p. 426.
- Grino PB, Griffin JE, Wilson JD (February 1990). “Testosterone at high concentrations interacts with the human androgen receptor similarly to dihydrotestosterone”. Endocrinology. 126 (2): 1165–72.
- Wilderer PA (1 September 2010). “Bioassays for Estrogenic and Androgenic Effects of Water Constituents”. Treatise on Water Science, Four-Volume Set. Newnes. pp. 1805–.
- Diamanti-Kandarakis E (1999). “Current aspects of antiandrogen therapy in women”. Current Pharmaceutical Design. 5 (9): 707–23. PMID 10495361.
- von Deutsch DA, Abukhalaf IK, Lapu-Bula R (15 October 2003). “Anabolic Doping Agents”. In Mozayani A, Raymon L (eds.). Handbook of Drug Interactions: A Clinical and Forensic Guide. Springer Science & Business Media. pp. 510–.
- Swerdloff RS, Wang C (October 1998). “Dihydrotestosterone: a rationale for its use as a non-aromatizable androgen replacement therapeutic agent”. Baillière’s Clinical Endocrinology and Metabolism. 12 (3): 501–6.
- Kohtz AS, Frye CA (2012). Dissociating behavioral, autonomic, and neuroendocrine effects of androgen steroids in animal models. Methods Mol. Biol. Methods in Molecular Biology. 829. pp. 397–431.
- Rizner TL, Lin HK, Peehl DM, Steckelbroeck S, Bauman DR, Penning TM (July 2003). “Human type 3 3alpha-hydroxysteroid dehydrogenase (aldo-keto reductase 1C2) and androgen metabolism in prostate cells”. Endocrinology. 144 (7): 2922–32.
- Weiner IB, Gallagher M (2003). Handbook of Psychology, Biological Psychology. John Wiley & Sons. pp. 333–.
- Schill W, Comhaire FH, Hargreave TB (26 August 2006). Andrology for the Clinician. Springer Science & Business Media. pp. 243–.
- Hyde TE, Gengenbach MS (2007). Conservative Management of Sports Injuries. Jones & Bartlett Learning. pp. 1100–.
- “Androstanolone Drug Profile”. Adis Insight. 4 December 2006.
- Elks J (14 November 2014). The Dictionary of Drugs: Chemical Data: Chemical Data, Structures and Bibliographies. Springer. pp. 640–.
- Index Nominum 2000: International Drug Directory. Taylor & Francis. January 2000. pp. 63–.
- List PH, Hörhammer L (12 March 2013). Chemikalien und Drogen: Teil B: R, S. Springer-Verlag. pp. 523–.
- “Drugs@FDA: FDA Approved Drug Products”. United States Food and Drug Administration. Retrieved 16 November 2016.
- “Drug Product Database – Health Canada”. Health Canada. Retrieved 13 November 2016.
- Blume-Peytavi U, Whiting DA, Trüeb RM (26 June 2008). Hair Growth and Disorders. Springer Science & Business Media. pp. 161–162.
- Azzouni F, Mohler J (2012). “Role of 5α-reductase inhibitors in prostate cancer prevention and treatment”. Urology. 79 (6): 1197–205.
- Lotti F, Maggi M (28 April 2015). “Hormonal Treatment for Skin Androgen-Related Disorders”. In Katsambas A, Lotti T, Dessinioti C, D’Erme AM (eds.). European Handbook of Dermatological Treatments. Springer.
- Wendowski, Oskar; Redshaw, Zoe; Mutungi, Gabriel (February 2017). “Dihydrotestosterone treatment rescues the decline in protein synthesis as a result of sarcopenia in isolated mouse skeletal muscle fibres”. Journal of Cachexia, Sarcopenia and Muscle. 8 (1): 48–56.
- Kohtz AS, Frye CA (2012). Dissociating behavioral, autonomic, and neuroendocrine effects of androgen steroids in animal models. Methods Mol. Biol. Methods in Molecular Biology. 829. pp. 397–431.
- Llewellyn W (2009). Anabolics. Molecular Nutrition Llc. pp. 19, 163.
- Okeigwe I, Kuohung W (2014). “5-Alpha reductase deficiency: a 40-year retrospective review”. Curr Opin Endocrinol Diabetes Obes. 21 (6): 483–7.
- Heesakkers J, Chapple C, Ridder DD, Farag F (24 February 2016). Practical Functional Urology. Springer. pp. 280–.
- Imperato-McGinley J, Zhu YS (2002). “Androgens and male physiology the syndrome of 5alpha-reductase-2 deficiency”. Mol. Cell. Endocrinol. 198 (1–2): 51–9.
- Coutts, S. B.; Kicman, A. T.; Hurst, D. T.; Cowan, D. A. (1997-11-01). “Intramuscular administration of 5α-dihydrotestosterone heptanoate: changes in urinary hormone profile”. Clinical Chemistry. 43 (11): 2091–2098.
- Imperato-McGinley J, Peterson RE, Gautier T, Sturla E (1979). “Androgens and the evolution of male-gender identity among male pseudohermaphrodites with 5alpha-reductase deficiency”. N. Engl. J. Med. 300 (22): 1233–7.
- Kang HJ, Imperato-McGinley J, Zhu YS, Rosenwaks Z (2014). “The effect of 5α-reductase-2 deficiency on human fertility”. Fertil. Steril. 101 (2): 310–6.
- Katz MD, Cai LQ, Zhu YS, Herrera C, DeFillo-Ricart M, Shackleton CH, Imperato-McGinley J (1995). “The biochemical and phenotypic characterization of females homozygous for 5 alpha-reductase-2 deficiency”. J. Clin. Endocrinol. Metab. 80 (11): 3160–7.
- Cilotti A, Danza G, Serio M (2001). “Clinical application of 5alpha-reductase inhibitors”. J. Endocrinol. Invest. 24 (3): 199–203.
- Bradbury R (30 January 2007). Cancer. Springer Science & Business Media. pp. 49–.Burchum J, Rosenthal L (2 December 2014). Lehne’s Pharmacology for Nursing Care. Elsevier Health Sciences. pp. 803–.
- Bostwick DG, Cheng L (24 January 2014). Urologic Surgical Pathology. Elsevier Health Sciences. pp. 492–.
- Harris GS, Kozarich JW (1997). “Steroid 5alpha-reductase inhibitors in androgen-dependent disorders”. Curr Opin Chem Biol. 1 (2): 254–9.
- Sun J, Xiang H, Yang LL, Chen JB (2011). “A review on steroidal 5α-reductase inhibitors for treatment of benign prostatic hyperplasia”. Curr. Med. Chem. 18 (23): 3576–89.
- Torres F (2015). Androgenetic, diffuse and senescent alopecia in men: practical evaluation and management. Curr. Probl. Dermatol. Current Problems in Dermatology. 47. pp. 33–44.
- Check JH, Cohen R (2015). “An update on the treatment of female alopecia and the introduction of a potential novel therapy”. Clin Exp Obstet Gynecol. 42 (4): 411–5.
- Blume-Peytavi U, Whiting DA, Trüeb RM (26 June 2008). Hair Growth and Disorders. Springer Science & Business Media. pp. 182, 369.
- Check JH, Cohen R (2015). “An update on the treatment of female alopecia and the introduction of a potential novel therapy”. Clin Exp Obstet Gynecol. 42 (4): 411–5.
- Blume-Peytavi U, Whiting DA, Trüeb RM (26 June 2008). Hair Growth and Disorders. Springer Science & Business Media. pp. 182, 369.
- https://jme.bioscientifica.com/view/journals/jme/36/2/0360247.xml
- https://physoc.onlinelibrary.wiley.com/doi/pdf/10.1113/jphysiol.2011.207175
- https://pubmed.ncbi.nlm.nih.gov/22419647/
- https://pubmed.ncbi.nlm.nih.gov/19854955/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6035750/
- https://www.nature.com/articles/4500931
