Per accedere alla prima parte clicca qui.
Le mistificazioni e i luoghi comuni sull’Insulina nel mondo del Fitness e BodyBuilding:

I luoghi comuni completamente o in buona parte errati sull’Insulina abbondano nel settore del Fitness e del BodyBuilding. Uno di questi luoghi comuni riguarda un’elevata assunzione di carboidrati e la sua presunta correlazione con livelli cronicamente (e sottolineo cronicamente) elevati di Insulina, i quali porterebbero il soggetto a ingrassare dal momento che la lipogenesi supererà costantemente la lipolisi (ricordate che l’aumento di grasso può avvenire solo se il tasso di lipogenesi supera quello di lipolisi). Tuttavia, nelle persone sane l’Insulina aumenta solo in risposta ai pasti. Ciò significa che la lipogenesi supera la lipolisi solo nelle ore successive al pasto (il cosiddetto periodo postprandiale). Durante i periodi di digiuno (come i periodi prolungati tra un pasto e l’altro o quando si dorme), la lipolisi supera la lipogenesi (cioè si ossidano i grassi). Nell’arco delle 24 ore, tutto si equilibra (a patto che non si assumano più calorie di quante se ne consumino), il che significa che non si ingrassa. Ecco un grafico che mostra come funziona:

Questo è ovviamente solo un grafico approssimativo, ma l’area rossa rappresenta la lipogenesi che si verifica in risposta a un pasto. L’area blu rappresenta la lipolisi che si verifica in risposta al digiuno tra i pasti e durante il sonno. Nell’arco delle 24 ore, questi valori si bilanciano, a patto che non si assumano più calorie di quante se ne consumino. Questo è vero anche se l’assunzione di carboidrati è elevata. Inoltre, se l’apporto energetico è inferiore al dispendio energetico, una dieta ad alto contenuto di carboidrati comporta una perdita di peso come qualsiasi altra dieta.
- Insulina, HSL e ASP
Un altro luogo comune sull’Insulina riguarda la sua necessità per l’accumulo di grasso. Peccato che non sia così. Il corpo ha modi per immagazzinare e trattenere i grassi anche quando l’Insulina è bassa. Ad esempio, nelle cellule adipose è presente un enzima chiamato lipasi ormonosensibile (HSL). L’HSL aiuta a scomporre i Trigliceridi di deposito in acidi grassi liberi. L’Insulina sopprime l’attività dell’HSL e quindi la scomposizione dei Trigliceridi. Questo ha portato le persone a puntare il dito contro i carboidrati come causa dell’aumento di grasso.
Tuttavia, i grassi sopprimono l’HSL anche quando i livelli di Insulina sono bassi. Ciò significa che non è possibile perdere grasso anche quando l’apporto di carboidrati è basso, se si esagera con le calorie. Se non si mangiassero carboidrati ma 5.000 calorie di grassi, non si riuscirebbe comunque a perdere grasso anche se l’Insulina non sarebbe elevata. Questo perché l’elevato apporto di grassi sopprime l’HSL. Questo significa anche che, se si segue una dieta a basso contenuto di carboidrati, per perdere peso è necessario mangiare meno calorie di quelle che si consumano.
Non dimentichiamoci del ruolo della proteina ASP (Proteina Stimolante l’Acilazione) e della sua marcata azione stimolante sulla sintesi di triacilglicerolo negli adipociti umani e nei fibroblasti cutanei. L’ASP è anche nota per il suo aumento del trasporto del glucosio e per la sua azione inibitoria sulla lipasi ormono-sensibile insulino-indipendente. A causa di queste azioni, è legata alla patogenesi dell’obesità, essendo stata dimostrata la sua presenza a livelli elevati in pazienti con obesità, diabete mellito di tipo II e malattia coronarica.
Ora, qualcuno potrebbe dire: “Provate a consumare 5.000 calorie di olio d’oliva e vedrete che risultati otterrete”. Beh, 5000 calorie di olio d’oliva non sono molto appetibili, quindi è ovvio che probabilmente non si riuscirà nell’impresa, soprattutto con regolarità. La stessa cosa accadrebbe consumando 5.000 calorie di puro zucchero da tavola.
Fermo restando che è ormai noto che l’Insulina sopprime acutamente l’appetito. Questo è stato dimostrato in decine e decine di esperimenti. Nonostante anche questa evidenza venga negata da alcuni.
- Proteine e stimolo insulinico
Molti pensano che l’Insulina sia legata solo e soltanto al consumo di Carboidrati (eh Sears, quanti danni hai fatto…). Questo è probabilmente il più grande luogo comune in circolazione. I carboidrati hanno una cattiva reputazione a causa del loro effetto sull’Insulina, ma anche le proteine stimolano la secrezione di Insulina. Anzi, possono essere uno stimolo per l’Insulina altrettanto maggiore di quello dei carboidrati. Uno studio ha confrontato gli effetti di due pasti diversi sull’Insulina. Un pasto conteneva 21g di proteine e 125g di carboidrati. L’altro pasto conteneva 75g di proteine e 75g di carboidrati. Entrambi i pasti contenevano 675 calorie. Ecco un grafico della risposta Insulinica:

Ecco un grafico della risposta glicemica:
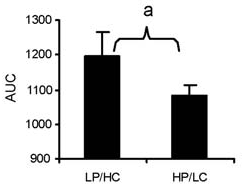
Si può notare che, nonostante la risposta glicemica fosse molto più alta nel pasto con più carboidrati, la risposta insulinica non era più alta. In realtà, la risposta insulinica era leggermente più alta dopo il pasto ad alto contenuto proteico, anche se non era statisticamente significativa.
Alcuni potrebbero obiettare che la condizione di “basso contenuto di carboidrati” non era veramente tale perché conteneva 75g di carboidrati. Ma non è questo il punto. Il punto è che la condizione ad alto contenuto di carboidrati aveva quasi il DOPPIO dei carboidrati, con una risposta di glucosio più elevata, ma la secrezione di Insulina era leggermente inferiore. Le proteine erano altrettanto potenti nello stimolare l’Insulina quanto i carboidrati.

Come potete notare nel grafico si osserva la tendenza a un picco di Insulina più rapido con la variabile ad alto contenuto proteico, con una risposta media di 45uU/mL a 20 minuti dal pasto, rispetto a circa 30uU/mL nella variabile ad alto contenuto di carboidrati.
Tornando al discorso accennato in precedenza, questa tendenza a una risposta insulinica più elevata era associata a una tendenza a una maggiore soppressione dell’appetito. I soggetti tendevano ad avere meno fame e più sazietà dopo il pasto ad alto contenuto proteico:

Ecco i risultati di un altro studio che ha confrontato gli effetti di 4 diversi tipi di proteine sulla risposta insulinica a un pasto. Questo studio è interessante perché sono stati preparati frullati con le diverse proteine (si, hanno usato anche frullati di tonno). I frullati contenevano solo 11g di carboidrati e 51g di proteine. Ecco la risposta insulinica ai diversi frullati:
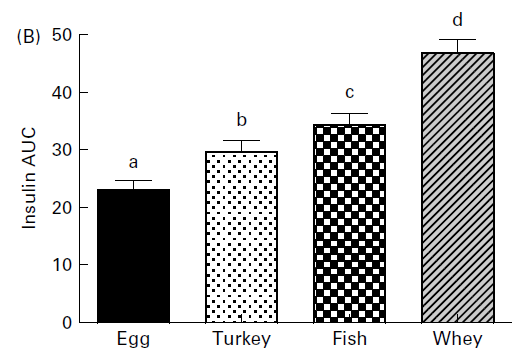
Si può notare che tutte queste proteine hanno prodotto una risposta insulinica, nonostante il fatto che i carboidrati nel frullato fossero bassi. La risposta insulinica è stata diversa anche tra le proteine, con il siero di latte che ha prodotto la risposta insulinica più elevata.
Ora, qualcuno potrebbe pensare che la risposta sia dovuta alla gluconeogenesi (un processo attraverso il quale il fegato converte le proteine in glucosio). L’idea è che le proteine vengano convertite in glucosio e che quindi aumentino i livelli di Insulina. Come ho già detto, si sostiene che questo comporta una risposta insulinica molto più lenta e prolungata, poiché il fegato impiega tempo a trasformare le proteine in glucosio. Tuttavia, non è così, perché la risposta insulinica è stata rapida, con un picco di 30 minuti e un rapido calo a 60 minuti:

Questa rapida risposta insulinica non era dovuta a variazioni della glicemia. Infatti, le proteine del siero del latte, che hanno provocato la maggiore risposta insulinica, hanno causato un calo della glicemia:
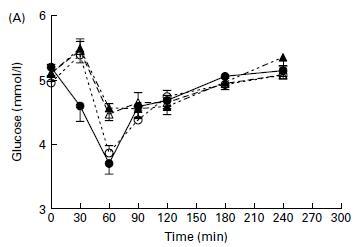
La risposta insulinica è stata associata alla soppressione dell’appetito. Infatti, le proteine del siero del latte, che avevano la risposta insulinica più alta, hanno causato la maggiore soppressione dell’appetito. Ecco un grafico che mostra l’apporto calorico dei soggetti quando hanno pranzato 4 ore dopo aver bevuto il frullato:
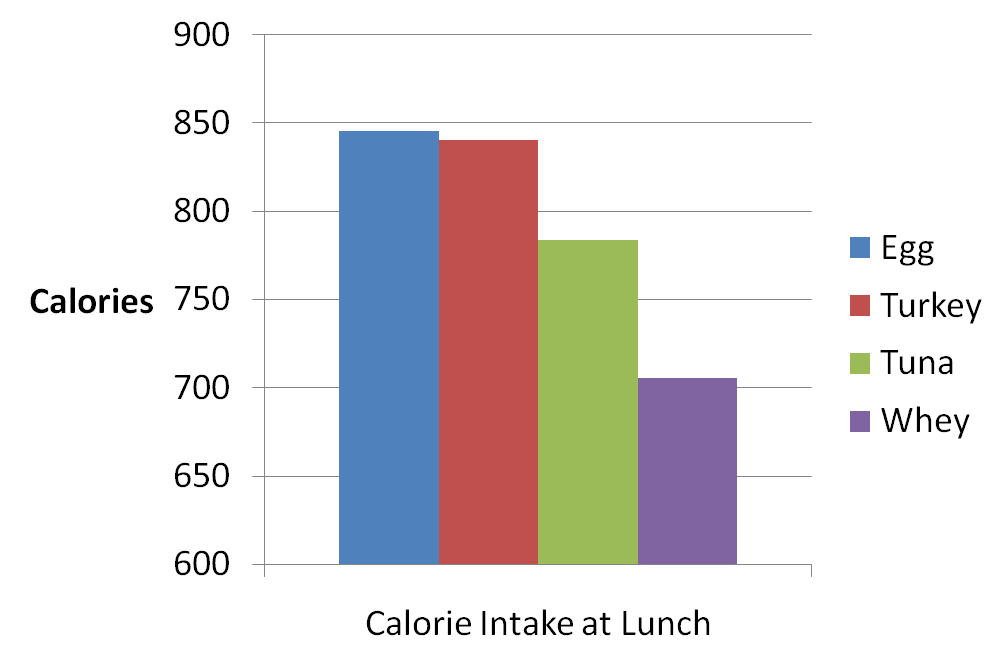
I soggetti hanno mangiato quasi 150 calorie in meno a pranzo quando hanno assunto proteine del siero di latte, che hanno anche provocato la maggiore risposta insulinica. In effetti, è stata riscontrata una fortissima correlazione inversa tra l’Insulina e l’assunzione di cibo (una correlazione di -0,93).
Ecco i dati di un altro studio che ha esaminato la risposta insulinica a un pasto che conteneva 485 calorie, 102g di proteine, 18g di carboidrati e quasi nessun grasso:
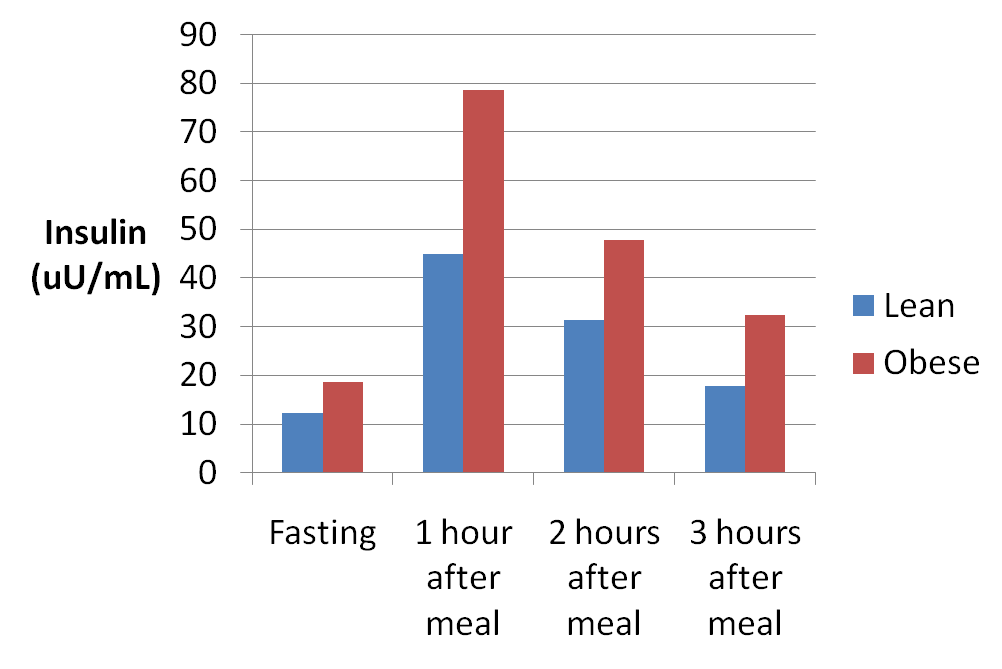
Si può notare che la risposta insulinica era esagerata nei soggetti obesi, probabilmente a causa della resistenza all’insulina. Ecco un grafico della risposta della glicemia ematica. Si può notare che non c’era alcuna relazione tra la risposta del glucosio e l’Insulina, come nello studio discusso in precedenza.

Il fatto è che le proteine sono un potente stimolatore della secrezione di Insulina, e questa secrezione di Insulina non è correlata a variazioni della glicemia o della gluconeogenesi da parte delle proteine. In effetti, uno studio ha rilevato che la carne di manzo stimola la secrezione di Insulina tanto quanto il riso integrale. La risposta glicemica di 38 alimenti diversi poteva spiegare solo il 23% della variabilità della secrezione insulinica in questo studio. Quindi, dietro la secrezione di Insulina c’è molto di più dei soli carboidrati.
Come possono quindi le proteine provocare un rapido aumento dell’Insulina, come dimostrato dallo studio sulle proteine del siero di latte? Gli aminoacidi (i mattoni delle proteine) possono stimolare direttamente il pancreas a produrre Insulina, senza doverla prima convertire in glucosio. Per esempio, l’aminoacido Leucina stimola direttamente le cellule del pancreas a produrre Insulina e c’è una relazione diretta dose-risposta (cioè, più Leucina c’è, più Insulina viene prodotta).
Prima ho affermato che l’Insulina sopprime la lipolisi. Ebbene, alcuni pensano che il Glucagone aumenti la lipolisi per annullare questo effetto.
L’idea che il Glucagone aumenti la lipolisi si basa su tre elementi: il fatto che il tessuto adiposo umano ha recettori per il Glucagone, il fatto che il Glucagone aumenta la lipolisi negli animali e il fatto che è stato dimostrato che il Glucagone aumenta la lipolisi nelle cellule adipose umane in vitro (in una coltura cellulare). Tuttavia, ciò che accade in vitro non è necessariamente ciò che accade in vivo (nel corpo). Si tratta di un caso in cui i dati più recenti hanno ribaltato il vecchio pensiero. Le ricerche condotte con tecniche moderne hanno dimostrato che il Glucagone non aumenta la lipolisi nell’uomo. Altre ricerche che hanno utilizzato le stesse tecniche hanno mostrato risultati simili.
Va ricordato perché il Glucagone viene rilasciato in risposta alle proteine. Poiché le proteine stimolano la secrezione di Insulina, se non si consumano carboidrati con le proteine, esse causano un rapido calo della glicemia. Il Glucagone impedisce questo rapido calo di zuccheri nel sangue stimolando il fegato a produrre glucosio.
Adesso sappiamo che le proteine alimentari possono causare picchi di Insulina proprio come i carboidrati alimentari, e questi picchi non sono legati alla gluconeogenesi delle proteine (cioè alla loro conversione in zucchero). Sappiamo anche che questi picchi sono in parte responsabili della soppressione dell’appetito causata dalle proteine alimentari (grazie agli effetti dell’Insulina sul cervello che inibiscono l’appetito).
- Picchi insulinici e aumento del peso
Vorrei approfondire un altro luogo comune riguardante l’Insulina e che interessa i rapidi picchi dell’ormone. Essi sono importanti nella regolazione della glicemia. E’ necessario quindi discutere le fasi della secrezione di Insulina. La secrezione di Insulina da parte del pancreas avviene in due fasi. La prima fase avviene molto rapidamente: il pancreas percepisce l’aumento del glucosio e l’Insulina viene rilasciata entro 1-2 minuti dall’aumento della glicemia. Questa risposta in fase rapida è il risultato del rilascio da parte del pancreas dell’Insulina immagazzinata. In genere si conclude entro 10 minuti. È stato riscontrato che questa risposta di fase rapida è compromessa nelle persone con alterata tolleranza al glucosio (persone che hanno risposte glicemiche ai pasti più elevate del normale e livelli di zucchero nel sangue a digiuno più elevati, ma che non sono diabetiche). Questa risposta in fase rapida è completamente assente nelle persone affette da diabete di tipo II.
Esiste una seconda fase che continua finché il glucosio è elevato. Questo rilascio di Insulina avviene attraverso la liberazione dell’Insulina immagazzinata e la creazione di nuova Insulina (l’Insulina viene creata da un precursore chiamato proinsulina, come abbiamo visto nella prima parte). Quando si infonde glucosio nel sangue di persone sane e di diabetici di tipo II, si ottengono risposte insuliniche di questo tipo:

Si può notare che i diabetici mancano completamente della risposta di fase rapida che è presente negli individui sani.
Esiste un farmaco chiamato Exenatide (Byetta), che si è rivelato in grado di ripristinare questa risposta insulinica di fase rapida nei diabetici:

Il ripristino della risposta insulinica in fase rapida migliora la regolazione della glicemia nei diabetici:
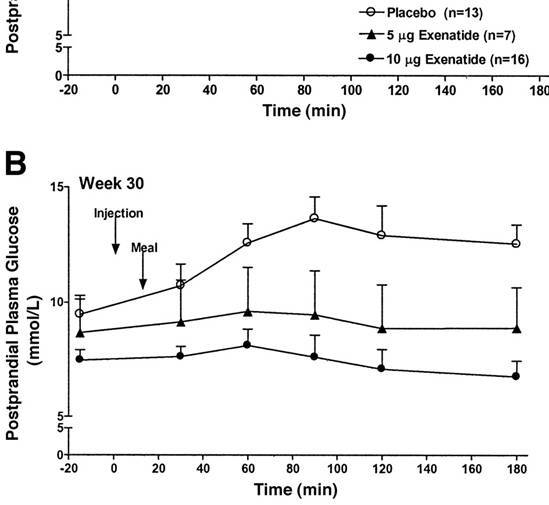
Nel grafico sopra riportato si può notare che la glicemia è rimasta costante in risposta a un pasto nei soggetti che assumevano l’Exenatide, mentre è aumentata nel tempo nei soggetti che assumevano il placebo.
A molti piace attribuire la colpa dell’obesità e dell’aumento di peso all’Insulina, ma l’Exenatide, che ripristina i picchi di Insulina nei diabetici di tipo II, fa perdere peso:

Parte di questa perdita di peso è dovuta a un miglioramento del senso di sazietà. L’Exenatide è un farmaco che imita gli effetti di un ormone chiamato peptide glucagone-simile-1 (GLP-1). Il GLP-1 è un ormone che stimola l’Insulina a livello intestinale (noto come Incretina). Il GLP-1 potenzia la secrezione di Insulina, aumenta la sintesi di Insulina, aumenta l’espressione genica dell’Insulina e inibisce la secrezione di Glucagone (l’ormone antagonista dell’Insulina). Eppure l’Exenatide, che imita il GLP-1 e contribuisce a stimolare la secrezione di Insulina, fa perdere peso.
Il fatto è che i rapidi picchi di Insulina di per sé non sono un male. Le proteine causano rapidi picchi di Insulina, ma le proteine riducono l’appetito e aiutano a perdere peso. Il GLP-1 e i farmaci come l’Exenatide contribuiscono ai picchi di Insulina, ma riducono l’appetito e fanno perdere peso. Il problema è che le persone confondono i picchi di Insulina con i picchi di glucosio nel sangue. È ormai assodato che un rapido aumento e una rapida diminuzione del glucosio nel sangue possono contribuire alla fame. Poiché i rapidi aumenti della glicemia causano anche rapidi aumenti dell’Insulina, le persone finiscono per incolpare l’Insulina (e gli effetti dei carboidrati ad alto indice glicemico sull’Insulina) del problema.
- Differenza del possibile impatto tra somministrazione esogena e secrezione endogena di Insulina sul peso corporeo
Un altro luogo comune sull’Insulina correla l’aumento di peso dei soggetti diabetici trattati con tale ormone agli aumenti di peso dei soggetti sani. Evidentemente queste persone non conoscono l’Amilina.

L’Amilina è un ormone che viene secreto dal pancreas contemporaneamente all’Insulina. L’Amilina riduce l’appetito e stimola la lipolisi (la scomposizione dei Trigliceridi in acidi grassi liberi).
I diabetici di tipo I non producono Amilina e nei diabetici di tipo II la secrezione di Amilina è compromessa. È stato riscontrato che la Pramlintide, un farmaco che imita gli effetti dell’Amilina, produce una perdita di peso nei diabetici.
Queste informazioni dimostrano che gli effetti dell’iniezione di Insulina in un diabetico non possono essere paragonati agli effetti delle variazioni fisiologiche dell’Insulina in un non diabetico, eppure molte persone fanno erroneamente questo confronto come se fossero simili.
- Prodotti lattiero-caseari e secrezione insulinica
Una delle premesse che alcune persone fanno è che i carboidrati stimolino l’accumulo di grasso stimolando la secrezione di Insulina. Ma abbiamo già visto come questa premessa sia errata. In particolare, abbiamo visto come anche le proteine stimolino la secrezione di Insulina (a volte tanto quanto i carboidrati), ma non favoriscano l’aumento di peso o di grasso. Vi ho anche mostrato come il farmaco Exenatide ripristini la secrezione di Insulina in fase rapida nei diabetici, pur favorendo la perdita di peso.
Se l’ipotesi carboidrati/insulina fosse vera, dovremmo prevedere che gli alimenti estremamente insulinemici favoriscano in modo esclusivo l’aumento di peso. Molti non si rendono conto che i latticini sono tra gli alimenti più insulinemici in circolazione. Infatti, creano risposte insulinemiche molto più elevate di quanto ci si aspetterebbe in base al loro contenuto di carboidrati. Non solo, ma il lattosio, il carboidrato principale dei latticini, è in realtà a basso indice glicemico e produce un lento aumento della glicemia (il lattosio ha un indice glicemico di 46 rispetto al pane bianco che è di 100, per quello che vale). In effetti, l’indice glicemico di molti prodotti lattiero-caseari è piuttosto basso, con il latte intero a 39, il latte scremato a 37, il gelato a 51 e lo yogurt alla frutta a 41.
Nonostante le risposte glicemiche basse, i latticini creano risposte insuliniche molto elevate. Per esempio, in uno studio, i latticini hanno creato risposte insuliniche simili o superiori a quelle del pane bianco, nonostante la risposta glicemica per alcuni dei latticini fosse del 60% inferiore a quella del pane bianco. In questo studio, i ricercatori hanno confrontato le risposte glicemiche e insulinemiche tra pane bianco, una miscela a basso contenuto di glutine/lattosio, una miscela ad alto contenuto di glutine/lattosio, merluzzo con aggiunta di lattosio, latte, proteine del siero del latte con aggiunta di lattosio e formaggio con aggiunta di lattosio. Tutte le variabili contenevano 25g di carboidrati e 18,2g di proteine, tranne il pane bianco e le miscele a basso contenuto di glutine/lattosio, che contenevano 25g di carboidrati e 2,8g di proteine. Pertanto, il lattosio era il carboidrato in tutte le condizioni, ad eccezione del pane bianco.
Osservando l’area dell’Insulina sotto la curva (AUC) per le varie condizioni, si può notare che i prodotti lattiero-caseari hanno effettivamente creato risposte insuliniche maggiori rispetto al pane bianco, pur avendo quantità simili di carboidrati:
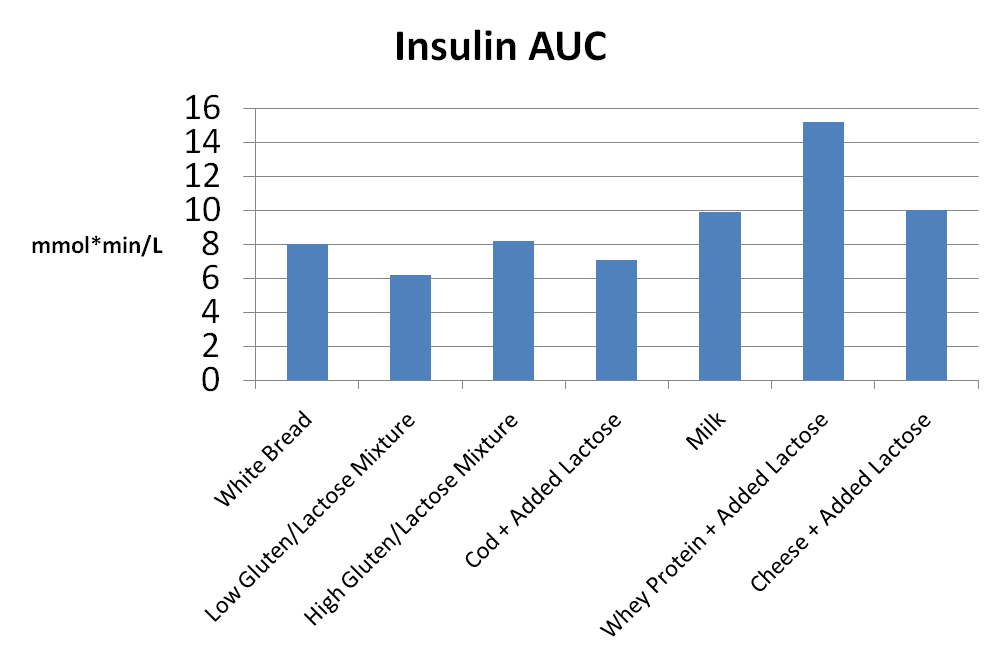
È evidente che non è il lattosio il responsabile della maggiore risposta insulinica, perché le miscele glutine/lattosio e merluzzo/lattosio hanno dato risposte insuliniche simili o inferiori a quelle del pane bianco.
Anche la risposta glicemica non è responsabile della maggiore risposta insulinica. Infatti, la risposta glicemica era più bassa in tutte le condizioni rispetto al pane bianco, con il latte che creava la risposta glicemica più bassa ma la terza risposta insulinica più alta:

L’indice insulinogenico, che mette in relazione la quantità di secrezione di Insulina con la risposta del glucosio nel sangue, era significativamente più alto nei prodotti lattiero-caseari, indicando che i prodotti lattiero-caseari stimolavano una secrezione di Insulina molto maggiore di quella che ci si aspetterebbe in base alla risposta del glucosio nel sangue:

Questo non è l’unico studio che mostra gli effetti insulinemici dei latticini. In precedenza si è visto come le proteine del siero di latte, una proteina casearia, creino la risposta insulinica più elevata rispetto alle proteine non casearie. In uno studio condotto su diabetici di tipo II, l’inclusione di proteine del siero di latte in un pasto ha aumentato la risposta insulinica del 31-57%, mentre la risposta glicemica si è ridotta fino al 21%. In un altro studio, l’aggiunta di 400ml di latte a un pasto a base di pane ha aumentato la risposta insulinica del 65%, nonostante non vi sia stata alcuna variazione nella risposta glicemica. Nello stesso studio, l’aggiunta di 200 o 400ml di latte a un pasto a base di spaghetti ha aumentato la risposta insulinica del 300%; anche in questo caso, la risposta glicemica non ha subito variazioni. In effetti, bere latte con il pasto di spaghetti ha creato una risposta insulinica simile a quella del pane bianco.
Ecco i risultati di un altro studio che mostra gli indici glicemici e insulinemici del latte rispetto al pane bianco:

È chiaro che i prodotti lattiero-caseari stimolano la secrezione di grandi quantità di Insulina, quanto o più del pane bianco. Uno dei motivi per cui i latticini creano grandi risposte insuliniche è dovuto al loro contenuto di aminoacidi. Infatti, la risposta insulinica postprandiale dei latticini è correlata all’aumento degli aminoacidi a catena ramificata leucina, valina e isoleucina. Ho già sottolineato come la leucina stimoli direttamente il pancreas a produrre Insulina.
Un altro motivo per cui i latticini stimolano la secrezione di Insulina è il loro effetto su un ormone chiamato polipeptide insulinotropico glucosio-dipendente (GIP). Come il GLP-1, di cui ho scritto precedentemente, il GIP è un’incretina. Ciò significa che è un ormone prodotto dall’intestino che stimola la secrezione di Insulina. I latticini stimolano una maggiore produzione di GIP. Nello studio di cui ho parlato in precedenza, che ha messo a confronto il siero di latte, il latte e il formaggio con il pane bianco, il siero di latte e il formaggio hanno prodotto risposte alla GIP superiori del 21-67% rispetto al pane bianco:
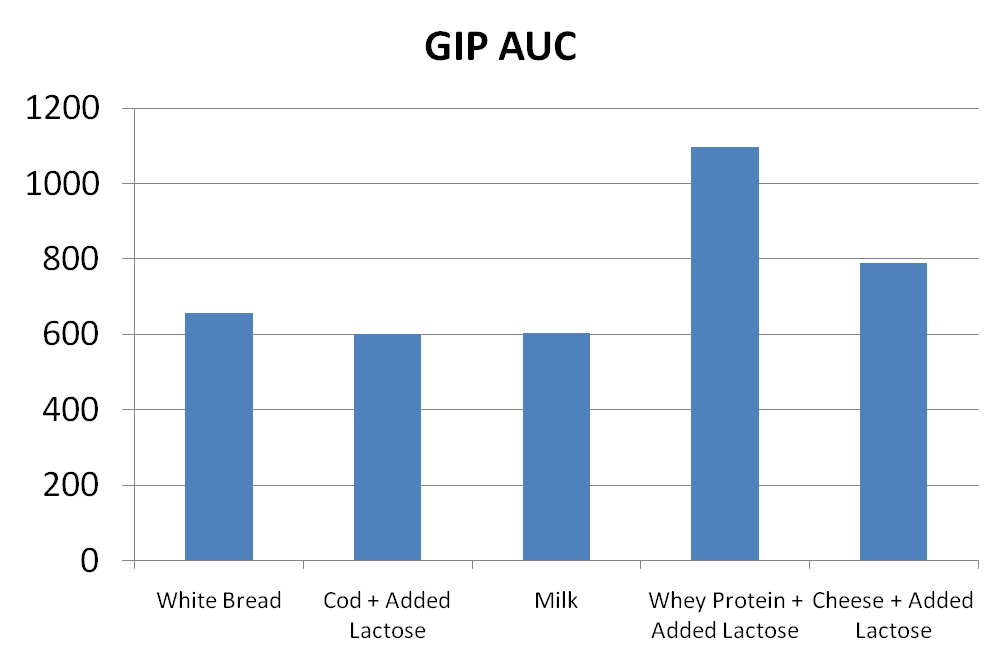
I dati sopra riportati illustrano uno dei problemi dell’ipotesi carboidrati/insulina… essa presuppone che i carboidrati siano lo stimolo principale della secrezione insulinica. Tuttavia, è chiaro che anche gli aminoacidi e le incretine svolgono un ruolo significativo nella secrezione di Insulina. E come ho sottolineato, la risposta glicemica di un alimento spiega solo il 23% della variazione della risposta insulinica. Pertanto, la secrezione di Insulina è molto più importante della risposta glicemica dovuta al consumo di carboidrati.
È quindi chiaro che i latticini sono estremamente insulinemici, più di molti altri alimenti ad alto contenuto di carboidrati. Pertanto, se l’ipotesi carboidrati/insulina fosse vera, si potrebbe prevedere che una dieta ricca di latticini dovrebbe favorire l’aumento di peso e di grasso. Tuttavia, gli studi non dimostrano alcuna relazione tra l’assunzione di latticini e l’aumento di peso. Per esempio, non c’è alcuna relazione tra l’assunzione di latticini e il BMI nelle donne giapponesi. Negli uomini statunitensi, non c’è alcuna relazione tra l’aumento del consumo di latticini e l’aumento di peso a lungo termine. Nelle donne in perimenopausa, un’elevata assunzione di latticini è in realtà inversamente associata all’aumento di peso (cioè, una maggiore assunzione di latticini è associata a un minore aumento di peso).
Sebbene si tratti di studi osservazionali, i risultati di studi controllati su animali ed esseri umani sono simili. In effetti, gli studi sugli animali mostrano un minore aumento di peso quando vengono nutriti con prodotti caseari. Nei topi, l’integrazione di yogurt determina un minore aumento di peso e di grasso rispetto ai controlli che seguono una dieta isocalorica. In un altro studio, i topi transgenici hanno perso peso con una dieta ipocalorica. I topi sono stati poi lasciati mangiare ad libitum (cioè quanto volevano). I topi alimentati con prodotti caseari hanno riacquistato meno grasso e peso durante la rialimentazione. In un terzo studio, l’assunzione di prodotti lattiero-caseari, ma non di un integratore di calcio, ha ridotto l’aumento di peso e il grasso corporeo nei topi alimentati con una dieta ad alto contenuto di grassi. In un quarto studio, le proteine dei latticini hanno attenuato l’aumento di grasso nei roditori alimentati con una dieta ad alto contenuto di grassi e zuccheri. In un quinto studio, una dieta a base di latticini ha attenuato l’aumento di peso settimanale nei ratti Sprague-Dawley.
Naturalmente, si tratta di studi sugli animali. E per gli esseri umani? In uno studio, i latticini a basso contenuto di grassi non hanno favorito l’aumento di peso, mentre quelli ad alto contenuto di grassi sì. È possibile che l’aumento di peso in questo studio sia stato causato semplicemente dall’eccesso di calorie e non dall’Insulina? In un altro studio, l’aumento dell’assunzione di latticini non ha influito sulla composizione corporea. In un terzo studio, l’aumento dell’assunzione di latticini non ha compromesso la perdita di peso. In uno studio di un anno, l’aumento dell’assunzione di latticini non ha influito sulle variazioni della massa grassa. In un follow-up di 6 mesi, un’elevata assunzione di latticini ha predetto livelli inferiori di massa grassa. In uno studio di 9 mesi, l’aumento dell’assunzione di latticini non ha influito sul mantenimento del peso, ma il gruppo ad alto contenuto di latticini ha evidenziato una maggiore ossidazione dei grassi.
Ora dovrebbe essere più che chiaro il fatto che le prove sono schiaccianti sulla questione che i prodotti lattiero-caseari non favoriscono l’aumento di peso e anzi lo inibiscono per via dell’effetto saziante. Questo nonostante il fatto che i latticini producano una risposta insulinica molto ampia, pari o superiore a quella di molti alimenti ad alto contenuto di carboidrati. Pertanto risulta chiaro che l’ipotesi carboidrati/insulina è errata.
Per concludere la serie di luoghi comuni sull’Insulina vi citerò quello che desterà maggiore incredulità…
Molti pensano che le cellule abbiano bisogno di Insulina per utilizzare il glucosio nel circolo ematico. Una delle prove a sostegno di questa tesi è rappresentata dal soggetto diabetico di tipo I. Quando un diabetico di tipo I non ha Insulina, la glicemia sale alle stelle. Questo perché, a quanto pare, il glucosio non riesce a entrare nelle cellule.
Tuttavia, lo scenario sopra descritto non è quello che si verifica in un diabetico di tipo I a cui è stata tolta l’Insulina. Il glucosio può entrare nelle cellule senza problemi. In realtà sta succedendo qualcos’altro. Un articolo pubblicato sul Journal of Anasthesia descrive in modo esauriente come l’Insulina sia stata fraintesa nel suo ruolo di regolazione della glicemia ematica.
Nel 1916, Sir Edward Schafer, professore di fisiologia del quale ho già parlato nella prima parte, pubblicò un libro intitolato “The Endocrine Organs”. In questo libro ipotizzò l’esistenza di quella che oggi chiamiamo Insulina:
I risultati dell’asportazione del pancreas e dell’innesto del pancreas si spiegano meglio ipotizzando che il tessuto delle isole produca un Autacoide che passa nel flusso sanguigno e agisce sul metabolismo dei carboidrati e sull’immagazzinamento dei carboidrati in modo tale da evitare un indebito accumulo di glucosio nel sangue. In via provvisoria sarà opportuno riferirsi a questa ipotetica sostanza come Insulina.
L’insulina sarebbe stata scoperta 5 anni dopo. Schafer ipotizzò anche che l’Insulina fosse creata da un precursore inattivo:
Va tuttavia precisato che non è ancora stato determinato se la sostanza attiva sia prodotta come tale nel pancreas o se esista come pro-insulina che viene convertita altrove in un autacoide attivo.
La pro-insulina fu scoperta quasi 50 anni dopo. Schafer era davvero un uomo in anticipo sui tempi.
Schafer evitava di usare il termine “ormone” per descrivere l’Insulina. Utilizzò invece i termini “autacoide” e “chalone”. Un autacoide è una sostanza con azione eccitatoria, cioè stimola l’azione del corpo. Un autacoide può essere considerato simile al pedale dell’acceleratore dell’auto; si preme il pedale e si stimola l’auto ad andare più veloce. Il chalone è una sostanza ad azione inibitoria, che rallenta le cose nel corpo. Il chalone può essere considerato simile al freno dell’auto. Schafer ipotizzò correttamente che l’Insulina agisse sia come autacoide che come chalone nell’organismo. Egli riteneva inoltre che l’Insulina agisse come chalone molto più che come autacoide nell’organismo. In altre parole, riteneva che le funzioni inibitorie dell’Insulina fossero molto più importanti di quelle eccitatorie o stimolatorie. Molti anni dopo si sarebbe dimostrato corretto.
Tuttavia, prima che a Schafer venisse data ragione, si verificò l'”età nera dell’endocrinologia”. Si tratta del periodo di tempo compreso tra il 1950 e il 1980, in cui gli scienziati estrapolavano conclusione che andavano ben oltre le loro effettive scoperte. Prendevano i dati di studi su animali o in vitro (ricerche condotte in provetta o in coltura) e poi ipotizzavano che la stessa cosa avvenisse nell’uomo in vivo (all’interno del corpo). Gli scritti come “Good Calories, Bad Calories” di Gary Taubes si basano pesantemente sulla ricerca di questo periodo, nonostante il fatto che gran parte di ciò che si pensava all’epoca sia stato ribaltato da ricerche migliori, o almeno modificato in modo significativo.

L’età nera dell’endocrinologia è quella che ha portato alla convinzione, oggi errata, che l’Insulina sia necessaria alle cellule per assorbire il glucosio. Gli esperimenti condotti negli anni Cinquanta dimostrarono che l’Insulina era in grado di stimolare l’assorbimento del glucosio da parte di campioni di muscolo e di grasso di ratto. Questi dati sono stati trasposti all’uomo e si è ipotizzato erroneamente che la mancanza di Insulina impedisca al glucosio di entrare nelle cellule e che quindi la glicemia salga a livelli pericolosi. Questo pensiero errato è stato insegnato nei libri di testo e nei corsi universitari di tutto il mondo per molti anni, dando vita a un vero e proprio dogma. Purtroppo è molto difficile superare una convinzione fortemente radicata, anche se negli anni ’70 è stato dimostrato che questo concetto di Insulina è sbagliato, continua a essere insegnato ancora oggi.
L’ipotesi errata secondo la quale la sospensione dell’Insulina provochi un’elevata glicemia perché “il glucosio non riesce a entrare nelle cellule” si basava sul presupposto che l’Insulina sia necessaria per l’assorbimento del glucosio da parte delle cellule, piuttosto che l’Insulina si limiti a migliorare l’assorbimento del glucosio. Quello che gli scienziati degli anni ’50 non hanno notato è che i tessuti possono assumere notevoli quantità di glucosio anche in assenza di Insulina.
Il glucosio entra nelle cellule attraverso una famiglia di trasportatori. Un trasportatore primario nelle cellule muscolari e adipose lo conosciamo più o meno tutti, si tratta del GLUT-4. L’Insulina stimola il GLUT-4 a spostarsi dall’interno della cellula alla superficie cellulare, dove il glucosio può legarsi al trasportatore GLUT-4 ed entrare nella cellula. Tuttavia, sulla superficie cellulare sono presenti numerosi trasportatori di glucosio, anche in assenza di Insulina. In effetti, ci sono abbastanza trasportatori sulla superficie cellulare per consentire alla cellula di ottenere abbastanza glucosio per sostenere il suo fabbisogno energetico. Pertanto, il trasporto di glucosio nelle cellule non è mai veramente dipendente dall’Insulina. L’Insulina favorisce l’assorbimento del glucosio nelle cellule, ma non è necessaria. Infatti, quando si elimina il Recettore dell’Insulina nei topi in modo che l’Insulina non possa stimolare l’assorbimento del glucosio nelle cellule muscolari o adipose (pur mantenendo intatto il Recettore dell’Insulina in altre cellule come il cervello e il fegato), gli animali non diventano diabetici e presentavano valori della glicemia ematica normali.
Gli studi sui traccianti metabolici ci hanno permesso di capire come funziona l’Insulina nell’uomo in vivo. Quando si toglie l’Insulina a un diabetico di tipo I, il glucosio nel sangue sale bruscamente. Tuttavia, non è perché il glucosio non riesce a entrare nelle cellule. In realtà, l’assorbimento del glucosio nelle cellule aumenta. Questo perché la concentrazione di glucosio nel sangue è talmente superiore a quella cellulare che il glucosio deve spostarsi all’interno delle cellule (ricordate che sulla superficie delle cellule ci sono già abbastanza trasportatori di glucosio anche in assenza di Insulina). Allora perché il glucosio nel sangue sale così tanto? Ricordiamo che la quantità di glucosio nel sangue è in funzione sia della quantità di glucosio che entra nel sangue (velocità di comparsa), sia della quantità di glucosio che esce dal sangue (velocità di scomparsa). In un diabetico a digiuno e senza Insulina, tutto il glucosio proviene dal fegato. Ricordiamo che il fegato contribuisce a mantenere i livelli di zucchero nel sangue a digiuno rilasciando glucosio; questo glucosio proviene sia dalla gluconeogenesi (la formazione di glucosio da fonti non glucidiche, come le proteine) sia dalla glicogenolisi (la degradazione del glicogeno immagazzinato nel fegato). L’Insulina agisce come un freno (un chalone, come lo ha definito il dottor Schafer) su questi processi. Pertanto, in assenza di Insulina, si verificano fenomeni di gluconeogenesi e glicogenolisi incontrollati. La glicemia elevata in un diabetico non controllato è quindi causata da una sovrapproduzione di glucosio da parte del fegato, non perché il glucosio non riesca a entrare nelle cellule.
Infatti, poiché l’Insulina non è presente, molti processi si attuano a ritmi elevati, completamente sregolati. L’Insulina normalmente inibisce la produzione di chetoni da parte del fegato; senza l’Insulina che rallenta la produzione di chetoni, questi ultimi vengono prodotti a ritmi elevati, dando luogo alla chetoacidosi diabetica. Ecco perché l’iperglicemia e la chetoacidosi si verificano contemporaneamente. Senza Insulina, si ha anche un’accelerazione della proteolisi (la scomposizione delle proteine) e della lipolisi (la scomposizione dei grassi). Gli aminoacidi elevati nel sangue forniscono ulteriore substrato al fegato per continuare a produrre grandi quantità di glucosio. Gli acidi grassi elevati forniscono al fegato il substrato per continuare a produrre grandi quantità di chetoni.
L’Insulina è quindi come un vigile urbano o un semaforo a un incrocio. Aiuta a rallentare e a controllare il traffico. Senza un semaforo o un vigile urbano, le auto attraversano l’incrocio senza controllo e si verificano incidenti stradali. Allo stesso modo, senza Insulina nell’organismo, la gluconeogenesi, la glicolisi, la proteolisi, la chetogenesi e la lipolisi procedono a ritmi elevati senza che nulla possa fermarle. Il risultato finale è l’iperglicemia, la chetoacidosi e infine la morte.
Quando si inietta l’Insulina in un diabetico non controllato, si frenano tutti i processi menzionati in precedenza. Si inibisce la produzione di glucosio da parte del fegato e la glicemia si abbassa. Poiché non c’è più iperglicemia, l’assorbimento di glucosio nelle cellule diminuisce. La lipolisi viene inibita, quindi la concentrazione di acidi grassi liberi scende quasi a zero. Poiché non ci sono più acidi grassi liberi per la produzione di chetoni, la produzione di chetoni rallenta. Anche la proteolisi viene inibita.
Gli studi sui traccianti metabolici hanno dimostrato ciò che Schafer aveva ipotizzato più di un secolo fa… che il ruolo principale dell’Insulina nell’organismo è inibitorio piuttosto che eccitatorio. Sebbene l’Insulina abbia certamente funzioni eccitatorie, non è principalmente un “ormone di stoccaggio” come molti sostengono. L’Insulina non è necessaria alle cellule per assorbire e immagazzinare il glucosio. Certamente ne favorisce l’assorbimento, ma c’è una grande differenza tra il favorire l’assorbimento e l’essere necessaria per l’assorbimento.
Naturalmente, questa ricerca ci dice solo cosa succede quando l’Insulina è presente rispetto a quando non è presente. Che dire della situazione normale di una persona sana, che ingerisce un pasto e vede un aumento del glucosio nel sangue? Cosa succede per riportare il glucosio alla normalità? E cosa succede in una persona diabetica di tipo II in questa situazione?
Un classico studio sui traccianti metabolici ha seguito cosa succede al glucosio quando viene assunto per via orale. In questo studio, ai diabetici di tipo II e ai soggetti sani di controllo è stato somministrato 1g di glucosio per chilogrammo di peso corporeo (quasi mezzo grammo per libbra). Utilizzando dei traccianti metabolici, i ricercatori hanno determinato non solo dove andava il glucosio, ma anche cosa succedeva alla produzione di glucosio da parte del fegato. I ricercatori hanno anche misurato i livelli di Insulina nel sangue.
Come prevedibile, il glucosio orale ha provocato un aumento del glucosio nel sangue e un corrispondente aumento dell’Insulina. Nelle persone sane, la produzione di glucosio da parte del fegato è stata drasticamente soppressa dall’aumento dell’Insulina. Infatti, la produzione di glucosio è diminuita del 70-80% a 75-105 minuti dall’ingestione del glucosio. Dopo 3,5 ore, la produzione di glucosio era ancora soppressa del 50%. Pertanto, uno dei modi in cui l’Insulina aiuta a controllare la glicemia dopo un pasto è quello di comunicare al fegato di smettere di produrre glucosio. Questo ha senso: non si vuole che il fegato produca glucosio quando il glucosio entra nel flusso sanguigno dall’apparato digerente.
Anche la produzione epatica di glucosio è stata soppressa nei diabetici di tipo II. Tuttavia, questa soppressione è stata compromessa. Tuttavia, questa soppressione era compromessa nei diabetici di circa il 40%. Si tratta di un caso di resistenza all’Insulina nel fegato dei diabetici; il fegato non risponde all’Insulina come dovrebbe (ricordiamo che l’Insulina sopprime la produzione epatica di glucosio) e quindi produce troppo glucosio. Nel documento gli autori affermano che:
…si può concludere che la sovrapproduzione di glucosio è un importante fattore determinante dell’iperglicemia diabetica, sia nello stato postassorbitivo che in quello postprandiale.
La produzione di glucosio da parte del fegato ci racconta solo metà della storia. Se da un lato l’Insulina inibisce la produzione di glucosio da parte del fegato, dall’altro aumenta la capacità dei tessuti di prelevare il glucosio dal sangue (ricordate che la migliora). Le cellule assorbono il glucosio in due modi… attraverso l’azione di massa del glucosio (cioè il gradiente di concentrazione, in cui la concentrazione di glucosio nel sangue è talmente superiore a quella delle cellule che il glucosio si sposta all’interno delle cellule) e attraverso la stimolazione dell’Insulina. In questo studio, l’assorbimento del glucosio nelle cellule era compromesso nei diabetici. Poiché il movimento del glucosio nelle cellule attraverso l’azione di massa è simile tra i diabetici e i soggetti sani, l’assorbimento ridotto del glucosio nei diabetici era dovuto all’insulino-resistenza nelle cellule. L’assorbimento del glucosio da parte dei tessuti era compromesso di circa il 27% nei diabetici.
Da questa ricerca emerge chiaramente che la risposta glicemica elevata di un diabetico di tipo II è dovuta sia a un’alterata risposta del fegato all’Insulina (per cui la produzione di glucosio è superiore a quella che dovrebbe essere), sia a un’alterata risposta delle cellule ad assorbire il glucosio dal sangue. Tuttavia, se si considerano le percentuali, la risposta alterata del fegato è maggiore di quella delle cellule. Un’altra ricerca pubblicata nello stesso anno ha mostrato una pari resistenza all’Insulina nel fegato e in altri tessuti, sebbene questa ricerca sia stata condotta con soggetti a digiuno. In quello studio, così come in quello di cui abbiamo parlato, è stata riscontrata una correlazione molto forte tra l’iperglicemia a digiuno e la produzione epatica di glucosio; ciò indica che, a digiuno, è la sovrapproduzione di glucosio da parte del fegato il fattore più importante nel causare l’iperglicemia in un diabetico. Da questa ricerca si evince anche che l’assorbimento di glucosio a digiuno è in realtà aumentato, non diminuito, nei diabetici di tipo II (proprio come nei diabetici di tipo I non controllati). Pertanto, l’iperglicemia a digiuno dei diabetici di tipo II e dei diabetici di tipo I non controllati è dovuta a una sovrapproduzione di glucosio da parte del fegato, non perché “il glucosio non riesce a entrare nelle cellule”. In un diabetico di tipo II, in risposta a un pasto, l’assorbimento del glucosio nelle cellule è compromesso, ma la resistenza all’Insulina nel fegato svolge comunque un ruolo importante.
Ciò che risulta chiaro da tutte queste ricerche è che le principali funzioni dell’Insulina nell’organismo sono inibitorie, agendo da freno su molti processi corporei. Sebbene l’Insulina stimoli l’immagazzinamento del glucosio e di altri nutrienti, questa funzione non è altrettanto importante di quella inibitoria. Pertanto, l’Insulina dovrebbe essere considerata più un vigile urbano che un ormone di stoccaggio.
Siete sconvolti ma consapevoli, oppure continuerete a vagare nel relativismo?
La conclusione è che l’Insulina non è il male assoluto, anzi, e le leggende e luoghi comuni che le ruotano intorno nel Fitness e BodyBuilding sono in definitiva sbagliati!
Per riassumere i punti chiave volti a demistificare i luoghi comuni sull’Insulina:
- L’Insulina sopprime l’appetito, non lo aumenta.
- Una dieta ad alto contenuto di carboidrati non causa livelli di Insulina cronicamente elevati.
- Le proteine sono insulinemiche e, in alcuni casi, possono essere insulinemiche quanto i carboidrati.
- Contrariamente a quanto si crede, il Glucagone non “annulla” la soppressione della lipolisi da parte dell’Insulina quando si ingeriscono proteine.
- Gli effetti insulinemici delle proteine sono dovuti a un effetto stimolante diretto sul pancreas e non alla conversione delle proteine in glucosio.
- La combinazione di proteine e carboidrati può produrre una maggiore secrezione di Insulina rispetto all’uno o all’altro da solo, eppure le diete ad alto contenuto di proteine e moderato-alto contenuto di carboidrati sono molto efficaci per la perdita di peso.
- È stato dimostrato che le diete ad alto contenuto di carboidrati producono una perdita di peso quando le persone sono in deficit energetico.
- I latticini sono estremamente insulinemici, tanto quanto il pane bianco, eppure non favoriscono l’aumento di peso in assenza di un surplus energetico. Questo dato è supportato da un numero molto elevato di studi, tra cui studi su animali, studi osservazionali e studi controllati randomizzati.
- L’Insulina non è necessaria per l’accumulo di grasso
- I livelli di Insulina non sono predittivi di aumento o perdita di peso nella maggior parte degli studi prospettici.
- L’Exenatide ripristina il rilascio di Insulina in fase rapida nei diabetici, ma provoca una perdita di peso
- Gli effetti dell’iniezione di Insulina non possono essere paragonati al normale rilascio fisiologico di Insulina, poiché l’Amilina è co-secreta con l’Insulina dal pancreas
- L’Insulina funziona principalmente come ormone inibitorio piuttosto che come ormone di accumulo, agendo come freno su molti importanti processi fisiologici
- Un diabetico di tipo I senza Insulina diventa iperglicemico a causa della sovrapproduzione di glucosio da parte del fegato, non perché il glucosio non riesca a entrare nelle cellule.
- L’Insulina favorisce l’assorbimento del glucosio nelle cellule, ma non è necessaria per questo.
- L’Insulina regola la glicemia dopo un pasto sia impedendo al fegato di produrre glucosio, sia favorendo l’assorbimento del glucosio nelle cellule.
- A digiuno, l’Insulina regola la glicemia controllando la produzione di glucosio da parte del fegato e non influenzando l’assorbimento del glucosio nelle cellule.
- Non ci si può limitare a considerare gli effetti temporanei dell’Insulina sulla lipolisi e sull’accumulo di glucosio. Bisogna considerare ciò che accade nell’arco delle 24 ore; il grasso corporeo non aumenta se non c’è un surplus energetico complessivo.
Tutto chiaro ora? Ecco, bravi, adesso però smettete di fare gli ortoressici isulinofobici!
Continua…
Gabriel Bellizzi [CEO BioGenTech]
Riferimenti:
- Gli studi utilizzati per realizzare questo articolo provengono dalla serie di articoli scritti e pubblicati da James Krieger sul suo sito weightology.net e intitolati “INSULIN: AN UNDESERVED BAD REPUTATION”.
