Introduzione:
Detesto parlare di argomenti già largamente dibattuti in altra sede, ma in questo caso, parlare in modo dettagliato di proteine vegetali e tasso di sintesi proteica correlato mi è sembrato in un certo senso doveroso. D’altra parte, non tollero gli slogan universalistici dei “nazivegani” e nemmeno quelli dei “paleonazi”. Indi per cui, eccomi qui, ad usare una recentissima e ottima review intitolata “The Anabolic Response to Plant-Based Protein Ingestion”, realizzata da Philippe J. M. Pinckaers, Jorn Trommelen, Tim Snijders & Luc J. C. van Loonche, la quale ci fornisce la bibliografia scientifica corretta per trattare nel migliore dei modi l’argomento in questione.
Il fatto che ci sia una palese e crescente tendenza globale di interesse verso le diete a base vegetale non è oggetto di dubbio alcuno. Ciò include un aumento del consumo di proteine di origine vegetale a scapito delle proteine di origine animale. Le proteine di origine vegetale sono ora frequentemente utilizzate anche nell’alimentazione sportiva. Finora, sappiamo che l’ingestione di proteine di origine vegetale, come le proteine della soia e del grano, determina una riduzione delle risposte di sintesi proteica muscolare post-prandiale rispetto all’ingestione di una quantità equivalente di proteine animali. Le minori proprietà anaboliche delle proteine vegetali rispetto a quelle di origine animale possono essere attribuite alle differenze nella loro digestione e nella cinetica di assorbimento degli amminoacidi che le compongono, nonché alle differenze nella composizione degli amminoacidi tra queste fonti proteiche. La maggior parte delle proteine vegetali ha un basso contenuto di aminoacidi essenziali e spesso è carente di uno o più aminoacidi specifici, come Lisina e Metionina. Tuttavia, ci sono grandi differenze nella composizione degli amminoacidi tra varie proteine di origine vegetale o fonti proteiche di origine vegetale. Finora, solo pochi studi hanno confrontato direttamente la risposta di sintesi proteica muscolare a seguito dell’ingestione di una proteina di origine vegetale rispetto a una proteina di origine animale di alta qualità. Le proprietà anabolizzanti inferiori proposte delle proteine di origine vegetale rispetto a quelle di origine animale possono essere compensate da:
- consumando una maggiore quantità di proteine di origine vegetale o fonte di proteine di origine vegetale per compensare la qualità inferiore;
- utilizzare miscele specifiche di proteine vegetali per creare un profilo aminoacidico più equilibrato;
- fortificare la proteina (fonte) a base vegetale con l’amminoacido/i libero/i specifico/i che è/sono carente/i.
Sono necessari studi clinici per valutare le proprietà anaboliche delle varie proteine di origine vegetale e delle loro fonti proteiche in vivo nell’uomo e per identificare i fattori che possono o meno compromettere la capacità di stimolare i tassi di sintesi proteica muscolare post-prandiale. Tale lavoro è necessario per determinare se la transizione verso una dieta più a base vegetale sia accompagnata da una transizione verso un maggiore fabbisogno di assunzione di proteine nella dieta.
Una singola sessione di esercizio contro resistenza aumenta i tassi di sintesi proteica muscolare e, in misura minore, i tassi di degradazione proteica muscolare [1]. Tuttavia, il bilancio proteico muscolare netto non diventa positivo a meno che non vengano forniti aminoacidi esogeni [2]. L’assunzione di proteine nella dieta aumenta i tassi di sintesi proteica muscolare a riposo [3,4,5] e aumenta ulteriormente i tassi di sintesi proteica muscolare durante il recupero dall’esercizio [2, 6, 7]. Diversi studi hanno dimostrato che oltre alla quantità di proteine [8,9,10,11], la cinetica di digestione e assorbimento [12] e la composizione aminoacidica di una proteina (fonte) [13,14] determinano in gran parte la risposta di sintesi proteica muscolare correlata all’alimentazione. La risposta sintetica delle proteine muscolari all’ingestione di proteine può, quindi, variare sostanzialmente tra le diverse fonti di proteine alimentari [13,14,15,16,17]. La risposta differenziale delle proteine muscolari sintetiche all’alimentazione dipende in gran parte dall’aumento post-prandiale delle concentrazioni plasmatiche di aminoacidi essenziali [5], con particolare importanza delle concentrazioni plasmatiche di Leucina [18,19,20,21,22,23,24] . L’aumento post-prandiale degli amminoacidi circolanti e il successivo aumento della velocità di sintesi proteica muscolare sono regolati su vari livelli, che vanno dalla digestione delle proteine alimentari, all’assorbimento degli amminoacidi, al sequestro degli amminoacidi splancnici, alla perfusione tissutale post-prandiale, all’assorbimento degli amminoacidi da parte del muscolo e l’attivazione del processo di sintesi delle proteine muscolari [4, 25]. Ad oggi, la maggior parte degli studi si è concentrata sulla valutazione della risposta sintetica delle proteine muscolari post-prandiale con fonti quali proteine del latte [15, 17, 21, 26,27,28,29,30,31] e della carne [10, 32,33,34]. Il sostanziale aumento dei tassi di sintesi proteica muscolare osservato a seguito dell’ingestione di queste proteine o fonti proteiche è stato attribuito al rapido aumento post-prandiale delle concentrazioni plasmatiche di aminoacidi essenziali circolanti.
Con la popolazione mondiale che si prevede raggiungerà circa 9,6 miliardi entro il 2050, la produzione di quantità sufficienti di alimenti convenzionali a base animale e ad alto contenuto proteico per soddisfare la domanda globale di proteine alimentari potrebbe non essere più auspicabile o fattibile. Le società occidentali benestanti mostrano una forte tendenza nella transizione verso una dieta più a base vegetale [35]. Ciò include un aumento del consumo di proteine di origine vegetale a scapito delle proteine di origine animale. Sebbene il mercato attuale offra già un’ampia selezione di proteine di origine vegetale e fonti proteiche di origine vegetale, vi è una scarsità di studi che hanno valutato la biodisponibilità e le proprietà anaboliche delle proteine di origine vegetale [13, 14, 16, 36 ,37,38]. Alcuni [14, 16, 36], ma non tutti [13, 37, 38] di questi studi mostrano che l’ingestione di proteine di origine vegetale, come le proteine della soia e del grano, determina una risposta sintetica delle proteine muscolari inferiore rispetto a l’ingestione di una quantità equivalente di proteine di origine animale. Di conseguenza, le proteine vegetali sono generalmente considerate avere proprietà anaboliche minori. Tuttavia, questo concetto si basa su un numero limitato di confronti e potrebbe non tradursi in tutte le fonti proteiche di origine vegetale. Le proprietà anabolizzanti minori proposte delle proteine vegetali rispetto a quelle animali sono state attribuite alle differenze nella loro digestione delle proteine e nella cinetica di assorbimento degli amminoacidi, nonché alle differenze nella composizione degli amminoacidi tra queste proteine. In precedenza, abbiamo riportato differenze sostanziali nella composizione degli amminoacidi tra varie fonti proteiche di origine vegetale [39]. Sebbene la composizione amminoacidica possa essere piuttosto variabile tra le diverse proteine vegetali, la maggior parte delle proteine vegetali ha un contenuto di amminoacidi essenziali relativamente basso e spesso è carente di uno o più amminoacidi specifici, come leucina, lisina e/o metionina [39]. Finora, solo pochi studi hanno confrontato direttamente la risposta sintetica delle proteine muscolari dopo l’ingestione di una proteina di origine vegetale rispetto a una proteina di origine animale di alta qualità [13, 14, 16, 36,37,38]. Inoltre, si sa ancora meno sulle diverse strategie che possono essere applicate per migliorare le proprietà anaboliche delle proteine vegetali.
Lo scopo della review che in questa sede viene usata come fonte principale, è quello di fornire una panoramica aggiornata sulla biodisponibilità e le proprietà anaboliche delle proteine vegetali in vivo nell’uomo. Si discuteranno diverse strategie che possono essere applicate per compensare la minore qualità delle proteine vegetali e, come tali, aumentare i tassi di sintesi proteica muscolare post-prandiale. Si tratterà la necessità di far progredire la ricerca nutrizionale estendendo gli studi dal semplice confronto dei tassi di sintesi proteica muscolare post-prandiale in seguito all’ingestione di isolati o concentrati proteici di origine vegetale rispetto a quelli di origine animale alla valutazione dell’impatto dell’ingestione di cibi integrali e pasti misti sul post-prandiale. sintesi proteica muscolare prandiale. Infine, si discuterà sulle credenze attuali riguardo all’uso di proteine vegetali nel campo della nutrizione sportiva e verranno forniti esempi di altre fonti proteiche alternative che possono essere applicate in futuro per supportare il condizionamento muscolare.
Digestione delle proteine e assorbimento degli aminoacidi:
Dopo l’ingestione di cibo, le proteine alimentari devono essere digerite e assorbite affinché gli aminoacidi diventino disponibili nella circolazione sistemica, dove possono modulare la sintesi proteica e il catabolismo del tessuto muscolare. La digestione delle proteine avviene nella bocca, nello stomaco e nell’intestino tenue, dove le proteine subiscono una scomposizione meccanica e chimica in costituenti più piccoli [40]. Quando gli amminoacidi vengono successivamente assorbiti dal lume gastrointestinale, sono considerati, per l’appunto assorbiti, assimilati. Una parte consistente degli amminoacidi assorbiti sarà trattenuta e metabolizzata nella regione splancnica, ma la maggior parte sarà rilasciata in circolo, dopodiché saranno disponibili per l’assorbimento nei tessuti periferici. La valutazione quantitativa della digeribilità delle proteine, dell’assorbibilità, dell’estrazione splancnica e del rilascio di aminoacidi nella circolazione è complessa e solo pochi studi hanno cercato di quantificare la manipolazione delle proteine post-prandiali in vivo nell’uomo [4]. Gli studi hanno riportato differenze sostanziali nella digestione delle proteine e nella cinetica di assorbimento degli aminoacidi in seguito all’ingestione di diverse proteine e fonti proteiche. In generale, gli alimenti integrali di origine vegetale hanno una capacità di assorbimento inferiore rispetto agli alimenti integrali di origine animale. Ad esempio, dati recenti sugli esseri umani hanno dimostrato che ~ 85-95% delle proteine negli albumi, nelle uova intere e nel pollo viene assorbito, rispetto al solo ~ 50-75% delle proteine in ceci, fagioli mung e piselli gialli [41, 42]. La minore assorbibilità delle proteine vegetali può essere attribuita a fattori antinutrizionali presenti nelle fonti proteiche vegetali, come fibre e tannini polifenolici [43]. Ciò sembra essere supportato dall’osservazione che la decorticazione dei fagioli mung aumenta la loro capacità di assorbire le proteine del ~ 10% [44]. Quando una proteina vegetale viene estratta e purificata da fattori antinutrizionali per produrre un isolato o concentrato proteico di origine vegetale, la successiva assorbibilità proteica raggiunge tipicamente livelli simili a quelli osservati per le fonti proteiche convenzionali di origine animale [45]. Ciò implica che la bassa assorbibilità delle fonti proteiche vegetali non è una proprietà intrinseca di una proteina vegetale di per sé, ma semplicemente il risultato della matrice alimentare integrale della fonte proteica.

L’assorbibilità delle proteine è stata a lungo riconosciuta come una componente cruciale della qualità nutrizionale di una fonte proteica [46]. Attualmente, l’Organizzazione delle Nazioni Unite per l’alimentazione e l’agricoltura (FAO) e l’Organizzazione Mondiale della Sanità (OMS) raccomandano il Digestible Indispensable Amino Acid Score (DIAAS) per quantificare la qualità delle proteine alimentari [47]. Il DIAAS di una proteina si basa sulla sua capacità di soddisfare il fabbisogno di ogni amminoacido essenziale, che si riflette nel profilo amminoacidico e nell’assorbibilità di ogni singolo amminoacido essenziale. Tuttavia, una limitazione del punteggio DIAAS è che tiene conto solo dell’assorbibilità complessiva delle proteine (assorbimento cumulativo) e non della cinetica di assorbimento degli amminoacidi (la velocità con cui vengono assorbiti gli amminoacidi). Diversi studi suggeriscono che un tasso più rapido di assorbimento degli aminoacidi è un fattore indipendente che modula la risposta di sintesi delle proteine muscolari dall’alimentazione [17, 48,49,50], sebbene tale associazione non sia sempre osservata [51, 52]. Sono disponibili pochi dati sulla cinetica di assorbimento degli aminoacidi in seguito all’ingestione di fonti proteiche vegetali o di isolati o concentrati proteici di origine vegetale. Per quanto riguarda l’aumento post-prandiale delle concentrazioni di aminoacidi circolanti come proxy per la digestione delle proteine e l’assorbimento degli aminoacidi, i dati sembrano suggerire che gli isolati o i concentrati proteici di origine vegetale sono rapidamente digeribili [13, 16, 38, 53, 54] e non sembrano differire sostanzialmente dalla maggior parte delle proteine o fonti proteiche di origine animale. È più che probabile che i fattori antinutrizionali nelle fonti proteiche vegetali (alimenti integrali) non solo compromettano l’assorbimento complessivo delle proteine, ma attenuino anche l’aumento post-prandiale dei tassi di assorbimento degli aminoacidi. A causa delle apparenti differenze nell’assorbimento delle proteine, nella digestione delle proteine e nella cinetica di assorbimento degli amminoacidi, dobbiamo fare attenzione quando ci riferiamo alle proteine vegetali per specificarle come fonti proteiche di origine vegetale o piuttosto come isolati o concentrati proteici di origine vegetale.
Composizione amminoacidica delle proteine:
Dopo la digestione delle proteine alimentari e l’assorbimento degli amminoacidi, una grande porzione degli amminoacidi derivati dalle proteine alimentari viene rilasciata nella circolazione. L’aumento post-prandiale della concentrazione di aminoacidi plasmatici attiva i processi di sintesi proteica nel tessuto muscolare scheletrico fornendo anche i precursori necessari per consentire l’aumento dei tassi di sintesi proteica muscolare [5, 7, 55]. Gli amminoacidi essenziali sono considerati i principali responsabili della stimolazione post-prandiale della sintesi proteica muscolare [55]. In accordo, è stata riportata una relazione dose-dipendente tra la quantità di aminoacidi essenziali ingeriti e la risposta di sintesi proteica muscolare post-prandiale [56]. Di conseguenza, le proteine con un contenuto più alto di aminoacidi essenziali sono generalmente considerate proteine di qualità più alta e hanno anche maggiori probabilità di stimolare (fortemente) la sintesi proteica muscolare post-prandiale. In precedenza, abbiamo dimostrato che il contenuto di amminoacidi essenziali delle proteine vegetali è generalmente inferiore rispetto alle proteine di origine animale [39, 57]. Nella review correntemente utilizzata, è stata inclusa una panoramica estesa della composizione amminoacidica di un’ampia varietà di proteine (fonti) che è stata analizzata (Fig. seguente). Tuttavia, ci sono anche proteine di origine vegetale (come proteine di soia, riso integrale, colza, piselli, mais e patate) che hanno un contenuto di aminoacidi essenziali relativamente alto, che soddisfa i requisiti raccomandati dall’OMS/FAO/UNU (United Nations University ) [58]. Infatti, i contenuti di aminoacidi essenziali delle proteine derivate da colza (29%), pisello (30%), mais (32%) e patate (37%) sono paragonabili o addirittura superiori a quelli della caseina (34%) o proteine dell’uovo (32%) [39]. Pertanto, alcune proteine vegetali potrebbero, in teoria, fornire amminoacidi essenziali sufficienti per consentire un significativo aumento post-prandiale del tasso di sintesi proteica del muscolo scheletrico.
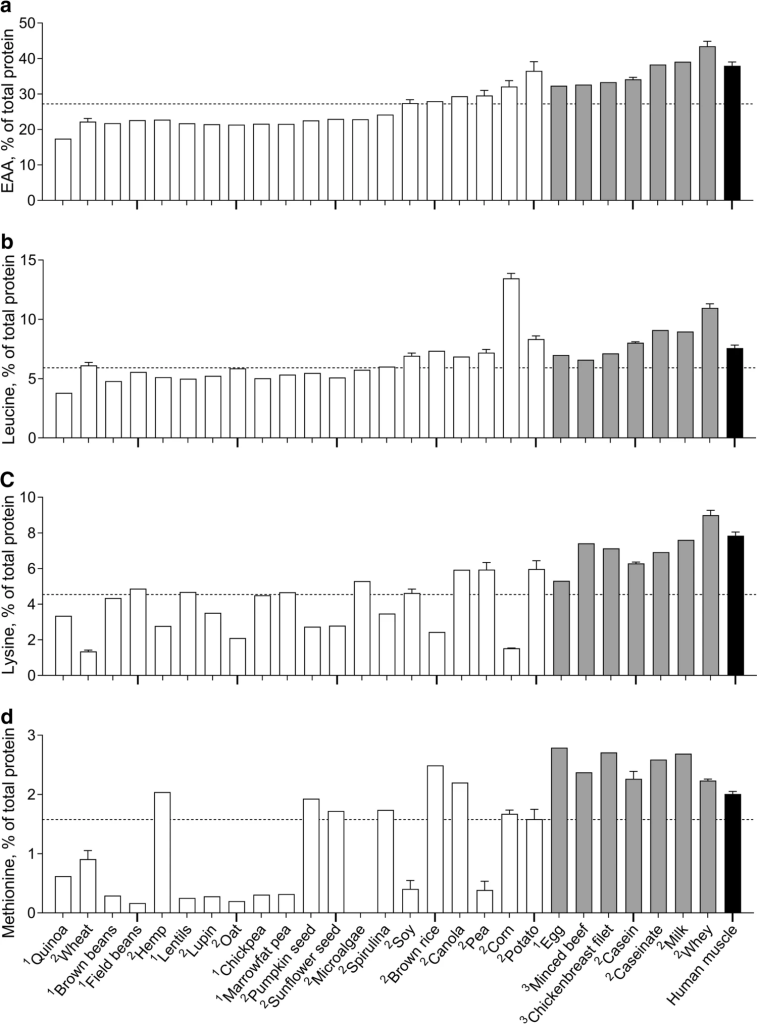
Tra tutti gli amminoacidi essenziali, la Leucina rappresenta l’amminoacido con le più forti proprietà anaboliche. La Leucina viene rilevata dalla sestrina2, che promuove la traslocazione del mTORC1 alla membrana del lisosoma dove viene attivato, con conseguente attivazione delle vie di segnalazione anabolizzanti a valle che controllano la sintesi proteica del tessuto muscolare [59,60,61 ]. L’attuale fabbisogno di Leucina all’interno di una determinata fonte proteica è fissato al 5,9% dall’OMS/FAO/UNU [58]. Mentre le proteine vegetali come la canapa (5,1% di Leucina) e il lupino (al 5,2%) sono inferiori, altre proteine come l’avena (5,9%), la spirulina (6,0%) e le proteine del grano (6,1%) forniscono Leucina in quantità prossime a quelle raccomandate. Inoltre, le proteine vegetali come la soia (6,9%), colza (6,9%), pisello (7,2%), riso integrale (7,4%), patate (8,3%) e mais (13,5%) hanno contenuti di Leucina che superano il requisiti consigliati. Il contenuto di Leucina delle proteine della patata (8,3%) è lievemente più elevato rispetto alla caseina (8,0%) o alle proteine dell’uovo (7,0%). Inoltre, il contenuto di Leucina delle proteine del mais (13,5%) è addirittura superiore alle proteine del siero di latte (11,0%), quest’ultima delle quali è tipicamente considerata la proteina con il più alto contenuto di Leucina e il più forte potenziale anabolico tra le proteine di origine animale ( figura seguente).
Precedenti studi hanno dimostrato che l’ingestione di 20-25g di proteine del siero di latte (che fornisce 2,2-2,7g di Leucina) aumenta notevolmente i tassi di sintesi proteica muscolare [11, 62,63,64]. La quantità di Leucina ingerita necessaria per stimolare al massimo il processo di sintesi proteica muscolare può essere modulata dalla sua matrice proteica (ad es. Digestione e cinetica di assorbimento e disponibilità di altri amminoacidi). Tuttavia, se assumiamo che l’ingestione di 2,7g di Leucina sia sufficiente per innescare al massimo il processo di sintesi proteica muscolare, è evidente che ciò può essere ottenuto anche mediante l’ingestione di fonti proteiche di origine vegetale. Le proteine vegetali possono fornire la stessa quantità di Leucina semplicemente fornendo una quantità equivalente di proteine in base al loro contenuto intrinseco del amminoacido in questione. Ad esempio, per le proteine derivate dal mais (13,5% di Leucina), l’ingestione di soli 20 g di proteine fornirebbe già 2,7g di Leucina. Al contrario, > 25g di altre proteine vegetali dovrebbero essere ingeriti per fornire 2,7g di Leucina. Infatti, l’ingestione di ~ 33g di proteine delle patate, ~ 37g di quelle del riso integrale, ~ 38g di quelle dei piselli, ~ 40g di quelle della colza, ~ 40g di quelle della soia e ~ 45g di proteine del grano sarebbe necessaria per ingerire 2,7g di Leucina [39]. Dalle proteine e dalle fonti proteiche analizzate, la proteina della quinoa sembra avere il contenuto di Leucina più basso (3,8%). Sarebbe necessario ingerire ~ 71g di proteine della quinoa per fornire 2,7g di Leucina. Naturalmente, questo rappresenta solo la quantità di Leucina che si ritiene attivi completamente il processo di sintesi delle proteine muscolari. Oltre ad attivare le vie di segnalazione che stimolano la sintesi proteica muscolare, possono essere necessari significative quantità di amminoacidi essenziali come precursori per consentire un efficiente accrescimento proteico muscolare [65]. Un apporto insufficiente di uno (o più) aminoacidi essenziali o non essenziali sarebbe teoricamente restrittivo e, come tale, attenuerebbe l’aumento post-prandiale del tasso di sintesi proteica muscolare.
Oltre ad avere un contenuto di aminoacidi essenziali relativamente basso (cioè basso contenuto di Leucina), molte proteine vegetali sono carenti di uno o più aminoacidi specifici. Le proteine vegetali sono spesso particolarmente basse nel contenuto di Lisina e/o Metionina (da 1,4 a 6% e da 0,2 a 2,5%, rispettivamente) rispetto alle proteine animali (da 5,3 a 9,0% e da 2,2 a 2,8%, rispettivamente). Il contenuto di Lisina nel frumento (1,4%), nel mais (1,5%), nell’avena (2,1%), nel riso integrale (2,4%), nei semi di zucca (2,7%), nei semi di girasole (2,8%), nella canapa (2,8%), nella quinoa (3,3%), e nelle proteine della spirulina (3,5%) e del lupino (3,5%) sono ben al di sotto dei requisiti OMS/FAO/UNU (4,5%) e sostanzialmente inferiori rispetto alle proteine della soia (4,6%), colza (5,9%), pisello (5,9%) e patate (6,0%). Un numero considerevole di proteine vegetali non soddisfa inoltre il fabbisogno di Metionina (1,6%), con avena (0,2%), fagiolino (0,2%), fagiolo marrone (0,3%), lenticchia (0,3%), ceci (0,3%). ), pisello grasso di midollo (0,3%), lupino (0,3%), pisello (0,4%), soia (0,4%), quinoa (0,6%) e proteine del grano (0,9%) che forniscono molta meno Metionina. Al contrario, altre proteine vegetali come quelle della patata (1,6%), del mais (1,7%), della spirulina (1,7%), dei semi di girasole (1,7%), dei semi di zucca (1,9%), della canapa (2,0%), della colza ( Il 2,2%) e le proteine del riso integrale (2,5%) tendono a soddisfare i requisiti di contenuto di Metionina. Chiaramente, c’è una notevole variabilità nella composizione degli amminoacidi tra le molte diverse proteine vegetali e le fonti proteiche vegetali.
Solo una manciata di studi ha confrontato direttamente i tassi di sintesi proteica muscolare post-prandiale dopo l’ingestione di proteine vegetali rispetto a quelle di origine animale [13, 14, 16, 36,37,38]. È stato dimostrato che l’ingestione di proteine della soia è meno efficace nello stimolare i tassi di sintesi proteica muscolare post-prandiale rispetto all’ingestione di una quantità equivalente di proteine del siero di latte sia nei giovani che negli anziani a riposo e durante il recupero dall’esercizio [13, 14, 36], ma più efficace delle proteine della caseina [13]. Inoltre, Yang et al. [14] hanno mostrato che l’ingestione di una quantità maggiore (40g contro 20g) di proteine della soia non ha compensato la minore risposta sintetica delle proteine muscolari rispetto all’ingestione di 20g di proteine del siero di latte isolate. Non è stato osservato un significativo aumento post-prandiale dei tassi di sintesi proteica muscolare a seguito dell’ingestione di 35g di idrolizzato proteico di grano in un gruppo di uomini anziani sani [16]. Quando è stato aumentata la quantità di idrolizzato proteico del grano a 60g, fornendo così la stessa quantità di Leucina presente in 35g di proteine del siero di latte, si è osservato un significativo aumento dei tassi di sintesi proteica muscolare. Chiaramente, questi dati sembrano supportare l’ipotesi che le differenze nella composizione amminoacidica possano essere, almeno in parte, compensate ingerendo maggiori quantità della specifica fonte proteica.
Più recentemente, non sono state osservate differenze nei tassi di sintesi proteica muscolare post-prandiale a seguito dell’ingestione di 30g di idrolizzato di proteine del grano o della stessa quantità di concentrato di proteine del latte [38]. In contrasto con il lavoro precedente del gruppo di ricerca responsabile della review utilizzata per questo articolo, questo studio è stato condotto su giovani adulti attivi nel tempo libero. La maggiore sensibilità del tessuto muscolare scheletrico alle proprietà anaboliche degli amminoacidi dovuta al più alto livello di attività abituale negli adulti più giovani e più attivi [66, 67] potrebbe essere stata responsabile dell’assenza di differenze misurabili nella risposta post-prandiale di sintesi proteica in seguito all’ingestione di 30g di proteine del grano rispetto a quelle derivate dal latte. Chiaramente, dobbiamo capire che le differenze nelle risposte anaboliche all’ingestione di fonti proteiche vegetali rispetto a quelle animali dipenderanno anche dalla quantità di proteine fornite e dalla popolazione specifica in cui viene effettuato il confronto.
In breve, la composizione aminoacidica delle fonti proteiche di origine vegetale può essere molto variabile. Pertanto, sono necessari ulteriori studi per valutare le proprietà anaboliche di varie proteine di origine vegetale e animale e fonti proteiche oltre i pochi confronti attualmente disponibili (proteine di soia e grano). Inoltre, va notato che l’esito di questi confronti sarà probabilmente diverso a seconda della quantità di proteine ingerite e della popolazione e dell’ambiente in cui vengono effettuati i confronti.
Migliorare le proprietà anabolizzanti delle proteine vegetali:
Come discusso in precedenza, le proprietà anaboliche minori proposte delle proteine di origine vegetale rispetto a quelle di origine animale possono essere attribuite a differenze nell’assorbimento delle proteine, nella digestione delle proteine e nella cinetica di assorbimento degli amminoacidi e/o nella composizione degli amminoacidi delle proteine. Esistono varie strategie nutrizionali che possono essere applicate per migliorare le proprietà anaboliche delle proteine vegetali a seconda del/i fattore/i responsabile/i della ridotta capacità anabolica proposta.
L’assorbibilità di una fonte proteica vegetale è spesso compromessa dalla presenza di fattori antinutrizionali nelle fonti proteiche vegetali, come fibre e tannini polifenolici [43]. La lavorazione di cibi integrali può aumentare fortemente l’assorbibilità delle proteine intrinseche. È stato dimostrato che la decorticazione dei fagioli prima del consumo rappresenta un mezzo efficace per aumentare la capacità di assorbire la proteina intrinseca [44]. L’estrazione di proteine e la purificazione da fattori antinutrizionali per produrre un isolato o concentrato di proteine di origine vegetale migliora ulteriormente l’efficienza con cui le proteine di origine vegetale possono essere assorbite [45]. Inoltre, il trattamento termico e l’idrolizzazione della proteina aumentano ulteriormente la digeribilità e/o migliorano la digestione delle proteine e la cinetica di assorbimento degli amminoacidi [3, 68]. Questi processi sono generalmente applicati nella maggior parte delle fonti proteiche vegetali e animali che acquistiamo come prodotti alimentari (lavorati) o come isolati o concentrati proteici. Chiaramente, quando si tratta di alimenti, i vari processi coinvolti nella raccolta, lavorazione, conservazione, cottura, masticazione e ingestione contribuiscono tutti all’assorbibilità della fonte proteica finale e alla velocità della sua digestione delle proteine e assorbimento degli amminoacidi. Questi processi differiscono anche tra i vari alimenti che insieme formano i nostri pasti compositi. Il lavoro futuro dovrà affrontare le proprietà anaboliche degli alimenti reali e, cosa più importante, la risposta di sintesi delle proteine muscolari all’ingestione di pasti completi.
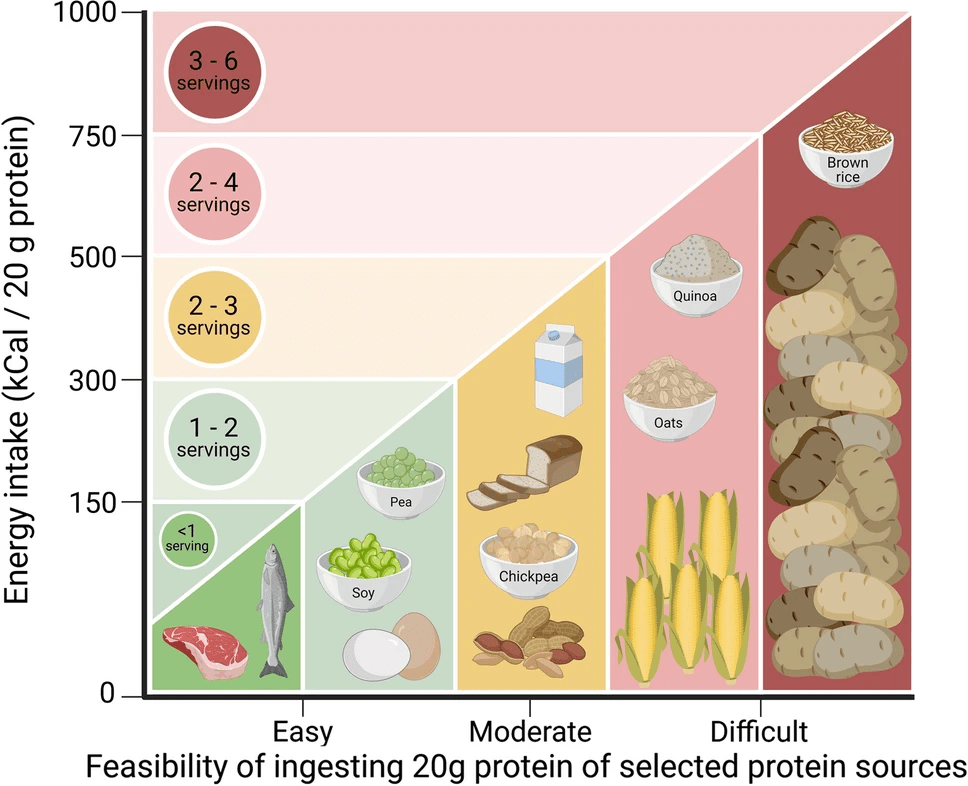
Le proprietà anaboliche minori di alcune proteine di origine vegetale possono essere attribuite al contenuto di amminoacidi essenziali (più basso) e/o alle carenze di amminoacidi specifici di quella fonte proteica. Il modo più semplice per compensare la qualità proteica inferiore di una fonte proteica a base vegetale rispetto a quella animale è semplicemente consumare una quantità maggiore della proteina di qualità inferiore. A supporto, abbiamo osservato che l’ingestione di 60g rispetto a 35g di un idrolizzato proteico di grano ha effettivamente aumentato i tassi di sintesi proteica muscolare post-prandiale in un gruppo di uomini anziani sani [16]. Sebbene questa strategia possa non applicarsi a tutte le proteine vegetali [64], l’aumento del dosaggio proteico per compensare il minor contenuto di aminoacidi essenziali o una specifica carenza di aminoacidi dovrebbe teoricamente migliorare la risposta di sintesi proteica post-prandiale. Tuttavia, mentre una tale strategia sarebbe facile da applicare quando si considera l’uso di un isolato o concentrato di proteine di origine vegetale, potrebbe non essere sempre pratica o fattibile quando si considerano gli alimenti (interi) a base vegetale. La minore densità proteica della maggior parte delle fonti proteiche vegetali aumenterebbe notevolmente sia il contenuto calorico totale che il volume del cibo vegetale che dovrebbe essere consumato. Il semplice consumo di 20g di proteine sotto forma di fonte proteica vegetale è già impegnativo, sia dal punto di vista del volume del cibo che del contenuto calorico. La ricerca attuale si è concentrata sulla valutazione delle proprietà anaboliche di isolati proteici o idrolizzati di origine vegetale. L’ingestione di grandi quantità di una singola fonte proteica vegetale sotto forma di alimento intero non sarà sempre fattibile, specialmente in un ambiente più clinico in cui l’assunzione di cibo è generalmente compromessa, o in un ambiente sportivo in cui gli atleti devono aderire a rigide regole quantitative di calorie.


Una strategia alternativa per aumentare il potenziale anabolico di una fonte proteica vegetale consiste nel combinare diversi tipi di proteine e/o fonti per fornire una miscela proteica con un profilo aminoacidico più equilibrato. Mentre alcune proteine vegetali sono particolarmente carenti di Lisina, altre sono carenti di Metionina [39]. Ad esempio, le proteine del mais, della canapa, del riso integrale, della soia e dei piselli hanno un basso contenuto di Lisina e/o Metionina. Per ogni fonte proteica, questa carenza potrebbe essere compensata consumando 2-4 volte di più della stessa proteina. Tuttavia, la combinazione di proteine di mais, canapa o riso integrale (basso contenuto di Lisina e alto contenuto di Metionina) con una quantità uguale di proteine della soia o dei piselli (basso contenuto di Metionina e alto contenuto di Lisina) fornisce una miscela con un profilo aminoacidico più equilibrato. Tali miscele richiederebbero solo 1,1-1,9 volte più proteine da consumare per compensare carenze specifiche di aminoacidi [39]. Oltre alle esclusive miscele proteiche a base vegetale, anche le combinazioni di proteine vegetali e animali possono svolgere un ruolo importante nella tendenza a ridurre il consumo di alimenti di origine animale senza compromettere la qualità delle proteine. L’avena, il lupino, la quinoa e le proteine del grano hanno un basso contenuto sia di Lisina che di Metionina, che potrebbe teoricamente essere compensato ingerendo da 3 a 8 volte più della rispettiva fonte proteica. Tuttavia, la miscelazione di queste proteine con una quantità uguale di una proteina di origine animale richiederebbe solo 1,05-1,4 volte di più della rispettiva miscela proteica da consumare per fornire quantità sufficienti di tutti gli amminoacidi essenziali [39]. Tali miscele proteiche rappresenterebbero la composizione di una dieta onnivora, in cui ~ 40-50% delle proteine consumate è generalmente derivato da fonti vegetali [69]. A supporto, sono stati riportati robusti aumenti dei tassi di sintesi proteica muscolare post-prandiale in seguito all’ingestione di siero di latte, caseina e miscele di proteine della soia [70,71,72]. Più recentemente, non sono state osservate differenze nella risposta sintetica delle proteine muscolari post-prandiali dopo l’ingestione di 30g di proteine del latte o di una miscela proteica di 30g che combina proteine del grano e del latte [38]. Molte altre miscele proteiche che combinano due o più fonti proteiche in vari rapporti possono essere composte per raggiungere obiettivi particolari in termini di composizione aminoacidica, prezzo, gusto e sostenibilità senza compromettere la capacità di stimolare la sintesi proteica muscolare.
Se una specifica carenza di aminoacidi costituisce il fattore limitante per una proteina a base vegetale per aumentare i tassi di sintesi proteica muscolare post-prandiale, un’opzione alternativa sarebbe quella di fortificare la proteina con uno o più aminoacidi (liberi) specifici. Poiché la Leucina è considerata fondamentale per la risposta di sintesi proteica muscolare post-prandiale, la fortificazione con Leucina libera potrebbe rappresentare una strategia fattibile per aumentare i tassi di sintesi proteica muscolare post-prandiale. A supporto, è stato riportato che la fortificazione con Leucina di un bolo di proteine intatte, miscele di aminoacidi o pasti misti aumenta ulteriormente i tassi di sintesi proteica muscolare post-prandiale [18, 20, 73, 74]. In base all’attuale conoscenza, non ci sono molti dati disponibili sull’impatto della fortificazione con Leucina delle proteine vegetali sui successivi tassi di sintesi proteica muscolare post-prandiale. Uno studio sui roditori ha dimostrato tassi di sintesi proteica muscolare inferiori dopo l’alimentazione con frumento rispetto alle proteine del siero di latte [75]. L’arricchimento delle proteine del grano con Leucina libera, per far corrispondere il contenuto di Leucina in una quantità equivalente di proteine del siero di latte, ha aumentato i tassi di sintesi proteica muscolare a un livello che non era più diverso dalla risposta osservata dopo l’alimentazione con proteine del siero di latte. Al contrario, non sono stati osservati tassi di sintesi proteica muscolare post-prandiale più elevati dopo l’ingestione di 20g di proteine della soia fortificate con 2,5g di Leucina libera rispetto a 20g di proteine della soia solo durante il recupero dall’esercizio nei giovani adulti [37]. Infatti, non sono state osservate differenze misurabili nei tassi di sintesi proteica muscolare post-prandiale dopo l’ingestione di 20g di siero di latte, 20g di proteine della soia o 20g di proteine della soia fortificate con 2,5g di Leucina libera per corrispondere alla quantità di Leucina presente in 20g di proteine del siero di latte [14] . Si può solo supporre che in queste condizioni il contenuto di Leucina non fosse un fattore limitante all’aumento post-prandiale dei tassi di sintesi proteica muscolare. Ciò può essere spiegato dall’aumento indotto dall’esercizio della sensibilità del tessuto muscolare scheletrico alle proprietà stimolanti di un aumento della concentrazione di Leucina circolante. Poiché molte proteine vegetali sono carenti di Lisina e/o Metionina, è stato ipotizzato che la fortificazione di queste proteine vegetali con i rispettivi amminoacidi carenti possa amplificare il loro potenziale anabolico. Sebbene la fortificazione con aminoacidi liberi selezionati sia comunemente applicata nei prodotti a base vegetale progettati per sostituire la carne o i latticini, non ci sono studi che abbiano valutato l’efficacia di tale strategia come mezzo per migliorare le proprietà anaboliche dell’ingestione di proteine vegetali .
Gestione postprandiale delle proteine dopo l’ingestione di un pasto:
Il lavoro sulle proprietà anaboliche delle proteine vegetali è stato in gran parte limitato al confronto dei tassi di sintesi proteica muscolare post-prandiale dopo l’ingestione di una manciata di isolati o concentrati proteici di origine vegetale rispetto a quelli di origine animale. Tuttavia, le proteine alimentari vengono generalmente consumate sotto forma di alimento intero o prodotto alimentare e come parte di un pasto più completo e composito. Ciò fornisce automaticamente una miscela di diverse fonti proteiche a base vegetale, migliorando la risposta sintetica delle proteine muscolari post-prandiali. Inoltre, quando si consumano proteine come parte di un prodotto e/o pasto, altri nutrienti come carboidrati, grassi, micronutrienti e altri composti (anti-)nutrizionali possono modificare la digestione proteica post-prandiale e la cinetica di assorbimento degli aminoacidi e la successiva sintesi proteica muscolare[76]. A sostegno, [77,78,79] è stato dimostrato che la digestione delle proteine post-prandiale e l’assorbimento degli amminoacidi possono essere ritardati quando carboidrati o grassi vengono ingeriti insieme alle proteine. Tuttavia, questo non sembra avere un grande impatto sui tassi di sintesi proteica muscolare post-prandiale [77, 80]. Inoltre, è stato suggerito che la co-ingestione di carboidrati con proteine potrebbe aumentare i tassi di sintesi proteica muscolare post-prandiale stimolando il rilascio di insulina post-prandiale. Tuttavia, l’impatto del rilascio di insulina endogena sul tasso di sintesi proteica muscolare post-prandiale si è dimostrato permissivo piuttosto che stimolante e il modesto aumento del rilascio di insulina osservato solo dopo l’ingestione di proteine è già sufficiente per consentire alla sintesi proteica muscolare post-prandiale di raggiungere i valori massimi. [81]. A supporto, è stato dimostrato che la co-ingestione di carboidrati con proteine non aumenta i tassi di sintesi proteica muscolare post-prandiale né a riposo [77, 78, 82] né durante il recupero dall’esercizio [79, 83, 84].
Sebbene tali studi forniscano informazioni sull’impatto della co-ingestione di altri macronutrienti sulla digestione delle proteine e sulla cinetica di assorbimento degli aminoacidi e sulla successiva stimolazione post-prandiale della sintesi proteica muscolare, non riflettono necessariamente la risposta anabolica all’ingestione degli alimenti interi da cui sono derivati. Mentre diversi studi hanno valutato i tassi di sintesi proteica muscolare post-prandiale a seguito dell’ingestione di cibi integrali come latte [32], carne [10, 32,33,34] e uova [85], ci sono meno dati disponibili sull’anabolismo in risposta all’ingestione di cibi integrali di origine vegetale. Questo divario di conoscenze ci impedisce di comprendere le vere proprietà anaboliche del consumo di alimenti a base vegetale poiché la matrice alimentare degli alimenti a base vegetale può compromettere la digestione delle proteine e la cinetica di assorbimento degli aminoacidi e, in quanto tale, attenuare l’aumento postprandiale dei tassi di sintesi proteica muscolare. Il lavoro precedente ha mostrato differenze sostanziali nelle risposte degli aminoacidi plasmatici post-prandiali dopo l’ingestione di una colazione a base di uova rispetto a quella a base di cereali, fornendo una quantità iso-azotata di proteine [86]. Le differenze osservate nell’aumento post-prandiale delle concentrazioni plasmatiche di aminoacidi dopo la colazione a base di uova rispetto a quella a base di cereali non hanno determinato differenze nei tassi di sintesi proteica muscolare. Ciò mostra chiaramente che la risposta sintetica delle proteine muscolari all’ingestione del pasto è complessa e non può essere prevista semplicemente valutando la composizione degli aminoacidi proteici o dei profili di aminoacidi plasmatici post-prandiali.
La matrice di cibi integrali, prodotti alimentari e/o pasti composti è, almeno in parte, definita dalla combinazione di una varietà di macronutrienti, micronutrienti e composti (anti)nutrizionali. Tuttavia, la matrice alimentare viene modificata anche dalla trasformazione alimentare commerciale e dalla preparazione alimentare interna, che spesso include il riscaldamento e/o la cottura [3, 87, 88]. Prima del consumo, il cibo viene tagliato o schiacciato e masticato, il che influirà anche sul tasso di digestione delle proteine e sull’assorbimento degli aminoacidi [3, 89, 90]. Numerosi fattori giocano un ruolo nel determinare la risposta sintetica delle proteine muscolari post-prandiali all’ingestione di cibo. Oltre all’impatto delle singole matrici alimentari sulla digestione delle proteine e sulla cinetica di assorbimento degli aminoacidi, è importante considerare che un pasto composto spesso include una varietà di alimenti di origine animale e vegetale, o almeno vari alimenti di origine vegetale. Ci sono attualmente informazioni limitate all’interno della letteratura sulla (potenziale) interazione tra diverse fonti proteiche all’interno di un singolo pasto sulla digestione delle proteine e sulla cinetica di assorbimento degli aminoacidi e sulla risposta sintetica delle proteine muscolari post-prandiali all’alimentazione.
Sebbene siano state acquisite molte informazioni sui vari fattori che modulano l’assorbimento delle proteine alimentari, la digestione delle proteine e l’assorbimento degli aminoacidi e la sintesi proteica muscolare post-prandiale, non si hanno informazioni sulla gestione delle proteine post-prandiali dopo l’ingestione di cibi integrali e pasti misti. Sono necessari studi futuri per valutare le proprietà anaboliche dell’ingestione di pasti composti e l’impatto che questo può avere sul condizionamento muscolare sia in salute che in malattia.
Proteine vegetali nella nutrizione sportiva:
Il passaggio verso una dieta più incentrata su fonti vegetali ha nell’ultimo periodo suscitato molto interesse tra gli atleti. Non sorprende che ciò sollevi anche interrogativi sull’impatto della (inferiore) qualità delle proteine vegetali sul condizionamento muscolare durante il recupero dall’esercizio. Esistono solo pochi studi che hanno confrontato le risposte di sintesi proteica muscolare post-esercizio a seguito dell’ingestione di proteine vegetali rispetto a quelle di origine animale [13, 14, 16, 36,37,38]. In questi studi, la principale fonte proteica di origine vegetale che è stata applicata è rappresentata dalla soia. Alcuni studi [13, 14, 36], ma certamente non tutti [37], hanno riportato un aumento minore dei tassi di sintesi proteica muscolare post-esercizio dopo l’ingestione di proteine della soia rispetto a una quantità equivalente di proteine del latte o proteine del siero di latte. Inoltre, è stato dimostrato che le proteine della soia determinano maggiori tassi di sintesi proteica muscolare durante le 3 ore di recupero post-esercizio rispetto alle proteine della caseina [13]. Poiché l’esercizio rende il muscolo più sensibile alle proprietà anaboliche della somministrazione di aminoacidi o proteine, si potrebbe ipotizzare che l’aumento post-prandiale della concentrazione di Leucina plasmatica in circolo sia di minore importanza quando si consumano proteine dopo l’esercizio. Pertanto, il contenuto inferiore di leucina della maggior parte delle proteine vegetali potrebbe non limitare più i tassi di sintesi proteica muscolare post-prandiale durante il recupero dall’esercizio. Di conseguenza, è più probabile che la capacità di una proteina di stimolare la sintesi proteica muscolare post-esercizio sia determinata dalla quantità di aminoacidi forniti come precursori per la sintesi proteica. Pertanto, un’ampia disponibilità di tutti gli amminoacidi senza carenze di amminoacidi specifici può essere di primaria importanza nel determinare la fonte proteica vegetale ottimale (miscela) per supportare il condizionamento muscolare post-esercizio. Chiaramente, la ricerca è giustificata per confrontare i tassi di sintesi proteica muscolare durante il recupero dall’esercizio mentre si ingeriscono proteine o fonti proteiche diverse da quelle vegetali rispetto a quelle animali. Questi studi forniranno informazioni sulle caratteristiche preferite di una proteina alimentare (miscela) che ottimizzerebbe la risposta adattativa del muscolo scheletrico in risposta allo stimolo dell’esercizio.
Gli studi di intervento a lungo termine che valutano l’impatto dell’integrazione proteica sulla risposta adattativa all’allenamento di tipo di contro-resistenza tendono a mostrare maggiori guadagni di massa muscolare e forza quando si applica l’integrazione proteica [91, 92]. Sono stati riportati aumenti dei tassi giornalieri di sintesi proteica muscolare e/o guadagni di massa muscolare a seguito di esercizi di tipo contro-resistenza durante l’integrazione di fonti proteiche di origine vegetale, come soia [93,94,95,96], piselli [97], riso [98] e proteine della patata [99]. Tuttavia, rimane dubbio se questi guadagni di massa muscolare e forza durante l’allenamento con esercizi contro-resistenza differiscano dai guadagni osservati quando viene integrata una quantità equivalente di proteine animali. Una recente meta-analisi ha concluso che l’origine animale o vegetale della fonte proteica integrata non influisce sui guadagni di massa magra o forza muscolare dopo un allenamento prolungato contro-resistenza [100]. Tuttavia, sembra evidente che questa conclusione dipenderebbe anche dalla popolazione, dal tipo di allenamento, dallo stato di allenamento dei volontari e soprattutto dalla quantità di proteine integrate e dall’assunzione abituale di proteine. Recenti lavori di Hevia-Larraín et al. [101] non hanno riportato differenze nella massa muscolare e nell’accumulo di forza dopo un allenamento prolungato con esercizi contro-resistenza mentre si consumava una dieta esclusivamente vegetale o una dieta onnivora. Questo potrebbe non essere una sorpresa poiché i soggetti non allenati stavano consumando una dieta ad alto apporto proteico (~ 1,6g/kg di massa corporea/giorno) durante il periodo di intervento dell’esercizio, con notevoli quantità di proteine (isolati di proteine della soia o del siero di latte) integrate due volte al giorno.
Sulla base delle differenze descritte nell’assorbimento delle proteine, nella digestione delle proteine e nella cinetica degli amminoacidi e nei tassi di sintesi proteica muscolare post-prandiale in seguito all’ingestione di fonti proteiche vegetali rispetto a quelle animali, potremmo ipotizzare che quando si passa a una dieta con prevalenza di base vegetale, sarebbero necessarie più proteine alimentari per consentire la stessa stimolazione dei tassi di sintesi proteica muscolare. Ciò implicherebbe anche che dovrebbero essere consumate e/o integrate più proteine vegetali per raggiungere lo stesso livello di accrescimento della massa muscolare in risposta ad un allenamento prolungato di tipo contro-resistenza. Tuttavia, la maggior parte degli atleti consuma già grandi quantità di proteine a causa del loro maggiore apporto energetico. Un’indagine a livello nazionale su atleti ben allenati ha riportato un apporto proteico di ~ 1,5g di proteine per kg di massa corporea al giorno [102]. Sebbene ciò rappresenti un apporto proteico giornaliero ben al di sopra della dose giornaliera raccomandata (RDA) proposta dall’OMS (0,8g/kg/giorno), è stato sostenuto che un apporto proteico di 1,6g/kg massimizzerebbe i guadagni di massa muscolare e forza in risposta ad un allenamento prolungato di tipo contro-resistenza [92]. Di conseguenza, si potrebbe ipotizzare che una dieta che fornisca proteine di bassa qualità potrebbe compromettere la risposta adattativa del muscolo scheletrico in risposta all’esercizio fisico. Tuttavia, quest’ultimo rappresenta più un concetto accademico in quanto piccole differenze nella qualità delle proteine non avranno un grande impatto sulla risposta adattativa all’esercizio fisico quando vengono consumate abitualmente quantità così grandi di proteine. Inoltre, gli atleti onnivori hanno un apporto proteico derivante da fonti vegetali già > 40% in rapporto al loro apporto proteico giornaliero totale[102].
Più importante è il potenziale impatto negativo di una transizione verso una dieta principalmente basata su fonti vegetali in condizioni in cui gli atleti riducono il loro apporto energetico e, come tale, riducono, in rapporto, il potenziale consumo di proteine e assimilazione amminoacidica. Gli atleti che cercano di ridurre il peso corporeo mediante la restrizione calorica o gli atleti che si stanno riprendendo da un infortunio richiederebbero in realtà un apporto proteico simile o addirittura maggiore (in termini assoluti) consumando meno cibo. In tali condizioni la qualità delle proteine consumate è della massima importanza e il passaggio a una dieta con proprietà meno anaboliche potrebbe compromettere il mantenimento muscolare o attenuare/rallentare il recupero muscolare. Pertanto, è necessario valutare gli aspetti positivi e potenzialmente negativi della transizione verso una dieta a base maggioritaria di fonti vegetali. Inoltre, è necessario valutare se ciò sia accompagnato da una modifica alimentare volta ad un maggiore consumo proteico per aumentato fabbisogno. È quindi richiesta la valutazione dell’impatto del consumo di una dieta composta da cibi integrali a base vegetale in modo particolare sulla massa muscolare e sulla funzione in varie popolazioni, sia in condizioni di salute che in stato patologico.
Fonti proteiche alternative:
Attualmente si stanno facendo enormi investimenti nella ricerca di una produzione più sostenibile di fonti proteiche di alta qualità che non siano derivate da animali. Questo processo si è ora esteso da fonti proteiche a base vegetale a varie altre fonti proteiche, tra cui la crescita di lieviti, funghi, microalghe, l’allevamento di insetti e persino la realizzazione di carne di sintesi in laboratorio come potenziali fonti proteiche per il consumo umano . Sebbene una discussione su queste fonti proteiche alternative e sostenibili vada oltre lo scopo di questo articolo, è utile almeno discutere su due di queste fonti proteiche poiché sono state recentemente valutate per la loro capacità di stimolare i tassi di sintesi proteica muscolare post-prandiale in vivo nell’uomo.
Recenti lavori hanno esaminato le proprietà anaboliche di una fonte alimentare derivata dalla coltivazione di un fungo (Fusarium venenatum), dando luogo a quella che è stata denominata micoproteina [103,104,105]. È stato riportato che questa fonte proteica ha un alto contenuto proteico (~ 45%) con la proteina che mostra una composizione di amminoacidi che non differisce molto dalle proteine del latte [106]. Il lavoro precedente ha suggerito una buona digeribilità basata sull’osservazione delle concentrazioni di aminoacidi essenziali (soprattutto Leucina) nel plasma post-prandiale le quali erano comparabili dopo l’ingestione di micoproteine all’ingestione di una quantità equivalente di proteine del latte. Più recentemente, questi ricercatori hanno mostrato che l’ingestione di un singolo bolo di micoproteine (70g, fornendo 31,5 g di proteine) ha aumentato i tassi di sintesi proteica muscolare sia a riposo che post-esercizio nei giovani maschi, con una risposta di sintesi proteica muscolare post-prandiale, che era maggiore della risposta osservata dopo aver ingerito un bolo di proteine del latte abbinato alla Leucina (31g, fornendo 26,2g di proteine) [103]. Questi dati mostrano che i funghi possono fornire una fonte proteica vitale e di alta qualità che è efficace nello stimolare la sintesi proteica muscolare.
Un’altra fonte proteica alimentare alternativa che ha suscitato molto interesse sono gli insetti commestibili. Sebbene tecnicamente gli insetti si classifichino anche come animali, possono essere prodotti su una scala commerciale più praticabile e sostenibile e, come tali, costituiscono un altro candidato promettente per contribuire a garantire la sicurezza alimentare globale [107, 108]. Gli insetti hanno un alto contenuto proteico e le loro proteine hanno una composizione di amminoacidi che ricorda da vicino le proteine animali convenzionali di alta qualità [107]. Recentemente, sono stati prodotti vermi della farina i quali sono stati nutriti con amminoacidi marcati con isotopi stabili [25], consentendo la quantificazione diretta della digestione delle proteine e la cinetica di assorbimento degli amminoacidi e la successiva risposta sintetica delle proteine muscolari a riposo e durante il recupero dall’esercizio dopo l’ingestione di un singolo bolo di vermi della farina. Le proteine derivate dal verme della farina sono state rapidamente digerite e assorbite nella loro componente amminoacidica, aumentando fortemente i tassi di sintesi proteica muscolare post-prandiale. Infatti, la risposta di sintesi proteica muscolare post-prandiale osservata non differiva dalla risposta osservata dopo l’ingestione di una quantità equivalente di proteine del latte [109].
Questi sono solo due esempi di altre fonti proteiche alternative e di alta qualità che possono essere prodotte su scala commerciale praticabile e più sostenibile e che sembrano avere proprietà anaboliche che non differiscono dalle fonti proteiche convenzionali di origine animale. Chiaramente, verrà svolto maggiore ricerca per stabilire la cinetica di digestione e assorbimento di molte di queste nuove fonti proteiche al fine di valutare le loro proprietà anaboliche post-prandiali. Sembrano esserci molte opportunità per la produzione di fonti proteiche alternative per soddisfare con successo la futura domanda globale di proteine alimentari.
Conclusioni:
Ricapitolando, la tendenza globale verso una alimentazione a base vegetale è sempre più preponderante, più per moda che per logica comprensione. Si ritiene generalmente che l’ingestione di proteine di origine vegetale determini una riduzione delle risposte di sintesi proteica muscolare post-prandiale rispetto all’ingestione di una quantità equivalente di proteine di origine animale. Le proprietà anaboliche minori delle proteine vegetali rispetto a quelle di origine animale sono state attribuite alle differenze nella digestione delle proteine in essi contenute e nella cinetica di assorbimento degli amminoacidi e nella composizione degli stessi. La maggior parte delle proteine vegetali ha un contenuto minore di amminoacidi essenziali e, come abbiamo visto, spesso è carente di uno o più amminoacidi specifici, come Lisina e Metionina. Tuttavia, ci sono grandi differenze nella composizione degli amminoacidi tra varie proteine di origine vegetale o fonti proteiche di origine vegetale. Finora, solo pochi studi hanno confrontato direttamente la risposta della sintesi proteica muscolare in seguito all’ingestione di una fonte proteica di origine vegetale rispetto a quella di origine animale. Le proprietà anabolizzanti inferiori proposte delle proteine di origine vegetale rispetto a quelle di origine animale possono essere compensate da:
- 1) consumando una maggiore quantità di proteine di origine vegetale o fonte di proteine di origine vegetale per compensare la qualità inferiore;
- 2) utilizzare miscele specifiche di proteine di origine vegetale per creare un profilo aminoacidico più equilibrato; o
- 3) fortificare la fonte proteica vegetale di base con l’amminoacido o gli amminoacidi liberi specifici che sono in essa carenti.
Sono necessari studi clinici per valutare le proprietà anaboliche delle varie proteine vegetali e delle loro fonti proteiche e per identificare i fattori che possono o meno compromettere la capacità di stimolare i tassi di sintesi proteica muscolare post-prandiale in vivo nell’uomo. Gli atleti sani e attivi in genere consumano una dieta che fornisce ben oltre ~ 1,5g di proteine per Kg di peso corporeo al giorno . Il consumo di più proteine vegetali, quindi, non dovrebbe necessariamente portare a un apporto proteico non ottimale. Di conseguenza, ci sono ampi dati per dimostrare che l’integrazione proteica con proteine di origine vegetale può (anche) supportare maggiori guadagni di massa muscolare e forza se combinata con un allenamento prolungato di tipo contro-resistenza. In condizioni di basso apporto energetico, come osservato durante interventi dietetici a supporto della perdita di grasso corporeo o in pazienti clinicamente compromessi, si potrebbe ipotizzare che la transizione verso una dieta a base vegetale possa compromettere la stimolazione post-prandiale dei tassi di sintesi proteica muscolare. Di conseguenza, la futura ricerca dovrà stabilire se la transizione verso una dieta più esclusiva a base vegetale sia accompagnata da una transizione verso un maggiore fabbisogno di proteine alimentari.
In base ai dati ad oggi a nostra disposizione, possiamo ipotizzare che, in condizione di dieta vegana, o vegetariana con minima componente di fonti proteiche animali o derivate, la quantità proteica per un bodybuilder che in condizione di dieta onnivora rispondeva positivamente ad una quantità proteica variabile secondo periodo preparatorio (“Bulk” o “Cut”) tra 1,5 e 2,5g/Kg, in caso di shift verso le prima citate condizioni alimentari, debba mantenersi generalmente in range più alti (es. 2g/Kg in “Bulk” e 3g/Kg in “Cut”) onde evitare carenze amminoacidiche per componenti dietetiche e/o per processi di cinetica nell’assorbimento di questi. Ovviamente, si ritengono fattori di “surplus proteico” anche l’inserimento di EAA o di AA specifici per compensare le carenze nutrizionali delle fonti vegetali comunemente consumate.
Gabriel Bellizzi
Riferimenti:
Fonte primaria: The Anabolic Response to Plant-Based Protein Ingestion
- Phillips SM, Tipton KD, Aarsland A, Wolf SE, Wolfe RR. Mixed muscle protein synthesis and breakdown after resistance exercise in humans. Am J Physiol. 1997;273(1 Pt 1):E99-107.
- Biolo G, Tipton KD, Klein S, Wolfe RR. An abundant supply of amino acids enhances the metabolic effect of exercise on muscle protein. Am J Physiol Endocrinol Metab. 1997.
- Gorissen SH, Remond D, van Loon LJ. The muscle protein synthetic response to food ingestion. Meat Sci. 2015.
- Groen BB, Horstman AM, Hamer HM, de Haan M, van Kranenburg J, Bierau J, et al. Post-prandial protein handling: you are what you just ate. PLoS ONE. 2015. Central Google Scholar
- Volpi E, Kobayashi H, Sheffield-Moore M, Mittendorfer B, Wolfe RR. Essential amino acids are primarily responsible for the amino acid stimulation of muscle protein anabolism in healthy elderly adults. Am J Clin Nutr. 2003.
- Moore DR, Tang JE, Burd NA, Rerecich T, Tarnopolsky MA, Phillips SM. Differential stimulation of myofibrillar and sarcoplasmic protein synthesis with protein ingestion at rest and after resistance exercise. J Physiol. 2009. Central Google Scholar
- Tipton KD, Ferrando AA, Phillips SM, Doyle D Jr, Wolfe RR. Postexercise net protein synthesis in human muscle from orally administered amino acids. Am J Physiol. 1999;276(4 Pt 1):E628–34.
- Churchward-Venne TA, Pinckaers PJM, Smeets JSJ, Betz MW, Senden JM, Goessens JPB, et al. Dose-response effects of dietary protein on muscle protein synthesis during recovery from endurance exercise in young men: a double-blind randomized trial. Am J Clin Nutr. 2020.
- 9.Moore DR, Robinson MJ, Fry JL, Tang JE, Glover EI, Wilkinson SB, et al. Ingested protein dose response of muscle and albumin protein synthesis after resistance exercise in young men. Am J Clin Nutr. 2009.
- Robinson MJ, Burd NA, Breen L, Rerecich T, Yang Y, Hector AJ, et al. Dose-dependent responses of myofibrillar protein synthesis with beef ingestion are enhanced with resistance exercise in middle-aged men. Appl Physiol Nutr Metab. 2013.
- Witard OC, Jackman SR, Breen L, Smith K, Selby A, Tipton KD. Myofibrillar muscle protein synthesis rates subsequent to a meal in response to increasing doses of whey protein at rest and after resistance exercise. Am J Clin Nutr. 2014.
- Boirie Y, Dangin M, Gachon P, Vasson M-P, Maubois J-L, Beaufrère B. Slow and fast dietary proteins differently modulate postprandial protein accretion. Proc Natl Acad Sci USA. 1997.
- Tang JE, Moore DR, Kujbida GW, Tarnopolsky MA, Phillips SM. Ingestion of whey hydrolysate, casein, or soy protein isolate: effects on mixed muscle protein synthesis at rest and following resistance exercise in young men. J Appl Physiol (1985). 2009.
- Yang Y, Churchward-Venne TA, Burd NA, Breen L, Tarnopolsky MA, Phillips SM. Myofibrillar protein synthesis following ingestion of soy protein isolate at rest and after resistance exercise in elderly men. Nutr Metab (Lond). 2012.
- Burd NA, Yang Y, Moore DR, Tang JE, Tarnopolsky MA, Phillips SM. Greater stimulation of myofibrillar protein synthesis with ingestion of whey protein isolate v. Micellar casein at rest and after resistance exercise in elderly men. Br J Nutr. 2012.
- Gorissen SH, Horstman AM, Franssen R, Crombag JJ, Langer H, Bierau J, et al. Ingestion of wheat protein increases in vivo muscle protein synthesis rates in healthy older men in a randomized trial. J Nutr. 2016.
- Pennings B, Boirie Y, Senden JM, Gijsen AP, Kuipers H, van Loon LJ. Whey protein stimulates postprandial muscle protein accretion more effectively than do casein and casein hydrolysate in older men. Am J Clin Nutr. 2011.
- Rieu I, Balage M, Sornet C, Giraudet C, Pujos E, Grizard J, et al. Leucine supplementation improves muscle protein synthesis in elderly men independently of hyperaminoacidaemia. J Physiol. 2006.
- Wilkinson DJ, Hossain T, Hill DS, Phillips BE, Crossland H, Williams J, et al. Effects of leucine and its metabolite beta-hydroxy-beta-methylbutyrate on human skeletal muscle protein metabolism. J Physiol. 2013.
- Wall BT, Hamer HM, de Lange A, Kiskini A, Groen BB, Senden JM, et al. Leucine co-ingestion improves post-prandial muscle protein accretion in elderly men. Clin Nutr. 2013.
- Wilkinson DJ, Bukhari SSI, Phillips BE, Limb MC, Cegielski J, Brook MS, et al. Effects of leucine-enriched essential amino acid and whey protein bolus dosing upon skeletal muscle protein synthesis at rest and after exercise in older women. Clin Nutr. 2017.
- Koopman R, Wagenmakers AJM, Manders RJF, Zorenc AHG, Senden JMG, Gorselink M, et al. Combined ingestion of protein and free leucine with carbohydrate increases postexercise muscle protein synthesis in vivo in male subjects. Am J Physiol Endocrinol Metab. 2005.
- Dickinson JM, Gundermann DM, Walker DK, Reidy PT, Borack MS, Drummond MJ, et al. Leucine-enriched amino acid ingestion after resistance exercise prolongs myofibrillar protein synthesis and amino acid transporter expression in older men. J Nutr. 2014. https://doi.org/10.3945/jn.114.198671.Article PubMed PubMed Central Google Scholar
- 24.Atherton PJ, Kumar V, Selby AL, Rankin D, Hildebrandt W, Phillips BE, et al. Enriching a protein drink with leucine augments muscle protein synthesis after resistance exercise in young and older men. Clin Nutr. 2017.
- Trommelen J, Holwerda AM, Pinckaers PJM, Van Loon LJC. Comprehensive assessment of post-prandial protein handling by the application of intrinsically labelled protein in vivo in human subjects. Proc Nutr Soc. 2021.
- Hamarsland H, Aas SN, Nordengen AL, Holte K, Garthe I, Paulsen G, et al. Native whey induces similar post exercise muscle anabolic responses as regular whey, despite greater leucinemia, in elderly individuals. J Nutr Health Aging. 2019.
- Moro T, Brightwell CR, Velarde B, Fry CS, Nakayama K, Sanbongi C, et al. Whey protein hydrolysate increases amino acid uptake, mtorc1 signaling, and protein synthesis in skeletal muscle of healthy young men in a randomized crossover trial. J Nutr. 2019.
- Reitelseder S, Agergaard J, Doessing S, Helmark IC, Lund P, Kristensen NB, et al. Whey and casein labeled with l-[1-13c]leucine and muscle protein synthesis: Effect of resistance exercise and protein ingestion. Am J Physiol Endocrinol Metab. 2011.
- Tang JE, Manolakos JJ, Kujbida GW, Lysecki PJ, Moore DR, Phillips SM. Minimal whey protein with carbohydrate stimulates muscle protein synthesis following resistance exercise in trained young men. Appl Physiol Nutr Metab. 2007.
- Tipton KD, Elliott TA, Cree MG, Wolf SE, Sanford AP, Wolfe RR. Ingestion of casein and whey proteins result in muscle anabolism after resistance exercise. Med Sci Sports Exerc. 2004.
- Churchward-Venne TA, Pinckaers PJM, Smeets JSJ, Peeters WM, Zorenc AH, Schierbeek H, et al. Myofibrillar and mitochondrial protein synthesis rates do not differ in young men following the ingestion of carbohydrate with milk protein, whey, or micellar casein after concurrent resistance- and endurance-type exercise. J Nutr. 2019.
- Burd NA, Gorissen SH, van Vliet S, Snijders T, van Loon LJ. Differences in postprandial protein handling after beef compared with milk ingestion during postexercise recovery: a randomized controlled trial. Am J Clin Nutr. 2015.
- Beals JW, Mackenzie RWA, van Vliet S, Skinner SK, Pagni BA, Niemiro GM, et al. Protein-rich food ingestion stimulates mitochondrial protein synthesis in sedentary young adults of different bmis. J Clin Endocrinol Metab. 2017.
- Beals JW, Sukiennik RA, Nallabelli J, Emmons RS, Van Vliet S, Young JR, et al. Anabolic sensitivity of postprandial muscle protein synthesis to the ingestion of a protein-dense food is reduced in overweight and obese young adults. Am J Clin Nutr. 2016.
- Kamiński M, Skonieczna-Żydecka K, Nowak JK, Stachowska E. Global and local diet popularity rankings, their secular trends, and seasonal variation in google trends data. Nutrition. 2020.
- Wilkinson SB, Tarnopolsky MA, Macdonald MJ, Macdonald JR, Armstrong D, Phillips SM. Consumption of fluid skim milk promotes greater muscle protein accretion after resistance exercise than does consumption of an isonitrogenous and isoenergetic soy-protein beverage. Am J Clin Nutr. 2007.
- Churchward-Venne TA, Pinckaers PJM, Smeets JSJ, Peeters WM, Zorenc AH, Schierbeek H, et al. Myofibrillar and mitochondrial protein synthesis rates do not differ in young men following the ingestion of carbohydrate with whey, soy, or leucine-enriched soy protein after concurrent resistance- and endurance-type exercise. J Nutr. 2019.
- Pinckaers PJM, Kouw IWK, Hendriks FK, Van Kranenburg JMX, De Groot LCPGM, Verdijk LB, et al. No differences in muscle protein synthesis rates following ingestion of wheat protein, milk protein, and their protein blend in healthy, young males. Br J Nutr. 2021.
- Gorissen SH, Crombag JJ, Senden JM, Waterval WH, Bierau J, Verdijk LB, et al. Protein content and amino acid composition of commercially available plant-based protein isolates. Amino Acids. 2018.
- Trommelen J, Tomé D, Van Loon LJC. Gut amino acid absorption in humans: concepts and relevance for postprandial metabolism. Clinical Nutrition Open Science. 2021.
- Kashyap S, Shivakumar N, Varkey A, Duraisamy R, Thomas T, Preston T, et al. Ileal digestibility of intrinsically labeled hen’s egg and meat protein determined with the dual stable isotope tracer method in Indian adults. Am J Clin Nutr. 2018.
- Kashyap S, Varkey A, Shivakumar N, Devi S, Rajashekar BH, Thomas T, et al. True ileal digestibility of legumes determined by dual-isotope tracer method in indian adults. Am J Clin Nutr. 2019.
- Sarwar Gilani G, Wu Xiao C, Cockell KA. Impact of antinutritional factors in food proteins on the digestibility of protein and the bioavailability of amino acids and on protein quality. Br J Nutr. 2012.
- Devi S, Varkey A, Sheshshayee MS, Preston T, Kurpad AV. Measurement of protein digestibility in humans by a dual-tracer method. Am J Clin Nutr. 2018.
- Gausserès N, Mahé S, Benamouzig R, Luengo C, Ferriere F, Rautureau J, et al. [15n]-labeled pea flour protein nitrogen exhibits good ileal digestibility and postprandial retention in humans. J Nutr. 1997.
- FAO/WHO Expert Consultation. Protein quality evaluation. FAO Food Nutr Pap. 1991; (51).
- FAO Expert Consultation. Dietary protein quality evaluation in human nutrition. FAO Food Nutr Pap. 2013; (92).
- West DW, Burd NA, Coffey VG, Baker SK, Burke LM, Hawley JA, et al. Rapid aminoacidemia enhances myofibrillar protein synthesis and anabolic intramuscular signaling responses after resistance exercise. Am J Clin Nutr. 2011.
- Koopman R, Walrand S, Beelen M, Gijsen AP, Kies AK, Boirie Y, et al. Dietary protein digestion and absorption rates and the subsequent postprandial muscle protein synthetic response do not differ between young and elderly men. J Nutr. 2009.
- Gorissen SHM, Trommelen J, Kouw IWK, Holwerda AM, Pennings B, Groen BBL, et al. Protein type, protein dose, and age modulate dietary protein digestion and phenylalanine absorption kinetics and plasma phenylalanine availability in humans. J Nutr. 2020.
- Chan AH, D’Souza RF, Beals JW, Zeng N, Prodhan U, Fanning AC, et al. The degree of aminoacidemia after dairy protein ingestion does not modulate the postexercise anabolic response in young men: A randomized controlled trial. J Nutr. 2019.
- Reitelseder S, Agergaard J, Doessing S, Helmark IC, Schjerling P, Van Hall G, et al. Positive muscle protein net balance and differential regulation of atrogene expression after resistance exercise and milk protein supplementation. Eur J Nutr. 2014.
- Brennan JL, Keerati-U-Rai M, Yin H, Daoust J, Nonnotte E, Quinquis L, et al. Differential responses of blood essential amino acid levels following ingestion of high-quality plant-based protein blends compared to whey protein—a double-blind randomized, cross-over, clinical trial. Nutrients. 2019.
- Liu J, Klebach M, Visser M, Hofman Z. Amino acid availability of a dairy and vegetable protein blend compared to single casein, whey, soy, and pea proteins: A double-blind, cross-over trial. Nutrients. 2019.
- Tipton K. Nonessential amino acids are not necessary to stimulate net muscle protein synthesis in healthy volunteers. J Nutr Biochem. 1999.
- Cuthbertson D, Smith K, Babraj J, Leese G, Waddell T, Atherton P, et al. Anabolic signaling deficits underlie amino acid resistance of wasting, aging muscle. FASEB J. 2005.
- van Vliet S, Burd NA, van Loon LJ. The skeletal muscle anabolic response to plant- versus animal-based protein consumption. J Nutr. 2015.
- FAO/WHO/UNU expert consultation. Protein and amino acid requirements in human nutrition. WHO Technical Report Series. 2007;935:1–265.Google Scholar
- Laplante M, David M. Mtor signaling in growth control and disease. Cell. 2012.
- Saxton RA, Knockenhauer KE, Wolfson RL, Chantranupong L, Pacold ME, Wang T, et al. Structural basis for leucine sensing by the sestrin2-mtorc1 pathway. Science. 2016.
- Wolfson RL, Chantranupong L, Saxton RA, Shen K, Scaria SM, Cantor JR, et al. Sestrin2 is a leucine sensor for the mtorc1 pathway. Science. 2016.
- Gorissen SH, Horstman AM, Franssen R, Kouw IW, Wall BT, Burd NA, et al. Habituation to low or high protein intake does not modulate basal or postprandial muscle protein synthesis rates: a randomized trial. Am J Clin Nutr. 2017.
- Mitchell C, McGregor R, D’Souza R, Thorstensen E, Markworth J, Fanning A, et al. Consumption of milk protein or whey protein results in a similar increase in muscle protein synthesis in middle aged men. Nutrients. 2015.
- Yang Y, Breen L, Burd NA, Hector AJ, Churchward-Venne TA, Josse AR, et al. Resistance exercise enhances myofibrillar protein synthesis with graded intakes of whey protein in older men. Br J Nutr. 2012.
- Fuchs CJ, Hermans WJH, Holwerda AM, Smeets JSJ, Senden JM, van Kranenburg J, et al. Branched-chain amino acid and branched-chain ketoacid ingestion increases muscle protein synthesis rates in vivo in older adults: a double-blind, randomized trial. Am J Clin Nutr. 2019.
- Wall BT, Gorissen SH, Pennings B, Koopman R, Groen BB, Verdijk LB, et al. Aging is accompanied by a blunted muscle protein synthetic response to protein ingestion. PLoS ONE. 2015.
- Burd NA, Gorissen SH, van Loon LJ. Anabolic resistance of muscle protein synthesis with aging. Exerc Sport Sci Rev. 2013. https://doi.org/10.1097/JES.0b013e318292f3d5.Article PubMed Google Scholar
- Koopman R, Crombach N, Gijsen AP, Walrand S, Fauquant J, Kies AK, et al. Ingestion of a protein hydrolysate is accompanied by an accelerated in vivo digestion and absorption rate when compared with its intact protein. 2009. Am J Clin Nutr.
- Food Balance Sheets. Food and agriculture organization of the United Nations statistics division 2013.
- Borack MS, Reidy PT, Husaini SH, Markofski MM, Deer RR, Richison AB, et al. Soy-dairy protein blend or whey protein isolate ingestion induces similar postexercise muscle mechanistic target of rapamycin complex 1 signaling and protein synthesis responses in older men. J Nutr. 2016.
- Reidy PT, Walker DK, Dickinson JM, Gundermann DM, Drummond MJ, Timmerman KL, et al. Soy-dairy protein blend and whey protein ingestion after resistance exercise increases amino acid transport and transporter expression in human skeletal muscle. J Appl Physiol (1985). 2014.
- Reidy PT, Walker DK, Dickinson JM, Gundermann DM, Drummond MJ, Timmerman KL, et al. Protein blend ingestion following resistance exercise promotes human muscle protein synthesis. J Nutr. 2013.
- Churchward-Venne TA, Breen L, Phillips SM. Alterations in human muscle protein metabolism with aging: protein and exercise as countermeasures to offset sarcopenia. BioFactors. 2014.
- Katsanos CS, Kobayashi H, Sheffield-Moore M, Aarsland A, Wolfe RR. A high proportion of leucine is required for optimal stimulation of the rate of muscle protein synthesis by essential amino acids in the elderly. Am J Physiol Endocrinol Metab. 2006.
- Norton LE, Wilson GJ, Layman DK, Moulton CJ, Garlick PJ. Leucine content of dietary proteins is a determinant of postprandial skeletal muscle protein synthesis in adult rats. Nutr Metab (Lond). 2012.
- Trommelen J, Betz MW, Van Loon LJC. The muscle protein synthetic response to meal ingestion following resistance-type exercise. Sports Med. 2019.
- Gorissen SH, Burd NA, Hamer HM, Gijsen AP, Groen BB, van Loon LJ. Carbohydrate coingestion delays dietary protein digestion and absorption but does not modulate postprandial muscle protein accretion. J Clin Endocrinol Metab. 2014.
- Hamer HM, Wall BT, Kiskini A, De Lange A, Groen BB, Bakker JA, et al. Carbohydrate co-ingestion with protein does not further augment post-prandial muscle protein accretion in older men. Nutr Metab (Lond). 2013.
- Koopman R, Beelen M, Stellingwerff T, Pennings B, Saris WHM, Kies AK, et al. Coingestion of carbohydrate with protein does not further augment postexercise muscle protein synthesis. Am J Physiol Endocrinol Metab. 2007.
- Gorissen SHM, Burd NA, Kramer IF, van Kranenburg J, Gijsen AP, Rooyackers O, et al. Co-ingesting milk fat with micellar casein does not affect postprandial protein handling in healthy older men. Clin Nutr. 2017.
- Trommelen J, Groen BBL, Hamer HM, De Groot LCPGM, Van Loon LJC. Mechanisms in endocrinology European journal of endocrinology of the European federation of endocrine societies: exogenous insulin does not increase muscle protein synthesis rate when administered systemically: a systematic review. Eur J Endocrinol. 2015.
- Glynn EL, Fry CS, Timmerman KL, Drummond MJ, Volpi E, Rasmussen BB. Addition of carbohydrate or alanine to an essential amino acid mixture does not enhance human skeletal muscle protein anabolism. J Nutr. 2013.
- Staples AW, Burd NA, West DWD, Currie KD, Atherton PJ, Moore DR, et al. Carbohydrate does not augment exercise-induced protein accretion versus protein alone. Med Sci Sports Exerc. 2011.
- Glynn EL, Fry CS, Drummond MJ, Dreyer HC, Dhanani S, Volpi E, et al. Muscle protein breakdown has a minor role in the protein anabolic response to essential amino acid and carbohydrate intake following resistance exercise. Am J Physiol Regul Integr Comp Physiol. 2010.
- van Vliet S, Shy EL, Abou Sawan S, Beals JW, West DW, Skinner SK, et al. Consumption of whole eggs promotes greater stimulation of postexercise muscle protein synthesis than consumption of isonitrogenous amounts of egg whites in young men. Am J Clin Nutr. 2017.
- Kim I-Y, Shin Y-A, Schutzler SE, Azhar G, Wolfe RR, Ferrando AA. Quality of meal protein determines anabolic response in older adults. Clin Nutr. 2018.
- Evenepoel P, Geypens B, Luypaerts A, Hiele M, Ghoos Y, Rutgeerts P. Digestibility of cooked and raw egg protein in humans as assessed by stable isotope techniques. J Nutr. 1998.
- Buffière C, Gaudichon C, Hafnaoui N, Migné C, Scislowsky V, Khodorova N, et al. In the elderly, meat protein assimilation from rare meat is lower than that from meat that is well done. Am J Clin Nutr. 2017.
- Pennings B, Groen BB, Van Dijk J-W, De Lange A, Kiskini A, Kuklinski M, et al. Minced beef is more rapidly digested and absorbed than beef steak, resulting in greater postprandial protein retention in older men. Am J Clin Nutr. 2013.
- Rémond D, Machebeuf M, Yven C, Buffière C, Mioche L, Mosoni L, et al. Postprandial whole-body protein metabolism after a meat meal is influenced by chewing efficiency in elderly subjects. Am J Clin Nutr. 2007.
- Cermak NM, Res PT, de Groot LC, Saris WH, van Loon LJ. Protein supplementation augments the adaptive response of skeletal muscle to resistance-type exercise training: a meta-analysis. Am J Clin Nutr. 2012.
- Morton RW, Murphy KT, McKellar SR, Schoenfeld BJ, Henselmans M, Helms E, et al. A systematic review, meta-analysis and meta-regression of the effect of protein supplementation on resistance training-induced gains in muscle mass and strength in healthy adults. Br J Sports Med. 2018.
- Hartman JW, Tang JE, Wilkinson SB, Tarnopolsky MA, Lawrence RL, Fullerton AV, et al. Consumption of fat-free fluid milk after resistance exercise promotes greater lean mass accretion than does consumption of soy or carbohydrate in young, novice, male weightlifters. Am J Clin Nutr. 2007.
- Lynch HM, Buman MP, Dickinson JM, Ransdell LB, Johnston CS, Wharton CM. No significant differences in muscle growth and strength development when consuming soy and whey protein supplements matched for leucine following a 12 week resistance training program in men and women: a randomized trial. Int J Environ Res Public Health. 2020.
- Mobley C, Haun C, Roberson P, Mumford P, Romero M, Kephart W, et al. Effects of whey, soy or leucine supplementation with 12 weeks of resistance training on strength, body composition, and skeletal muscle and adipose tissue histological attributes in college-aged males. Nutrients. 2017.
- Thomson RL, Brinkworth GD, Noakes M, Buckley JD. Muscle strength gains during resistance exercise training are attenuated with soy compared with dairy or usual protein intake in older adults: A randomized controlled trial. Clin Nutr. 2016.
- Banaszek A, Townsend JR, Bender D, Vantrease WC, Marshall AC, Johnson KD. The effects of whey vs. Pea protein on physical adaptations following 8-weeks of high-intensity functional training (hift): a pilot study. Sports. 2019.
- Joy JM, Lowery RP, Wilson JM, Purpura M, De Souza EO, Wilson SM, et al. The effects of 8 weeks of whey or rice protein supplementation on body composition and exercise performance. Nutr J. 2013.
- Oikawa SY, Bahniwal R, Holloway TM, Lim C, McLeod JC, McGlory C, et al. Potato protein isolate stimulates muscle protein synthesis at rest and with resistance exercise in young women. Nutrients. 2020.
- Lim MT, Pan BJ, Toh DWK, Sutanto CN, Kim JE. Animal protein versus plant protein in supporting lean mass and muscle strength: a systematic review and meta-analysis of randomized controlled trials. Nutrients. 2021.
- 101.Hevia-Larraín V, Gualano B, Longobardi I, Gil S, Fernandes AL, Costa LAR, et al. High-protein plant-based diet versus a protein-matched omnivorous diet to support resistance training adaptations: a comparison between habitual vegans and omnivores. Sports Med. 2021.
- Gillen JB, Trommelen J, Wardenaar FC, Brinkmans NYJ, Versteegen JJ, Jonvik KL, et al. Dietary protein intake and distribution patterns of well-trained Dutch athletes. Int J Sport Nutr Exerc Metab. 2017.
- Monteyne AJ, Coelho MOC, Porter C, Abdelrahman DR, Jameson TSO, Jackman SR, et al. Mycoprotein ingestion stimulates protein synthesis rates to a greater extent than milk protein in rested and exercised skeletal muscle of healthy young men: a randomized controlled trial. Am J Clin Nutr. 2020.
- Monteyne AJ, Dunlop MV, Machin DJ, Coelho MOC, Pavis GF, Porter C, et al. A mycoprotein-based high-protein vegan diet supports equivalent daily myofibrillar protein synthesis rates compared with an isonitrogenous omnivorous diet in older adults: a randomised controlled trial. Br J Nutr. 2020.
- Coelho MOC, Monteyne AJ, Dunlop MV, Harris HC, Morrison DJ, Stephens FB, et al. Mycoprotein as a possible alternative source of dietary protein to support muscle and metabolic health. Nutr Rev. 2020.
- Dunlop MV, Kilroe SP, Bowtell JL, Finnigan TJA, Salmon DL, Wall BT. Mycoprotein represents a bioavailable and insulinotropic non-animal-derived dietary protein source: A dose–response study. Br J Nutr. 2017.
- Churchward-Venne TA, Pinckaers PJM, van Loon JJA, van Loon LJC. Consideration of insects as a source of dietary protein for human consumption. Nutr Rev. 2017.
- van Huis A, Van Itterbeeck J, Klunder H, Mertens E, Halloran A, Muir G, et al. Edible insects: Future prospects for food and feed security. London: Food and Agriculture Organization of the United Nations; 2013.
- Hermans WJH, Senden JM, Churchward-Venne TA, Paulussen KJM, Fuchs CJ, Smeets JSJ, et al. Insects are a viable protein source for human consumption: From insect protein digestion to post-prandial muscle protein synthesis in vivo in humans: a double- blind randomized trial. Am J Clin Nutr. 2021.

Ma perché devo tenermi la formula chimica mentre leggo? A che pro? Mah!?
Si legge con grave difficoltà!
"Mi piace""Mi piace"
Punto primo sono nucleotidi … e non formule chimiche … punto secondo, usi il PC …
"Mi piace""Mi piace"