Introduzione all’argomento:

Con l’attuale pandemia di COVID-19 il web è letteralmente invaso da una pestilenza parallela che rischia di far diventare quella virale ancor peggiore di come la mala gestione statale l’ha già fatta diventare. Chi, in questi giorni di isteria collettiva, non si è imbattuto in uno o più post dove l’autore millantava prodigiosi effetti protettivi dati dalla somministrazione di mega dosi di Vitamina C, A e D? Postando in allegato tanto di letteratura scientifica? Ben pochi immagino. Purtroppo, sono molto pochi coloro che si prendono l’onere di approfondire tali studi citati e sono ancora meno coloro che sono in grado di capirli e contestualizzarli. Chi scrive questi post è per lo più sprovvisto della più elementare conoscenza di base in virologia per poter trattare l’argomento in modo non solo esaustivo ma anche, e soprattutto, credibile. Ed ecco il motivo che mi spinge ora a scrivere il presente articolo: per spiegare in modo più fruibile possibile cos’è un virus e fin dove la ricerca ci può dare, ad oggi, direttive veramente utili per prevenire e trattare una contaminazione virale, smontando le “perle guresche” che rischiano di far sottovalutare un problema lievitato a causa, per l’appunto, di una sottovalutazione eccessiva fatta di ignoranza all’italiana e paragoni impropri.
Virus: loro scoperta e caratteristiche

Un Virus (la parola “virus” deriva dalla parola latina vīrus, che significa “tossina” o “veleno”) è un microrganismo acellulare con caratteristiche di parassita obbligato, in quanto si replica esclusivamente all’interno delle cellule di altri organismi. Infatti, i Virus possono infettare tutti i tipi di forme di vita, dagli animali, alle piante, ai microrganismi (compresi batteri e archeobatteri)[1] e anche altri Virus.[2][3]
Nel 1892 Dmitri Ivanovsky descrisse in un articolo un agente patogeno non batterico in grado di infettare le piante di tabacco, da cui in seguito, sei anni più tardi, Martinus Beijerinck scoprì il Virus del mosaico del tabacco nel 1898.[4] Già tempo prima, Louis Pasteur riuscì a determinare l’agente eziologico per la rabbia e previde l’esistenza di un patogeno troppo piccolo per essere rilevato utilizzando un microscopio.[5] Nel 1884, il microbiologo francese Charles Chamberland inventò un filtro (conosciuto oggi come il filtro Chamberland o filtro di Chamberland-Pasteur) con pori più piccoli dei batteri. Così, egli poteva passare una soluzione contenente batteri attraverso esso e quindi rimuoverli completamente dalla soluzione.[6]

Gli esperimenti di Dmitri Ivanovsky hanno dimostrato che estratti di foglie da piante di tabacco schiacciate e infettate rimangono infettive dopo la filtrazione. Ivanovsky suggerì che l’infezione poteva essere causata da una tossina prodotta da batteri, ma non approfondì la questione.[7] Al momento si pensava che tutti gli agenti infettivi potessero essere trattenuti dai filtri e coltivati su un terreno nutritivo.[8] Nel 1898, il microbiologo olandese Martinus Beijerinck ripeté gli esperimenti e si convinse che la soluzione filtrata conteneva una nuova forma di agente infettivo.[9] Egli osservò che questo agente si moltiplicava solo nelle cellule che si stavano dividendo, ma poiché i suoi esperimenti non mostrarono che fosse fatto di particelle, lo chiamò contagium vivum fluidum (solubile germe di vita), e reintrodusse la parola virus.[7] Beijerinck sostenne che i virus fossero liquidi in natura, una teoria più tardi screditata da Wendell Meredith Stanley, che dimostrò che erano delle particelle.[7] Nello stesso anno Friedrich Loeffler e Paolo Frosch isolarono il primo virus animale, l’agente dell’afta epizootica (aphthovirus), attraverso un filtro simile.[10]
Nel XX secolo, il batteriologo inglese Frederick Twort scoprì un gruppo di virus capaci di infettare i batteri, oggi chiamati batteriofagi[8] (o comunemente fagi) e il microbiologo franco-canadese Félix d’Herelle descrisse un virus che, quando aggiunto a batteri su agar, produrrebbe aree di batteri morti. I fagi furono considerati come un potenziale trattamento per alcune malattie come il tifo e il colera, ma tale idea fu messa da parte grazie all’introduzione della penicillina. Lo studio di fagi, tuttavia, ha permesso di capire alcuni aspetti dell’espressione genica e un meccanismo utile per introdurre geni estranei nei batteri.
Alla fine del XIX secolo, i virus vennero classificati secondo la loro infettività, la loro capacità di essere filtrati e i requisiti per i loro ospiti viventi. Inizialmente i virus vennero coltivati solo nelle piante e negli animali. Nel 1906, Ross Granville Harrison introdusse un metodo per la coltivazione nella linfa, e, nel 1913, E. Steinhardt, C. Israeli, and R. A. Lambert utilizzarono questo metodo per allevare i virus destinati a diventare vaccini in frammenti di tessuto corneale di una cavia.[11] Nel 1928, HB Maitland e MC Maitland fecero moltiplicare i virus vaccino in sospensioni di reni di galline. Il loro metodo incominciò a essere ampiamente adottato a partire dal 1950, quando il poliovirus venne coltivato su larga scala per la produzione del vaccino antipoliomielite.[12]

Nel 1931 il patologo statunitense Ernest William Goodpasture fece crescere il virus dell’influenza e molti altri virus nelle uova di galline fecondate.[13-23] Nel 1949, John Franklin Enders, Thomas Weller e Frederick Robbins fecero crescere il virus della poliomielite in cellule in coltura su embrioni umani, il primo virus a essere coltivato senza l’uso di tessuti animali solidi o uova. Questo lavoro permise a Jonas Salk di realizzare un efficace vaccino antipolio.[14-24]
Nel 1935, dopo l’invenzione del microscopio elettronico evvenuta nel 1931 grazie al lavoro degli ingegneri tedeschi Ernst Ruska e Max Knoll [15], il biochimico e virologo americano Wendell Meredith Stanley analizzò il virus del mosaico del tabacco e dimostrò che era per la maggior parte costituito da proteine.[16] Poco tempo dopo, fu possibile separare in questo virus le proteine dall’RNA.[17] Le prime immagini a raggi X di diffrazione del virus cristallizzato, furono ottenute da Bernal e Fankuchen nel 1941. Sulla base delle loro foto, Rosalind Franklin scoprì, nel 1955, la struttura completa del virus.[18] Nello stesso anno, Heinz Fraenkel-Conrat e Robley Williams dimostrarono che il virus del mosaico del tabacco purificato e il suo rivestimento proteico sono in grado di assemblare da soli dei virus funzionali, suggerendo che questo semplice meccanismo è probabilmente stato il mezzo attraverso cui i virus vengono composti all’interno delle loro cellule ospiti.[19]

La seconda metà del XX secolo è stato un periodo d’oro per lo studio dei virus, e buona parte delle circa 5000 specie è stata scoperta nel corso di questi anni.[20] Nel 1957 fu scoperto l’arteriviridae equino, la causa della diarrea virale bovina (una pestivirus). Nel 1963 Baruch Blumberg scoprì il virus dell’epatite B,[21] e nel 1965, Howard Temin descrisse il primo retrovirus. La trascrittasi inversa, l’enzima che i retrovirus utilizzano per fare copie di DNA del loro RNA, è stata descritta per la prima volta nel 1970, indipendentemente da Howard Martin Temin e da David Baltimore.[22] Nel 1983, il gruppo guidato da Luc Montagnier, presso l’Istituto Pasteur in Francia, isolò per primo il retrovirus oggi chiamato HIV.[23]
Come precedentemente accennato, i virus sono tutti parassiti endocellulari obbligati. All’esterno delle cellule ospiti sono costituiti da un virione, formato da una capsula proteica (detta capside) contenente l’acido nucleico. I virus degli Eucarioti possono possedere anche una membrana che avvolge il capside detta peplos o pericapside. Talvolta tra il capside e il peplos presentano un ulteriore strato proteico che prende il nome di tegumento. I virioni non possiedono metabolismo: vengono quindi trasportati passivamente finché non trovano una cellula da infettare. L’infezione di una cellula ospite richiede il legame con proteine specifiche di membrana.
Nelle cellule infettate i virus perdono la loro individualità strutturale: consistono negli acidi nucleici e nei loro prodotti che assumono il controllo di parte dell’attività biosintetica cellulare al fine di produrre nuovi virioni.
In alternativa, alcuni virus possono inserire fisicamente il loro genoma in quello dell’ospite in modo che sia replicato insieme con esso. Il genoma virale inserito in quello dell’ospite, detto provirus, riprende la sua individualità e produce nuovi virioni in caso di danneggiamento della cellula ospite.

Attenzione: sebbene virus e batteri possano provocare malattie, sono assai diversi tra loro! Sebbene abbiano alcune caratteristiche comuni, come la capacità di trasmettersi da un individuo a un altro, e possano indurre, talvolta, patologie simili, sono molto diversi tra loro. I batteri sono organismi costituiti da una sola cellula (unicellulari) procarioti (ossia privi di nucleo cellulare), ma assimilabili a organismi viventi completi, poiché sono dotati di tutte le strutture e gli enzimi necessari per espletare le funzioni metaboliche fondamentali, potendo quindi vivere in modo indipendente e riprodursi autonomamente, per divisione cellulare. I virus sono, mediamente, 100 volte più piccoli dei batteri (al punto da risultare invisibili al microscopio ottico), e non possiedono né una struttura cellulare completa, né tutti gli enzimi necessari per la sopravvivenza e la replicazione del proprio acido nucleico, che può essere costituito da DNA o RNA (in questo secondo caso vengono chiamati “retrovirus” e l’esponente più noto del gruppo è l’HIV). Inoltre, i virus non posseggono ribosomi, che sono gli organelli cellulari indispensabili per produrre tutte le proteine esistenti in natura, quindi anche quelle che formano il capside virale, corrispondente all’involucro del virus. Ciò rende i virus incapaci di riprodursi autonomamente e fa sì che, per potersi moltiplicare e causare infezioni, debbano entrare in una cellula ospite “completa” (che può essere una cellula animale o vegetale oppure una cellula batterica) e sfruttarne le strutture e gli enzimi di cui sono carenti. I virus che infettano e sfruttano cellule batteriche sono chiamati “batteriofagi”.
Vorrei rammentare, quindi, che gli antibiotici non hanno alcun effetto sui virus!
L’origine dei virus non è tuttavia chiara anche perché non formano fossili nel senso classico del termine; tecniche molecolari sono state utilizzate per confrontare il DNA o l’RNA dei virus e si sono dimostrate molto utili per indagare su come si potevano presentare in principio. [24] Inoltre, il materiale genetico virale può occasionalmente passare nella linea germinale degli organismi ospitanti, per cui i discendenti ospitanti avranno il virus integrato nel proprio genoma. Ciò fornisce una preziosa fonte di informazioni per i virologi per poter risalire ai “virus primari”. Attualmente, vi sono tre ipotesi principali che mirano a spiegare le origini dei virus:[25][26]
Ipotesi regressiva
Questa teoria presenta due diverse varianti espositive. La prima, prettamente evoluzionista, afferma che i virus potrebbero essere stati una volta delle piccole cellule parassitarie di cellule più grandi. Nel corso del tempo, i geni non richiesti dalla loro natura parassitaria sono andati persi. La seconda, molto simile alla prima, ricerca la variazione genetica sotto la luce dell’entropia, ovvero della perdita di informazioni geniche dei sistemi virali primari, ed è la più accreditabile rispetto alla precedente versione sebbene si discosti di poche essenziali puntualizzazioni. Comunque sia, i batteri rickettsia e clamidia sono le cellule che, come i virus, sono in grado di riprodursi solo all’interno di cellule ospiti viventi. Essi prestano sostegno a questa ipotesi per il fatto che la loro dipendenza da parassitismo probabilmente causò loro la perdita dei geni, oppure la perdita di informazioni geniche ne è stato l’imput, che gli potevano permettere di sopravvivere al di fuori di una cellula. Questa ipotesi è chiamata anche di degenerazione[27][28] o di riduzione.[29]
Ipotesi dell’origine cellulare
Questa, talvolta chiamata ipotesi del vagabondaggio[27][30] o ipotesi di fuga,[29] consiste nel credere, e sottolineo “credere”, che alcuni virus si siano evoluti da frammenti di DNA o RNA che sono “sfuggiti” da geni di un organismo più grande. Il DNA fuggito avrebbe potuto provenire da plasmidi (frammenti di DNA che possono muoversi tra le cellule) o trasposoni/retrotrasposoni (molecole di DNA che si replicano e si muovono da diverse posizioni all’interno dei geni della cellula).[31] Una volta chiamati “geni che saltano”, i trasposoni sono esempi di elementi genetici mobili che potrebbero essere l’origine di alcuni virus perché hanno delle sequenze analoghe. Essi sono stati scoperti nel mais da Barbara McClintock nel 1950.[32]
Ipotesi della coevoluzione
La teoria più eccentrica e meno scientifica (nel senso più stretto del termine) è senz’altro quella chiamata anche ipotesi del primo virus[29] e propone che i virus si siano evoluti da molecole complesse di proteine e acidi nucleici contemporaneamente alla prima apparizione sulla Terra della cellula e sarebbero rimasti dipendenti dalla vita cellulare per miliardi di anni. I viroidi sono molecole di RNA che non sono classificati come virus poiché mancano di un rivestimento proteico. Tuttavia, essi hanno caratteristiche che sono comuni a diversi virus e sono spesso chiamati agenti subvirali.[33] I viroidi sono importanti patogeni delle piante.[34] Loro non codificano proteine ma interagiscono con la cellula ospite e utilizzano le sue strutture per replicarsi.[35] Il virus dell’epatite delta degli esseri umani ha un genoma RNA simile ai viroidi, ma è dotato di un rivestimento proteico derivato dal virus dell’epatite B e non può produrne uno suo. È, quindi, un virus difettoso. Sebbene il genoma del virus dell’epatite delta possa replicarsi indipendentemente all’interno di una cellula ospite, esso richiede la presenza del virus dell’epatite B che gli fornisca un rivestimento proteico in modo che possa essere trasmesso alle nuove cellule.[36] In modo analogo, il virofago Sputnik dipende dai mimivirus, e infetta il protozoo Acanthamoeba castellanii.[37] Questi virus, che dipendono dalla presenza di altre specie di virus nella cellula ospite, sono chiamati “satelliti” e possono rappresentare intermedi evolutivi dei viroidi e dei virus.[38][39]
In passato, vi sono stati problemi con tutte queste ipotesi: l’ipotesi regressiva non spiega il motivo per cui anche il più piccolo dei parassiti cellulari non assomigli ai virus in alcun modo. L’ipotesi della fuga non spiega la presenza di capsidi complessi e altre strutture di particelle virali. L’ipotesi del primo virus viola la stessa definizione di virus che richiede una cellula ospite.[29] I virus sono ora riconosciuti come molto antichi e con una data d’origine antecedente alla divergenza della vita nei tre domini.[40] Questa scoperta ha portato i virologi moderni a riconsiderare e rivalutare le tre ipotesi classiche.[40-51]
L’evidenza di un mondo ancestrale delle cellule RNA[41] e le analisi al computer di sequenze di DNA virale stanno fornendo una migliore comprensione delle relazioni evolutive tra i diversi virus e potranno aiutare a identificare gli antenati dei virus moderni. Fino a oggi, queste analisi non hanno potuto dimostrare quale di queste ipotesi sia più corretta.[41] Tuttavia, sembra improbabile che tutti i virus attualmente conosciuti abbiano un antenato comune e probabilmente molti virus sono nati in passato con diversi meccanismi.[42]
Qualunque sia la loro origine primordiale, vi è una divergenza di opinioni sulla questione se i virus siano una forma di vita o strutture organiche che interagiscono con gli organismi viventi. Nonostante possiedano geni, essi non hanno una struttura cellulare, aspetto che viene spesso visto, da un certo filone di ricercatori, come l’unità base della vita. I virus non hanno nemmeno un proprio metabolismo e necessitano della cellula ospite per realizzare nuovi prodotti. Essi, pertanto, non possono naturalmente riprodursi al di fuori di una cellula ospite.[43] Tuttavia specie batteriche come la rickettsia e la clamidia sono considerati organismi viventi nonostante abbiano la stessa limitazione.[44][45] Forme di vita accettate come tali utilizzano la divisione cellulare per riprodursi, mentre i virus si assemblano spontaneamente all’interno delle cellule. Si differenziano dalla crescita autonoma dei cristalli per il fatto che ereditano mutazioni genetiche e sono soggetti alla selezione naturale. Sebbene la cerchia degli evoluzionisti abbia affermato che tali caratteristiche di “auto-assemblaggio” dei virus nelle cellule ospiti comporta implicazioni per lo studio dell’origine della vita, in quanto, secondo loro ipotesi, conferisce ulteriore credito all’ipotesi che la vita possa aver avuto origine da molecole organiche auto-assemblate.[1] In realtà, tale caratteristica continua ad avvalorare il fenomeno entropico dei geni e spinge ad ipotizzare che i virus siano “mezzi di controllo” specifici interagenti con le forme di vita e soggetti a degenerazione sistemica del genoma con la conseguente comparsa di forme virali mutate e potenzialmente dannose in alcuni casi e a diversa entità.
I virus mostrano una grande diversità di forme e dimensioni, chiamate morfologie. In generale, i virus sono molto più piccoli dei batteri. La maggior parte dei virus che sono stati studiati hanno un diametro tra 20 e 300 nanometri. Alcuni filovirus arrivano fino a una lunghezza totale a 1400 nm, ma il loro diametro è solo di circa 80 nm.[46] Per questo motivo maggior parte dei virus non possono essere visti con un microscopio ottico e dunque per visualizzare i virioni è necessario utilizzare il microscopio elettronico.[47]
Una particella virale completa, nota come un virione, è costituita da acido nucleico circondato da un rivestimento protettivo formato da proteine chiamato capside. Questo è realizzato da subunità proteiche identiche chiamati capsomeri.[48] I virus possono avere una “sacca” lipidica derivata dalla membrana della cellula ospite. Il capside è costituito da proteine codificate dal genoma virale e la sua forma serve come base per la distinzione morfologica.[49][50] Perché le subunità proteiche virali codificate si possano auto-assemblare per formare il capside, in generale si richiede la presenza del genoma virale. Virus complessi codificano proteine che aiutano la costruzione del loro capside. Le proteine associate all’acido nucleico sono note come nucleoproteine e l’associazione di proteine del capside virale con l’acido nucleico virale è chiamato nucleocapside. Il capside e l’intera struttura del virus possono essere fisicamente sondati attraverso il microscopio a forza atomica.[51][52]
In generale, i virus si possono distinguere in quattro tipologie morfologiche:
Elicoidale

Questi virus sono composti da un unico tipo di capsomero accatastato intorno a un asse centrale, formando una struttura elicoidale, che può avere una cavità centrale. Questa disposizione comporta virioni a forma di bastoncello o filamentosi: questi possono essere brevi ed estremamente rigidi o lunghi e molto flessibili. Il materiale genetico, in generale, RNA a singolo filamento, ma in alcuni casi anche DNA a singolo filamento, è vincolato nell’elica proteica dalle interazioni tra l’acido nucleico caricato negativamente e le cariche positive poste sulla proteina. In generale, la lunghezza di un capside elicoidale è correlato alla lunghezza dell’acido nucleico in esso contenuto e il diametro dipende dalla dimensione e disposizione dei capsomeri. Il virus del mosaico del tabacco è un esempio ben analizzato di virus elicoidale.[53]
Icosaedrica

La maggior parte dei virus che colpiscono gli animali sono di morfologia icosaedrica o quasi sferica con simmetria icosaedrica. Un icosaedro regolare è un modo ottimale per formare un guscio chiuso da sub-unità identiche. Il numero minimo di capsomeri identici richiesto è dodici, ciascuno composto da cinque subunità identiche. Molti virus, come il rotavirus, possiedono più di dodici capsomeri e sembrano sferici pur mantenendo questa simmetria. I capsomeri agli apici sono circondati da altri cinque capsomeri e sono chiamati pentoni. I capsomeri sulle facce triangolari sono circondati da altri sei e sono chiamati esoni.[54] Gli esoni sono essenzialmente pianeggianti, mentre i pentoni che formano i 12 vertici sono curvilinei. La stessa proteina può agire come subunità sia nei pentoni sia negli esoni o possono essere composti da proteine differenti.
Ovoidale

Si tratta di una forma a icosaedro allungata di circa cinque volte lungo l’asse ed è tipica delle teste dei batteriofagi. Questa struttura è composta da un cilindro con una capsula a entrambe le estremità.[55]
Involucro

Alcune specie di virus si avvolgono in una forma modificata di una delle membrane cellulari, o la membrana esterna che circonda la cellula ospite infettata o le membrane interne come la membrana nucleare o il reticolo endoplasmatico, ottenendo così un doppio strato lipidico esterno noto come pericapside o involucro virale. Questa membrana è costellata da proteine codificate dal genoma virale e dal genoma ospite; la stessa membrana lipidica e qualsiasi carboidrato presente provengono interamente dall’ospite. Il virus influenzale e quello dell’HIV usano questa strategia. L’infettività della maggior parte di questi virus dipende dal loro involucro.[56]
Complesso

Questi virus possiedono un capside che non è né puramente elicoidale né puramente icosaedrico e che può possedere strutture extra come code proteiche o una parete esterna complessa. Alcuni batteriofagi, come, il batteriofago t4 hanno una struttura complessa costituita da una testa icosaedrica associata a una coda elicoidale, che può avere una piastra di base esagonale con una coda proteica sporgente. Tale struttura a coda agisce come una siringa molecolare, attaccandosi al batterio ospite e per poi iniettare il genoma virale nella cellula.[57]
Il genoma virale è associato con le proteine all’interno di una struttura centrale del disco, conosciuta come nucleoide. Il nucleoide è circondato da una membrana e due corpi laterali dalla funzione ad oggi sconosciuta. Il virus ha un involucro esterno con uno strato molto spesso di proteine costellato sulla sua superficie. L’intero virione è leggermente pleimorfico, dalla forma ovoidale.[58]
Un’enorme varietà di strutture genomiche possono essere riscontrate tra le specie virali; come gruppo, essi contengono una diversità genomica strutturale maggiore rispetto alle piante, agli animali, agli archeobatteri o ai batteri. Vi sono milioni di diversi tipi di virus,[6] anche se solo circa 5.000 tipi sono stati descritti in dettaglio.[5] A settembre 2015, il database NCBI dei genoma dei virus contava più di 75.000 sequenze genomiche complete[59], ma senza dubbio ve ne sono molte di più ancora da scoprire.[60]
Un virus può essere dotato di un genoma a DNA o uno a RNA e pertanto vengono denominati rispettivamente virus a DNA o virus a RNA; la stragrande maggioranza sono a RNA. I virus delle piante tendono ad avere genomi composti da un singolo filamento di RNA mentre i batteriofagi spesso hanno un genoma a DNA a doppia elica.[61]
I genomi virali possono essere circolari, come nel poliomavirus, o lineari come negli adenovirus. Il tipo di acido nucleico è irrilevante per la forma del genoma. Tra virus a RNA e certi virus a DNA, il genoma è spesso diviso in parti distinte, nel qual caso esso è chiamato “segmentato”. Per i virus a RNA, ogni segmento spesso codifica per una sola proteina e si trovano solitamente in un unico capside. Tuttavia, non è necessario che tutti i segmenti siano nello stesso virione perché il virus sia infettivo, come dimostrato dal virus del mosaico del bromus e da molti altri virus delle piante.[46]
Un genoma virale, indipendentemente dal tipo di acido nucleico, è quasi sempre a singolo filamento o doppio filamento. Genomi a singolo filamento consistono di un acido nucleico spaiato. Genomi a doppio filamento sono costituiti da due acidi nucleici complementari accoppiati. Le particelle virali di alcune famiglie di virus, come quelli appartenenti agli Hepadnaviridae, contengono un genoma che è parzialmente a doppio filamento e parzialmente a singolo filamento.[61]
Per la maggior parte dei virus con genoma a RNA e alcuni con genomi a DNA a singolo filamento, i singoli filamenti sono classificati a senso-positivo (chiamato filamento positivo) o senso-negativo (chiamato filamento negativo), a seconda se sono complementari all’RNA messaggero virale (mRNA). L’RNA virale a senso positivo è nello stesso senso dell’mRNA virale e quindi almeno una parte di esso può essere tradotto immediatamente dalla cellula ospite. L’RNA virale a senso negativo è complementare all’mRNA e quindi deve essere convertito in RNA a senso-positivo tramite una RNA polimerasi RNA-dipendente prima della traduzione. La nomenclatura dei virus DNA con un genoma a un solo senso ssDNA è simile alla nomenclatura RNA, in quanto il filamento stampo per l’mRNA virale è complementare a esso (-) e il filamento codificante è una copia (+).[46] Tuttavia, diversi tipi di virus ssDNA e ssRNA hanno genomi che sono ambisenso e che la trascrizione può verificarsi fuori da entrambi i filamenti in un doppio filamento replicativo intermedio. Gli esempi includono i geminivirus, che sono i virus ssDNA delle piante e gli arenavirus che sono i virus ssRNA degli animali.[62]
La dimensione del genoma varia notevolmente tra le specie. I genomi virali più piccoli, i circoviruses ssDNA della famiglia dei circoviridae, codificano solo per due proteine e hanno una dimensione del genoma di due sole kilobase;[63] il più grande dei pandoravirus possono avere dimensioni del genoma di circa due megabasi che codificano per circa 2500 proteine.[64]
In generale, i virus a RNA hanno dimensioni del genoma più piccoli rispetto ai virus a DNA a causa di un più alto tasso di errore durante la replica e hanno un limite di dimensione massima superiore. Al di là di questo limite, gli errori nel genoma durante la replica rendono il virus inutile o non infettivo. Per compensare questo, i virus a RNA spesso hanno un genoma segmentato: il genoma risulta pertanto diviso in molecole più piccole, riducendo così la possibilità che un errore in un singolo componente inabiliti l’intero genoma. Al contrario, i virus a DNA, in genere, possiedono genomi più grandi a causa della alta fedeltà dei loro enzimi di replicazione.[65] I virus a DNA a singolo filamento sono un’eccezione a questa regola, tuttavia, i tassi di mutazione di questi genomi possono avvicinarsi al caso estremo dei virus ssRNA.[66]
I virus, al pari degli altri sistemi biologici, subiscono mutazioni genetiche attraverso diversi meccanismi. Tra questi, un processo chiamato deriva antigenica le cui basi individuali nel DNA o RNA mutano altre basi ma sempre all’interno della tipologia virale di appartenenza. La maggior parte di queste mutazioni puntiformi sono “silenziose”, ovvero non cambiano la proteina che il gene codifica. Ma altri possono conferire diversità adattative quali la resistenza ai farmaci antivirali.[67-84][68-85] Lo spostamento antigenico si verifica quando vi è un cambiamento importante nel genoma del virus. Questo può essere il risultato di una ricombinazione o un riassortimento dei nucleotidi già presenti. Quando questo accade con i virus influenzali, possono verificarsi le pandemie, come quella che stiamo attualmente subendo.[69-86] I virus a RNA spesso esistono come “quasispecie” o sciami di virus della stessa specie, ma con una sequenza nucleotidica leggermente diversa del genoma. Tali quasispecie sono un obiettivo primario per la selezione naturale scientificamente intesa, ossia una riduzione delle informazioni che determina ad un certo punto la scomparsa di un ceppo virale o, in precedenza, la sua modifica di attività.[70]
Sequenze di genomi conferiscono vantaggi adattativi in ambienti specifici; diversi ceppi di un virus con un genoma segmentato possono mischiare e combinare i geni e quindi produrre prole virus con caratteristiche uniche. Questo è chiamato riassortimento.[71]
La ricombinazione genetica è il processo mediante il quale un filamento di DNA viene rotto per poi essere unito al termine di una diversa molecola di DNA. Questo può verificarsi quando i virus infettano cellule simultaneamente e studi riguardanti l’evoluzione virale hanno dimostrato che la ricombinazione è stata molto frequente nelle specie studiate.[72] La ricombinazione è comune a entrambi i virus, sia a RNA sia a DNA.[73][74]
I virus non sono in grado di riprodursi attraverso la divisione cellulare poiché non sono cellule. Per tanto sfruttano il metabolismo e le risorse di una cellula ospite per produrre copie multiple di sé che si assemblano nella cellula.
Il ciclo di vita dei virus varia molto attraverso le diverse specie, ma vi sono sei fasi fondamentali:[75]
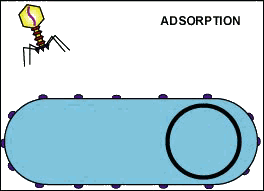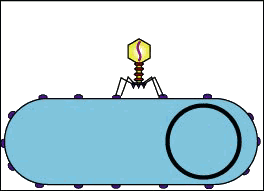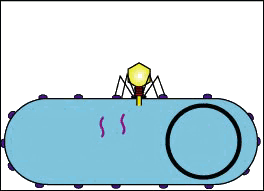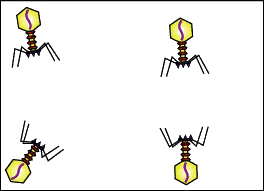
- L’attaccamento è un legame tra le proteine del capside virale e specifici recettori che si trovano sulla superficie cellulare sulla cellula ospite. La presenza di dati recettori sulla superficie determinano la gamma degli ospiti di un virus. Ad esempio, l’HIV infetta una gamma limitata di leucociti umani. Questo perché le sue proteine di superficie, gp120, interagiscono specificamente con la molecola CD4, un recettore delle chemochine, che frequentemente si trova sulla superficie dei linfociti T. Questo meccanismo si è evoluto in modo da favorire quei virus che infettano solo le cellule in cui sono in grado di replicarsi. Il recettore attaccato può indurre la proteina dell’involucro virale a subire cambiamenti che si traducono nella fusione tra le membrane virali e cellulari, o cambiamenti alle proteine senza involucro di superficie del virus che non gli permettono di entrare.
- L’ingresso segue l’attaccamento: virioni entrano nella cellula ospite mediante endocitosi mediata da recettori o attraverso la fusione delle membrane. Questo è spesso chiamato ingresso del virus. L’infezione delle cellule delle piante e dei funghi è diversa da quella delle cellule animali. Le piante hanno una parete cellulare rigida formata da cellulosa, mentre i funghi una di chitina, quindi la maggior parte dei virus possono entrare all’interno di queste cellule solo dopo aver perpetrato una rottura alla parete cellulare.[76] Tuttavia, quasi tutti i virus delle piante (come il virus mosaico del tabacco) possono anche passare direttamente da cellula a cellula, sotto forma di complessi a singolo filamento nucleoproteici, attraverso i pori chiamati plasmodesmi.[77] I batteri, come le piante, hanno pareti cellulari che un virus deve violare per infettare la cellula. Tuttavia, dato che le pareti delle cellule batteriche sono molto meno spesse delle pareti cellulari delle piante, per via delle loro dimensioni molto più piccole, alcuni virus possiedono evoluti meccanismi che iniettano il loro genoma della cellula batterica attraverso la parete cellulare, mentre il capside virale rimane all’esterno.[78]
- L’uncoating è un processo in cui il capside virale viene rimosso: questo può essere dovuto alla degradazione da parte degli enzimi virali o agli enzimi ospiti o per semplice dissociazione; il risultato finale è la liberazione dell’acido nucleico genomico virale.
- La replicazione dei virus coinvolge principalmente la moltiplicazione del genoma. La replica consiste nella sintesi dell’RNA messaggero (mRNA) virale dai geni “early” (con eccezioni per i virus RNA a senso positivo), la sintesi proteica virale, il possibile montaggio delle proteine virali, quindi la replicazione del genoma virale. Questo può essere seguito, per i virus più complessi con genomi più grandi, da parte di uno o più cicli di sintesi di mRNA.
- Assemblaggio, dopo l’auto-assemblaggio struttura-mediata delle particelle virali, alcune modifiche delle proteine si verifica spesso. Nei virus come l’HIV, questa modifica (a volte chiamato la maturazione) avviene dopo che il virus è stato rilasciato dalla cellula ospite.[79]
- Rilascio, i virus possono essere rilasciati dalla cellula ospite per lisi, un processo che uccide la cellula rompendo la sua membrana e la parete cellulare, se presenti: questo avviene in molti batteri e di alcuni virus animali. Alcuni virus subiscono un ciclo lisogenico in cui il genoma virale è incorporato mediante la ricombinazione genetica in un luogo specifico dei cromosomi dell’ospite. Il genoma virale è quindi noto come “provirus” o, nel caso di un batteriofagi “profago”.[80-97] Ogni volta che l’ospite si divide, anche il genoma virale viene replicato. Il genoma virale è per lo più silente all’interno dell’ospite. Tuttavia, a un certo punto, il provirus o profago possono dar luogo al virus attivo, che può lisare le cellule ospiti.[81] I virus capsulati (ad esempio, l’HIV) di solito vengono rilasciati dalla cellula ospite per gemmazione. Durante questo processo il virus acquisisce il suo involucro, che è una parte modificata del plasma dell’ospite o della membrana interna.[82]
Il materiale genetico all’interno delle particelle del virus e il metodo con cui il materiale viene replicato, varia notevolmente tra i diversi tipi di virus.
Virus a DNA
La replicazione del genoma della maggior parte dei virus a DNA avviene nel nucleo della cellula. Se la cellula possiede il recettore appropriato sulla sua superficie, questi virus entrano, a volte, nella cellula per fusione diretta con la membrana cellulare (per esempio, l’herpes virus) o, più spesso. per endocitosi mediata da recettori. La maggior parte dei virus a DNA dipendono interamente dal DNA della cellula ospite e dai suoi strumenti di sintesi e lavorazione dell’RNA. Tuttavia, virus dotati di genomi più grandi, possono codificare gran parte di questi stessi strumenti. Negli eucarioti, il genoma virale deve attraversare la membrana nucleare della cellula per accedere ai meccanismi di replicazione, mentre nei batteri deve solo entrare nella cellula.[83]
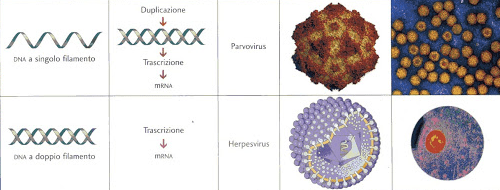
Virus a RNA
La replicazione di solito avviene nel citoplasma. I virus a RNA possono essere classificati in quattro gruppi differenti in base alle modalità di replicazione. La polarità (se può o non può essere utilizzata direttamente dai ribosomi per produrre proteine) dei virus a singolo filamento di RNA determina in gran parte il meccanismo di replicazione; l’altro criterio principale è se il materiale genetico è a singolo o doppio filamento. Tutti i virus a RNA utilizzano i propri enzimi RNA replicasi per creare copie dei loro genomi.[84]

Virus a trascrizione inversa

I virus a trascrizione inversa, possiedono ssRNA (Retroviridae, Metaviridae, Pseudoviridae) o dsDNA (Caulimoviridae, Hepadnaviridae) nelle loro particelle. Quelli con genomi a RNA (retrovirus), utilizzano un intermedio del DNA per replicare, mentre quelli con genomi di DNA (pararetroviruses) utilizzano un intermedio di RNA durante la replicazione del genoma. Entrambi i tipi utilizzano una trascrittasi inversa, o un enzima DNA polimerasi (RNA-dipendente) per effettuare la conversione dell’acido nucleico. I retrovirus integrano il DNA prodotto dalla trascrizione inversa nel genoma dell’ospite come provirus come parte del processo di replica; tuttavia, i pararetroviruses non lo fanno, anche se copie del genoma di particolari pararetroviruses infiltrati nei vegetali possono dar luogo a virus infettivo.[85] Essi sono suscettibili di farmaci antivirali che inibiscono l’enzima della trascrittasi inversa, ad esempio, la zidovudina e la lamivudina. Un esempio del primo tipo è l’HIV, che è un retrovirus. Esempi del secondo tipo sono il l’hepadnaviridae, che comprende il virus dell’epatite B.[86]
Vi è un’ampia serie di effetti strutturali e biochimici che i virus producono sulla cellula ospite.[87] Questi sono chiamati effetti citopatici.[88] La maggior parte delle infezioni da virus alla fine provocano la morte della cellula ospite. Le cause di morte sono la lisi cellulare, le alterazioni della membrana superficie della cellula e l’apoptosi.[89-106] Spesso la morte delle cellule è causata dalla cessazione delle sue normali attività a causa della soppressione da parte delle proteine specifiche del virus, che non tutti sono componenti della particella virale.[90]
Alcuni virus non provocano cambiamenti apparenti alla cellula infettata. Le cellule in cui il virus è latente e inattivo mostrano pochi segni di infezione e spesso vivono normalmente.[91] Ciò provoca infezioni persistenti e il virus rimane spesso in sospeso per molti mesi o anni. Ciò avviene frequentemente, ad esempio, con l’herpes virus.[92][93] Alcuni virus, come il virus di Epstein-Barr, possono indurre le cellule a proliferare senza provocare malignità,[94] mentre altri, come il papillomavirus, sono cause ormai stabilite di insorgenza di tumori.[95]
I virus sono di gran lunga le più abbondanti entità biologiche sulla Terra e superano tutte le altre messe insieme.[96] Essi sono in grado di infettare tutti i tipi di vita cellulare, tra cui animali, piante, batteri e funghi.[5] Tuttavia, le diverse tipologie di virus possono infettare solo una gamma limitata di ospiti e molti sono specie-specifici. Alcuni, come il virus del vaiolo, ad esempio, possono infettare solo una specie, in questo caso l’uomo,[97-114] e pertanto si dice che hanno una gamma di ospiti potenziali ristretta. Altri virus, come il virus della rabbia, possono infettare diverse specie di mammiferi e si dice che hanno una gamma di ospiti vasta.[98] I virus che infettano le piante sono innocui per gli animali e la maggior parte dei virus che infettano gli altri animali sono innocui per gli esseri umani.[99] La gamma dei possibili ospiti di alcuni batteriofagi è limitata a un unico ceppo di batteri e può possono essere usati per rintracciare la fonte di focolai di infezioni, tramite un metodo chiamato fagotipizzazione.[100]
La classificazione dei virus cerca di descrivere la loro diversità nominandoli e raggruppandoli sulla base di somiglianze. Nel 1962, André Lwoff, Robert W. Horne e Paul Tournier per primi svilupparono un sistema di classificazione dei virus, in base al sistema gerarchico di Linneo.[101] Questo approccio si basa sul phylum, sulla classe, sull’ordine, sulla famiglia, sul genere e sulla specie. I virus sono stati raggruppati in base alle loro proprietà condivise (non quelle dei loro ospiti) e al tipo di acido nucleico che forma i loro genomi.[102] In seguito l’International Committee on Taxonomy of Viruses è stato costituito. Tuttavia, i virus non sono stati classificati sulla base del phylum o sulla classe, poiché con le piccole dimensioni del genoma e l’alto tasso di mutazione, rende difficile determinare la loro ascendenza sopra l’ordine. Così la classificazione di Baltimore è utilizzata per integrare la gerarchia più tradizionale.
L’International Committee on Taxonomy of Viruses (ICTV) ha sviluppato l’attuale sistema di classificazione e ha formulato le linee guida che attribuiscono un peso maggiore ad alcune proprietà virali per mantenere l’uniformità della famiglia. È stata istituita un tassonomia unificata (un sistema universale di classificazione per i virus). Il rapporto lCTV 9[103] definisce il concetto di specie virale come il gruppo più basso nella gerarchia della ramificazione dei virus.[104] Tuttavia, attualmente solo una piccola parte dei virus è stata studiata, con analisi di campioni provenienti da esseri umani che hanno dimostrato che il 20% circa delle sequenze virali recuperate non sono mai state viste prima, mentre campioni provenienti dall’ambiente, come dall’acqua di mare e sedimenti oceanici hanno rivelato la presenza di una grande maggioranza di sequenze totalmente nuove.[105]
La struttura tassonomica generale è la seguente:
- Ordine (-virales)
- Famiglia (-viridae)
- Sottofamiglia (-virinae)
- Genere (-virus)
- Specie (-virus)
Nell’attuale (2019) tassonomia ICTV, sono stati istituiti 7 ordini: Caudovirales, Herpesvirales, Ligamenvirales, Mononegavirales, Nidovirales, Picornavirales e Tymovirales. Il comitato non distingue formalmente tra sottospecie, varietà e isolati. In totale vi sono 7 ordini, 103 famiglie, 22 sottofamiglie, 455 generi, circa 2.827 specie e oltre 4.000 tipi non ancora classificati.[106][107]
Il biologo premio Nobel David Baltimore ha ideato il sistema di classificazione di Baltimore.[108] La moderna classificazione dei virus utilizza una combinazione del sistema ICTV e del sistema di Baltimore.[109][110][111]
La classificazione dei virus di Baltimore è basato sul meccanismo di produzione di mRNA. I virus devono generare mRNA dai loro genomi per produrre proteine e replicarsi, ma diversi meccanismi sono utilizzati per raggiungere questo obiettivo in ogni famiglia di virus. I genomi virali possono essere a singolo filamento (ss) o doppio filamento (ds), RNA o DNA, e possono o non possono utilizzare la trascrittasi inversa (RT).
Inoltre, i virus ssRNA possono essere sia senso (+) sia antisenso (-). Questa classificazione pone i virus in sette gruppi:
I: virus dsDNA (Papillomaviridae, Herpesviridae, Poxviridae)
II: virus ssDNA (“senso” +) DNA (ad esempio, Parvovirus)
III: virus dsRNA (ad esempio Reoviridae)
IV: virus (+)ssRNA (senso +) RNA (es Picornaviridae, Togaviridae)
V: virus (−)ssRNA (antisenso -) RNA (es Hepadnaviridae, Rhabdoviridae)
VI: virus ssRNA-RT (senso +) di RNA con intermedio DNA nel ciclo di vita (ad esempio Retrovirus)
VII: virus dsDNA-RT (ad esempio Hepadnaviridae)
Come esempio di classificazione virale, il virus della varicella, il varicella zoster (VZV), appartiene all’ordine Herpesvirales, famiglia Herpesviridae, sottofamiglia Alphaherpesvirinae e genere Varicellovirus. VZV è nel gruppo I della classificazione Baltimore perché è un virus dsDNA che non utilizza la trascrittasi inversa.
Esempi di comuni malattie umane causate da virus includono il raffreddore comune, l’influenza, la varicella e l’herpes labiale. Vi sono anche gravi condizioni, come l’AIDS, la malattia da virus Ebola, l’influenza aviaria e la SARS, che sono causate da virus. La capacità relativa di un virus di causare una malattia è descritta in termini della sua virulenza. Altre patologie sono tutt’oggi indagate per scoprire se hanno un virus come agente causale, come ad esempio se vi sia una possibile connessione tra l’herpesvirus umano 6 (HHV-6) e malattie neurologiche come la sclerosi multipla e la sindrome da affaticamento cronico.[112] Vi sono accesi dibattiti sulla possibilità che il bornavirus, ritenuto causa di malattie neurologiche nei cavalli, possa essere anche responsabile per alcune malattie psichiatriche negli esseri umani.[113]
I virus hanno differenti meccanismi per cui causano una malattia in un organismo, i quali dipendono in larga misura dalla specie virale. Meccanismi a livello cellulare comprendono principalmente la lisi cellulare, che comporta la rottura della cellula e la sua conseguente morte. Negli organismi pluricellulari, se un numero abbastanza consistente di cellule muoiono, l’intero organismo incomincerà a subirne gli effetti. Sebbene i virus causino la perdita dell’omeostasi, con conseguente insorgenza di una malattia, possono esisterne di relativamente innocui all’interno di un organismo. Un esempio potrebbe includere la capacità del virus dell’herpes simplex, responsabile dell’herpes labiale, di rimanere in uno stato inattivo nel corpo umano, una condizione denominata di “latenza”[114] che è una caratteristica dei virus herpes, tra cui il virus di Epstein-Barr, che provoca la febbre ghiandolare, e del virus della varicella-zoster, causa della varicella e dell’herpes zoster. La maggior parte delle persone al mondo, nella loro vita, sono state infettate con almeno uno di questi tipi di herpes virus.[115] Tuttavia, questi virus latenti possono talvolta essere utili, infatti la presenza del virus può aumentare l’immunità contro alcuni batteri patogeni, come lo Yersinia pestis.[116]
Alcuni virus possono causare un’infezione permanente o cronica, in cui i virus continuano a replicarsi nel corpo, nonostante i meccanismi di difesa dell’ospite.[117] Questo è comune nei virus dell’epatite B e nelle infezioni da virus dell’epatite C. Le persone con una infezione cronica sono note come vettori, in quanto fungono da serbatoi del virus infettivo.[118] Nelle popolazioni con un’alta percentuale di portatori, la malattia si dice che sia endemica.[119]
L’epidemiologia virale è una branca della scienza medica che si occupa di studiare la trasmissione e controllare le infezioni da virus negli esseri umani. La trasmissione di virus può essere verticale, cioè da madre a figlio, o orizzontale, il che significa che da persona a persona. Esempi di trasmissione verticale comprendono il virus dell’epatite B e l’HIV, in cui il bambino nasce già infettato con il virus.[120] Un altro, più raro, esempio è il virus della varicella zoster, che, pur causando infezioni relativamente lievi negli esseri umani, può essere fatale per il feto e il neonato.[121]
La trasmissione orizzontale è il meccanismo più comune di diffusione del virus nelle popolazioni. La trasmissione può verificarsi quando vi è scambio di fluidi corporei durante un rapporto sessuale, come nel caso dell’HIV; o quando vi è contaminazione di sangue infetto come durante una trasfusione o con lo scambio di aghi, come spesso si riscontra nella trasmissione dell’epatite C; lo scambio di saliva dalla bocca, per esempio può portare alla trasmissione del virus di Epstein-Barr; il norovirus può trasmettersi con l’ingestione di cibo o acqua contaminati; il virus dell’influenza per inalazione; mentre insetti vettori, come le zanzare, trasmettono all’organismo ospite alcuni virus come quello della febbre dengue. Il tasso o la velocità di trasmissione delle infezioni virali dipende da vari fattori che includono la densità della popolazione, il numero dei soggetti suscettibili (cioè quelli che non immuni),[122] la qualità dell’assistenza sanitaria e il tempo.[123]
L’epidemiologia tenta di interrompere la catena delle infezioni nelle popolazioni durante le epidemie di malattie virali.[124] Le misure di controllo utilizzate si basano sulla conoscenza di come il virus si trasmette. È fondamentale trovare la fonte, o le fonti, del focolaio, in modo da identificare il virus. Una volta che è stato identificato, la catena di trasmissione può talvolta essere interrotta grazie a vaccini. Quando essi non sono disponibili, misure di igiene e la disinfezione possono essere rimedi efficaci. Spesso, le persone infette vengono isolate dal resto della comunità e quelli che sono stati esposti al virus vengono posti in quarantena.[125] Per controllare l’epidemia di afta epizootica nel bestiame avvenuta nel 2001 in Gran Bretagna, migliaia di bovini sono stati abbattuti.[126] Le infezioni virali degli esseri umani e degli altri animali hanno periodi di incubazione durante i quali l’infezione provoca segni o sintomi.[127] I periodi di incubazione per le malattie virali variano da pochi giorni a settimane, ma sono noti per la maggior parte delle infezioni.[127] Con una piccola sovrapposizione, al termine del periodo di incubazione vi è il periodo di contagiosità, in cui un individuo infetto può trasmettere la malattia a un altro.[127] Anche questo periodo è noto per molte infezioni virali e la conoscenza della durata di entrambi i periodi è importante nel controllo dei focolai.[128] Quando un focolaio provoca una percentuale insolitamente alta di casi in una popolazione o in una comunità o una regione, questi casi prendono il nome di epidemie. Se i focolai sono geograficamente distribuiti, essi sono chiamati pandemie.[129]
Le popolazioni dei nativi americani furono decimate dalle malattie contagiose, in particolare dal vaiolo, portate dai coloni europei in America. Non è chiaro quanti siano deceduti a causa delle malattie importare dagli stranieri dopo l’arrivo di Colombo, ma le stime indicano un possibile 70% della popolazione indigena.[senza fonte] Tutto ciò ha contribuito in modo significativo ai tentativi europei di spostare e sottomettere la popolazione nativa.[130]

Una pandemia è un’epidemia mondiale. La pandemia influenzale del 1918 (chiamata “influenza spagnola”) che durò fino al 1919, fu catalogata come pandemia di livello 5, causata da un virus influenzale particolarmente aggressivo e mortale. Le vittime furono spesso giovani adulti sani, in contrasto con la maggior parte dei focolai di influenza che colpiscono prevalentemente i pazienti pediatrici, gli anziani o gli individui già indeboliti.[131] Le stime più datate indicano che questa pandemia abbia ucciso tra le 40 e le 50 milioni di persone,[132] mentre ricerche più recenti suggeriscono che tale dato potrebbe arrivare fino a 100 milioni di persone, il 5% della popolazione mondiale del 1918.[133]
La maggior parte dei ricercatori ritiene che l’origine del virus HIV sia nell’Africa sub-sahariana e che sia nato nel corso del XX secolo.[134] Anche la sua diffusione è oramai considerata una pandemia, con una stima di 38,6 milioni di persone infettate in tutto il mondo.[135] Le stime del Programma delle Nazioni Unite per l’AIDS/HIV(UNAIDS) e dell’Organizzazione Mondiale della Sanità (OMS) indicando che l’AIDS (la condizione dovuta al virus HIV) abbia ucciso più di 25 milioni di persone dal 5 giugno 1981, quando è stato riconosciuto, rendendola una delle epidemie più devastanti della storia.[136] Nel 2007 sono state stimate 2,7 milioni di nuove infezioni da HIV e 2 milioni di decessi correlati alla condizione.[137]
Diversi agenti patogeni virali altamente letali sono membri dei Filoviridae. I filovirus sono virus simili a filamenti che causano febbre emorragica, e comprendono l’Ebolavirus e il Marburgvirus. Il virus di Marburg, scoperto nel 1967, ha attirato l’attenzione dei media nel mese di aprile 2005 per un focolaio in Angola.[138] Il virus della malattia da virus Ebola ha causato epidemie intermittenti con alti tassi di mortalità, dal 1976 quando è stato identificato. Quella peggiore e più recente è stata l’epidemia di in Africa Occidentale del 2014.[139]
Si è stabilito che i virus siano una causa di tumore negli esseri umani e in altre specie. Tuttavia, i tumori virali si verificano solo in una minoranza di persone (o animali) infette. I virus causa di tumore possono far parte di diverse famiglie di virus, compresi i virus a RNA e DNA e quindi non esiste un unico tipo di “oncovirus” (un termine ormai obsoleto). Lo sviluppo della neoplasia è determinato da una serie di fattori come ad esempio l’immunità dell’ospite[140] e le sue mutazioni.[141] I virus ritenuti in grado di provocare tumori negli umani comprendono alcuni genotipi di papillomavirus umano, il virus dell’epatite B, il virus dell’epatite C, il virus di Epstein-Barr, l’herpesvirus associato al sarcoma di Kaposi e il virus T-linfotropico dell’uomo. Il virus causa di tumore umano più recentemente scoperto è un poliomavirus (poliomavirus delle cellule di Merkel) che causa la maggior parte dei casi di una rara forma di tumore della pelle, chiamato carcinoma a cellule di Merkel.[142]

I virus dell’epatite possono sviluppare una infezione virale cronica che può portare al tumore del fegato.[143][144] L’infezione da virus T-linfotropico dell’uomo può portare a paraparesi spastica tropicale e la leucemia a cellule T dell’adulto.[145] I papillomavirus umani sono una causa consolidata di tumori della cervice uterina, della pelle, dell’ano e del pene.[146] Gli Herpesvirus umano 8 provoca il sarcoma di Kaposi, mentre il virus di Epstein-Barr causa il linfoma di Burkitt, il linfoma di Hodgkin, disordini linfoproliferativi delle cellule B e il carcinoma nasofaringeo.[147] Il poliomavirus delle cellule di Merkel è strettamente correlato al Simian virus 40 e al poliomavirus del topo; entrambi vengono utilizzati, da oltre 50 anni, come modelli animali per i virus tumorali.[148]
La prima linea di difesa dell’organismo contro i virus è il sistema immunitario innato. Questo comprende le cellule e gli altri meccanismi che difendono l’ospite da infezioni in modo non specifico. Ciò significa che le cellule del sistema innato riconoscono e rispondono agli agenti patogeni in modo generico ma, a differenza del sistema immunitario adattativo, esso non conferisce un’immunità duratura.[149]
L’interferenza dell’RNA è un importante difesa innata contro i virus.[150] Molti virus adottano una strategia di replica che coinvolge l’RNA a doppio filamento (dsRNA). Quando un virus infetta una cellula, rilascia la sua molecola di RNA che si lega immediatamente a un complesso proteico chiamato ribonucleasi III che taglia l’RNA in pezzi più piccoli. Un percorso biochimico, il complesso RISC, si attiva assicurando la sopravvivenza cellulare degradando l’mRNA virale. I rotavirus si sono evoluti per evitare questo meccanismo di difesa evitando di tagliare completamente l’RNA all’interno della cellula ma rilasciando una nuova produzione di mRNA attraverso i pori del capside interno della particella. In questo modo il loro dsRNA genomico resta protetto all’interno del nucleo del virione.[151][152]
Quando il sistema immunitario adattativo di un vertebrato incontra un virus, produce anticorpi specifici che si legano a esso e spesso sono in grado di renderlo non infettivo. Ciò è chiamata immunità umorale. Due tipi di anticorpi sono importanti. I primi, chiamati IgM, sono altamente efficaci nel neutralizzare i virus, ma vengono prodotti dalle cellule del sistema immunitario solo per poche settimane. I secondi, chiamati IgG, vengono prodotti di continuo. La presenza di IgM nel sangue dell’ospite viene utilizzato per diagnosticare la presenza di una infezione acuta, mentre le IgG indicano un’infezione passata.[153] Quando i test di immunità vengono effettuati, vengono misurati gli anticorpi IgG.[154]
Gli anticorpi possono continuare a essere un meccanismo di difesa efficace anche dopo che i virus sono riusciti a ottenere l’ingresso nella cellula ospite. Una proteina presente nelle cellule, chiamata TRIM21, è in grado di legarsi agli anticorpi sulla superficie della particella virale. Questo innesca la successiva distruzione del virus da parte degli enzimi del proteosoma della cellula.[155]
Una seconda difesa dei vertebrati contro i virus, si chiama immunità cellulo-mediata e coinvolge le cellule immunitarie conosciute come cellule T. Le cellule del corpo mostrano costantemente brevi frammenti delle loro proteine sulla superficie della cellula e se una cellula T riconosce un frammento virale sospetto, la cellula ospite viene distrutta dalle cellule T killer e le cellule T virus-specifiche proliferano. Le cellule, come i macrofagi sono specialisti in questa presentazione dell’antigene.[156] La produzione di interferone è anch’esso un importante meccanismo di difesa dell’ospite. Questo è un ormone prodotto dal corpo quando vi è la presenza di virus. Il suo ruolo nel sistema immunitario è complesso; ma sostanzialmente mette fine alla riproduzione del virus, uccidendo la cellula infetta e le sue vicine.[157]

Non tutte le infezioni da virus producono una risposta immunitaria protettiva in questo modo. L’HIV elude il sistema immunitario cambiando continuamente la sequenza aminoacidica delle proteine sulla superficie del virione. Questa tecnica è nota come “mutazione di fuga”. Questi virus persistono nell’eludere il sistema immunitario, attraverso il sequestro e blocco della presentazione dell’antigene, la resistenza alle citochine, l’evasione delle attività delle cellule natural killer, evitare l’apoptosi e la sostituzione antigenica.[158] Altri virus, chiamati virus neurotropi, sfruttano la diffusione neurale in cui il sistema immunitario potrebbe non essere in grado di raggiungerli.
Poiché i virus utilizzano vie metaboliche vitali all’interno cellule ospiti per replicarsi, essi risultano difficili da eliminare senza usare farmaci che causino effetti tossici alle cellule dell’ospite. Gli approcci medici più efficaci per le malattie virali sono le vaccinazioni, in grado di fornire l’immunità alle infezioni, e i farmaci antivirali che interferiscono selettivamente con la replicazione del virus.
Nota: non posso di certo essere definito un “Full-Vax” ma nemmeno un folle riduzionista opposto “No-Vax”. Sono piuttosto uno “Smart-Vax”.

La vaccinazione è un modo economico ed efficace per prevenire le infezioni da virus. I vaccini sono stati usati per prevenire le infezioni virali molto prima della scoperta dei virus reali. Il loro utilizzo ha portato a un drastico calo della morbilità (l’ammalarsi) a alla mortalità (morte) associata a infezioni virali, come la poliomielite, il morbillo, la parotite e la rosolia.[159] Le infezioni di vaiolo sono state debellate.[160] A oggi, 2015, vi è la disponibilità di vaccini per oltre tredici infezioni virali che colpiscono gli esseri umani,[161] e molti altri vengono utilizzati per prevenire le infezioni virali degli animali.[162]
I vaccini possono essere costituiti da virus vivi, attenuati o morti, o da proteine virali (antigeni).[163] Le forme di vaccini vivi, contengono virus indeboliti che non causano la malattia ma, ciò nonostante, conferiscono l’immunità. I vaccini vivi possono essere pericolosi quando somministrati a persone con una debole immunità (individui immunocompromessi) poiché in queste persone il virus indebolito può provocare la malattia originale.[164] La biotecnologia e le tecniche di ingegneria genetica vengono utilizzate per la produzione di vaccini di subunità. Questi vaccini utilizzano solo le proteine del capside del virus. Il vaccino contro l’epatite B è un esempio di questo tipo di vaccino.[165] I vaccini di subunità sono sicuri per i pazienti immunocompromessi perché non possono in nessun modo provocare la malattia.[166] Il vaccino contro il virus della febbre gialla, un ceppo vivo attenuato e chiamato 17D, è probabilmente il più sicuro e il più efficace vaccino mai prodotto.[167]

Un mezzo di contrasto all’infezione virale è rappresentatpo dai farmaci antivirali. Essi sono spesso analoghi nucleosidici (costruzioni di DNA falso), che i virus erroneamente incorporano nei loro genomi durante la replicazione. Il ciclo di vita del virus viene bloccata perché il DNA di nuova sintesi risulta inattivo. Infatti in questi analoghi mancano i gruppi ossidrilici, che, insieme con gli atomi di fosforo, si collegano insieme per formare il la forte “spina dorsale” della molecola di DNA. Ciò prende il nome di interruzione della catena del DNA.[168] Esempi di analoghi nucleosidici sono l’aciclovir per il Virus dell’herpes simplex e la lamivudina per le infezioni da virus HIV e epatite B. L’aciclovir è uno dei più antichi farmaci antivirali e più frequentemente prescritti.[169] Altri farmaci antivirali utilizzano come bersaglio diverse fasi del ciclo di vita del virus. L’HIV dipende da un enzima proteolitico chiamato HIV-1 proteasi per farlo diventare completamente infettivo. Vi è un vasto gruppo di farmaci, chiamati inibitori della proteasi, che inattivano questo enzima.
L’epatite C è causata da un virus a RNA. Nel 80% delle persone infette la malattia risulta cronica e in assenza di trattamento restano infetti per tutta la loro vita. Tuttavia, vi è ora un trattamento efficace che utilizza un analogo nucleosidico, la ribavirina, combinato con l’interferone.[170] Il trattamento dei portatori cronici del virus dell’epatite B utilizzando una strategia simile utilizzando la lamivudina.[171]
Nota: i virus possono essere considerati regolatori delle forme biologiche “semplici” e “complesse”.
Una caratteristica dei virus, che la maggior parte delle persone non conosce, è che molti di essi hanno azione benefica. Lo ammetto, ogni volta che viene detto per molti è un vero è oroprio shock, ma in effetti le cose stanno così: la maggior parte dei virus ha azione benefica. Provate solo a considerare il fatto che vi sono più virus nell’intestino che batteri! In effetti, la popolazione virale (chiamata “viroma”[172]) svolge un ruolo importante nella regolazione del numero e dei tipi di batteri nel corpo.[173] Senza di essi, potremmo essere rapidamente consumati dai piccoli batteri affamati che vivono nel nostro intestino.
Avete presente quando nuotate nel mare? Ecco, è un po’ come nuotare in una zuppa batterica altamente concentrata. Ci sono molti batteri nell’acqua del mare, di molte specie diverse. Ma, come nell’intestino, ci sono più virus che batteri e probabilmente i primi svolgono un ruolo nel mantenere e bilanciare la popolazione batterica nelle acque marine. Alcuni si pongono se vi sarebbe vita negli oceani/mari se non vi fossero virus. Ed è questo il motivo per il quale in precedenza ho denominato i virus come “agenti regolatori” che influenzano altre entità biologiche.

L’esempio della “zuppa batterico-virale” può essere applicata anche ad un lago. Infatti, in esso possono aver nuotato anatre, cigni o oche. Di conseguenza vi si possono trovare virus dell’influenza. In effetti, gli uccelli acquatici trasportano tutti i possibili tipi di virus influenzale, compresi quelli che non infettano l’uomo. Questi virus vengono introdotti nell’acqua quando gli uccelli defecano. Ma la presenza del virus di solito non produce malattie in questi uccelli, [174] o in un soggetto umano, anche se entrano in contatto con occhi, orecchie, naso e bocca. Un evoluzionista potrebbe dire che il motivo per cui gli uccelli non si ammalano (di solito) è perché la convivenza prolungata nel tempo del ceppo virale e dell’animale ha portato ad una condizione collaborativa, dove in virus usa l’ospite semplicemente come mezzo per sopravvivere senza causarne malessere o il decesso. Dal punto di vista dell’intelligence design , il virus dell’influenza ha probabilmente un ruolo benefico per gli uccelli, oppure ha semplicemente subito mutazioni degenerative che lo rendono controllabile dall’organismo ospite in questione.
Dal momento che le nostre cellule posseggono molte delle stesse cose di cui sono composti i virus (rivestimenti proteici, DNA e RNA, disponiamo di meccanismi per spostare il DNA in diverse parti del genoma, ecc), alcuni virus, come già accennato, potrebbero aver avuto origine dalle normali operazioni cellulari.[175] Le componenti sono tutte lì, a volte esse sono assemblate in cose che sembrano quasi virus. Basterebbero alcune modifiche non ben calibrate e l’assemblaggio potrebbe sfuggire di mano e “diventare virale”.
Ma non tutti i virus sono genoma-simili. Molti virus che causano malattie sembrano progettati per fare ciò. Quindi, la domanda che sorge spontanea è: da dove vengono ? Bene, se esiste un virus progettato per infettare un batterio, una cellula di topo o di una persona, probabilmente ci sono controlli e equilibri in quel sistema. Se uno di questi controlli fallisce, il virus potrebbe essere in grado di riprodursi molto più velocemente di quanto originariamente era stato progettato di fare. Ciò comporterebbe una malattia. Pertanto, un virus “benefico” potrebbe essere in grado di mutare in un virus pericoloso, sempre un virus ma con effetti differenti per mutazione. Potrebbero essere necessarie alcune piccole mutazioni, come forse un cambiamento in un fattore di riconoscimento cellulare che impedisce alle cellule ospiti di rilevare e quindi regolare il virus.

Adesso che abbiamo sufficienti e reali informazioni sui Virus possiamo iniziare a trattare l’argomento Covid-19 per comprendere la prima epidemia virale mondiale del XXI Secolo, caratteristiche del patogeno e cosa realmente possiamo fare per prevenirne il contagio e quali sono le attuali possibilità di trattamento degli infetti.
Continua…
Gabriel Bellizzi
Riferimenti:
1- Koonin EV, Senkevich TG, Dolja VV, The ancient Virus World and evolution of cells, in Biol. Direct, vol. 1, 2006, p. 29.
2- Bernard La Scola, Christelle Desnues e Isabelle Pagnier, The virophage as a unique parasite of the giant mimivirus, in Nature, vol. 455, nº 7209, pp. 100–104.
3- Ed Yong, The virophage – a virus that infects other viruses, su National Geographic – Phenomena, 8 luglio 2008. URL consultato il 12 marzo 2016.
4- Nigel J. Dimmock, Andrew J. Easton e Keith N. Leppard, Introduction to Modern Virology, VI, Blackwell Publishing, 2007.
5- Bordenave G, Louis Pasteur (1822–1895), in Microbes and Infection / Institut Pasteur, vol. 5, nº 6, 2003, pp. 553–60.
6- eri Shors, Understanding Viruses, Jones and Bartlett Publishers, 2008.
7- Leslie Collier, Albert Balows e Max Sussman, Virology, in Brian H Mahy e Leslie Collier (a cura di), Topley and Wilson’s Microbiology and Microbial Infections, vol. 1, 9ª ed., Arnold, 1998.
8- Teri Shors, Understanding Viruses, Jones and Bartlett Publishers, 2008.
9- Nigel J. Dimmock, Andrew J. Easton e Keith N. Leppard, Introduction to Modern Virology, VI, Blackwell Publishing, 2007.
10- F. Fenner, History of Virology: Vertebrate Viruses, in Brian W. J. Mahy e Marc H. V. Van Regenmortel (a cura di), Desk Encyclopedia of General Virology, 1ª ed., Oxford, UK, Academic Press, 2009, pp. 15-19.
11- Steinhardt E, Israeli C, Lambert R.A., Studies on the cultivation of the virus of vaccinia, in J. Inf Dis., vol. 13, nº 2, 1913, pp. 294–300.
12- Leslie Collier, Albert Balows e Max Sussman, Virology, in Brian H Mahy e Leslie Collier (a cura di), Topley and Wilson’s Microbiology and Microbial Infections, vol. 1, 9ª ed., Arnold, 1998.
13- Goodpasture EW, Woodruff AM, Buddingh GJ, The cultivation of vaccine and other viruses in the chorioallantoic membrane of chick embryos, in Science, vol. 74, nº 1919, 1931, pp. 371–372.
14- Rosen, FS, Isolation of poliovirus—John Enders and the Nobel Prize, in New England Journal of Medicine, vol. 351, nº 15, 2004, pp. 1481–83.
15- From Nobel Lectures, Physics 1981–1990, (1993) Editor-in-Charge Tore Frängsmyr, Editor Gösta Ekspång, World Scientific Publishing Co., Singapore.
In 1887, Buist visualised one of the largest, Vaccinia virus, by optical microscopy after staining it. Vaccinia was not known to be a virus at that time. (Buist J.B. Vaccinia and Variola: a study of their life history Churchill, London).
16- Stanley WM, Loring HS, The isolation of crystalline tobacco mosaic virus protein from diseased tomato plants, in Science, vol. 83, nº 2143, 1936, p. 85.
17- Stanley WM, Lauffer MA, Disintegration of tobacco mosaic virus in urea solutions, in Science, vol. 89, nº 2311, 1939, pp. 345–347.
18- Creager AN, Morgan GJ, After the double helix: Rosalind Franklin’s research on Tobacco mosaic virus, in Isis, vol. 99, nº 2, 2008, pp. 239–72.
19- Nigel J. Dimmock, Andrew J. Easton e Keith N. Leppard, Introduction to Modern Virology, VI, Blackwell Publishing, 2007.
20- Norrby E, Nobel Prizes and the emerging virus concept, in Arch. Virol., vol. 153, nº 6, 2008, pp. 1109–23.
21- Leslie Collier, Albert Balows e Max Sussman, Virology, in Brian H Mahy e Leslie Collier (a cura di), Topley and Wilson’s Microbiology and Microbial Infections, vol. 1, 9ª ed., Arnold, 1998, ISBN 0-340-66316-2.
22- Temin HM, Baltimore D, RNA-directed DNA synthesis and RNA tumor viruses, in Adv. Virus Res., vol. 17, 1972, pp. 129–86.
23- Barré-Sinoussi, F. et al., Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS), in Science, vol. 220, nº 4599, 1983, pp. 868–871.
24- Sanjuán R, Nebot MR, Chirico N, Mansky LM, Belshaw R, Viral mutation rates, in Journal of Virology, vol. 84, nº 19, October 2010, pp. 9733–48.
25- Teri Shors, Understanding Viruses, Jones and Bartlett Publishers, 2008.
26- Leslie Collier, Albert Balows e Max Sussman, Virology, in Brian H Mahy e Leslie Collier (a cura di), Topley and Wilson’s Microbiology and Microbial Infections, vol. 1, 9ª ed., Arnold, 1998.
27- Nigel J. Dimmock, Andrew J. Easton e Keith N. Leppard, Introduction to Modern Virology, VI, Blackwell Publishing, 2007.
28- Leslie Collier, Albert Balows e Max Sussman, Virology, in Brian H Mahy e Leslie Collier (a cura di), Topley and Wilson’s Microbiology and Microbial Infections, vol. 1, 9ª ed., Arnold, 1998.
29- Mahy WJ & Van Regenmortel MHV (eds), Desk Encyclopedia of General Virology, Oxford, Academic Press, 2009, pp. 24.
30- Leslie Collier, Albert Balows e Max Sussman, Virology, in Brian H Mahy e Leslie Collier (a cura di), Topley and Wilson’s Microbiology and Microbial Infections, vol. 1, 9ª ed., Arnold, 1998.
31- Teri Shors, Understanding Viruses, Jones and Bartlett Publishers, 2008.
32- B. McClintock, The origin and behavior of mutable loci in maize, in Proc Natl Acad Sci U S A., vol. 36, nº 6, 1950, pp. 344–55.
33- Nigel J. Dimmock, Andrew J. Easton e Keith N. Leppard, Introduction to Modern Virology, VI, Blackwell Publishing, 2007.
34- Teri Shors, Understanding Viruses, Jones and Bartlett Publishers, 2008.
35- Tsagris EM, de Alba AE, Gozmanova M, Kalantidis K, Viroids, in Cell. Microbiol., vol. 10, nº 11, 2008, pp. 2168.
36- Teri Shors, Understanding Viruses, Jones and Bartlett Publishers, 2008.
37- Tsagris EM, de Alba AE, Gozmanova M, Kalantidis K, Viroids, in Cell. Microbiol., vol. 10, nº 11, 2008, pp. 2168,
38- Teri Shors, Understanding Viruses, Jones and Bartlett Publishers, 2008.
39- a Scola B, Desnues C, Pagnier I, Robert C, Barrassi L, Fournous G, Merchat M, Suzan-Monti M, Forterre P, Koonin E, Raoult D, The virophage as a unique parasite of the giant mimivirus, in Nature, vol. 455, nº 7209, 2008, pp. 100–4.
40- Mahy WJ & Van Regenmortel MHV (eds), Desk Encyclopedia of General Virology, Oxford, Academic Press, 2009, pp. 28.
41- Mahy WJ & Van Regenmortel MHV (eds), Desk Encyclopedia of General Virology, Oxford, Academic Press, 2009, pp. 26.
42- Dimmock, pp. 15-16.
43- Holmes EC, Viral evolution in the genomic age, in PLoS Biol., vol. 5, nº 10, 2007, pp. e278.
44- Wimmer E, Mueller S, Tumpey TM, Taubenberger JK, Synthetic viruses: a new opportunity to understand and prevent viral disease, in Nature Biotechnology, vol. 27, nº 12, 2009, pp. 1163–72.
45- Horn M, Chlamydiae as symbionts in eukaryotes, in Annual Review of Microbiology, vol. 62, 2008, pp. 113–31.
46- Collier, pp. 33-55.
47- Collier, pp. 33-37.
48- Collier, p. 40.
49- Caspar DL, Klug A, Physical principles in the construction of regular viruses, in Cold Spring Harb. Symp. Quant. Biol., vol. 27, 1962, pp. 1–24.
50- Crick FH, Watson JD, Structure of small viruses, in Nature, vol. 177, nº 4506, 1956, pp. 473–5.
51- M.R. Falvo, S. Washburn, R. Superfine, M. Finch, F.P. Brooks Jr, V. Chi, R.M. Taylor 2nd, Manipulation of individual viruses: friction and mechanical properties, in Biophysical Journal, vol. 72, nº 3, 1997, pp. 1396–1403.
52- Yu. G. Kuznetsov, A. J. Malkin, R. W. Lucas, M. Plomp, A. McPherson, Imaging of viruses by atomic force microscopy, in J Gen Virol, vol. 82, nº 9, 2001, pp. 2025–2034.
53- Collier, p. 37.
54- Collier, pp. 40, 42.
55- Casens, S., Desk Encyclopedia of General Virology, Boston, Academic Press, 2009, pp. 167–174.
56- Collier, pp. 42-43.
57- Rossmann MG, Mesyanzhinov VV, Arisaka F, Leiman PG, The bacteriophage T4 DNA injection machine, in Current Opinion in Structural Biology, vol. 14, nº 2, 2004, pp. 171–80.
58- Long GW, Nobel J, Murphy FA, Herrmann KL, Lourie B, Experience with electron microscopy in the differential diagnosis of smallpox, in Appl Microbiol, vol. 20, nº 3, 1970, pp. 497–504.
59- NCBI Viral Genome database, su ncbi.nlm.nih.gov.
60- Pennisi E, Microbiology. Going viral: exploring the role of viruses in our bodies [collegamento interrotto], in Science, vol. 331, nº 6024, 2011, pp. 1513.
61- Collier, pp. 96-99.
62- Carter, p. 72.
63- Belyi VA, Levine AJ e Skalka AM, Sequences from ancestral single-stranded DNA viruses in vertebrate genomes: the parvoviridae and circoviridae are more than 40 to 50 million years old, in J. Virol., vol. 84, nº 23, 2010, pp. 12458–62.
64- Philippe N, Legendre M, Doutre G, Couté Y, Poirot O, Lescot M, Arslan D, Seltzer V, Bertaux L, Bruley C, Garin J, Claverie JM e Abergel C, Pandoraviruses: amoeba viruses with genomes up to 2.5 Mb reaching that of parasitic eukaryotes, in Science, vol. 341, nº 6143, 2013, pp. 281–6.
65- Pressing J, Reanney DC, Divided genomes and intrinsic noise, in J Mol Evol, vol. 20, nº 2, 1984, pp. 135–46.
66- Duffy S, Holmes EC, Validation of high rates of nucleotide substitution in geminiviruses: phylogenetic evidence from East African cassava mosaic viruses, in The Journal of General Virology, vol. 90, Pt 6, 2009, pp. 1539–47.
67- Sandbulte MR, Westgeest KB, Gao J, Xu X, Klimov AI, Russell CA, Burke DF, Smith DJ, Fouchier RA, Eichelberger MC, Discordant antigenic drift of neuraminidase and hemagglutinin in H1N1 and H3N2 influenza viruses, in Proceedings of the National Academy of Sciences of the United States of America, vol. 108, nº 51, December 2011, pp. 20748–53.
68- Moss RB, Davey RT, Steigbigel RT, Fang F, Targeting pandemic influenza: a primer on influenza antivirals and drug resistance, in The Journal of Antimicrobial Chemotherapy, vol. 65, nº 6, June 2010, pp. 1086–93.
69- Hampson AW, Mackenzie JS, The influenza viruses, in Med. J. Aust., vol. 185, 10 Suppl, 2006, pp. S39–43.
70- Metzner KJ, Detection and significance of minority quasispecies of drug-resistant HIV-1, in J HIV Ther, vol. 11, nº 4, 2006, pp. 74–81.
71- Goudsmit.
72- Worobey M, Holmes EC, Evolutionary aspects of recombination in RNA viruses, in J. Gen. Virol., 80 ( Pt 10), 1999, pp. 2535–43.
73- Lukashev AN, Role of recombination in evolution of enteroviruses, in Rev. Med. Virol., vol. 15, nº 3, 2005, pp. 157–67.
74- Umene K, <171::AID-RMV243>3.0.CO;2-A Mechanism and application of genetic recombination in herpesviruses, in Rev. Med. Virol., vol. 9, nº 3, 1999, pp. 171–82.
75- Collier, pp. 75-91.
76- Dimmock, p. 70.
77- Boevink P, Oparka KJ, Virus-host interactions during movement processes, in Plant Physiol., vol. 138, nº 4, 2005, pp. 1815–21.
78- Dimmock, p. 71.
79- Barman S, Ali A, Hui EK, Adhikary L, Nayak DP, Transport of viral proteins to the apical membranes and interaction of matrix protein with glycoproteins in the assembly of influenza viruses, in Virus Res., vol. 77, nº 1, 2001, pp. 61–9.
80- Shors, pp. 60, 597.
81- Dimmock, Capitolo 15, Mechanisms in virus latentcy, pp.243–259.
82- Dimmock, pp. 185-187.
83- Shors, p. 54; Collier, p. 78.
84- Collier, p. 79.
85- Staginnus C, Richert-Pöggeler KR, Endogenous pararetroviruses: two-faced travelers in the plant genome, in Trends in Plant Science, vol. 11, nº 10, 2006, pp. 485–91.
86- Collier, pp. 88-89.
87- Collier, pp. 115-146.
88- Collier, p. 115.
89- Roulston A, Marcellus RC, Branton PE, Viruses and apoptosis, in Annu. Rev. Microbiol., vol. 53, 1999, pp. 577–628.
90- Alwine JC, Modulation of host cell stress responses by human cytomegalovirus, in Curr. Top. Microbiol. Immunol., vol. 325, 2008, pp. 263–79.
91- Sinclair J, Human cytomegalovirus: Latency and reactivation in the myeloid lineage, in J. Clin. Virol., vol. 41, nº 3, 2008, pp. 180–5.
92- Jordan MC, Jordan GW, Stevens JG, Miller G, Latent herpesviruses of humans, in Annals of Internal Medicine, vol. 100, nº 6, 1984, pp. 866–80.
93- Sissons JG, Bain M, Wills MR, Latency and reactivation of human cytomegalovirus, in J. Infect., vol. 44, nº 2, 2002, pp. 73–7.
94- Barozzi P, Potenza L, Riva G, Vallerini D, Quadrelli C, Bosco R, Forghieri F, Torelli G, Luppi M, B cells and herpesviruses: a model of lymphoproliferation, in Autoimmun Rev, vol. 7, nº 2, 2007, pp. 132–6.
95- Subramanya D, Grivas PD, HPV and cervical cancer: updates on an established relationship, in Postgrad Med, vol. 120, nº 4, 2008, pp. 7–13.
96- Crawford, p. 16.
97- Shors, p. 388.
98- Shors, p. 353.
99- Dimmock, p. 272.
100- Baggesen DL, Sørensen G, Nielsen EM, Wegener HC, Phage typing of Salmonella Typhimurium – is it still a useful tool for surveillance and outbreak investigation?, in Eurosurveillance, vol. 15, nº 4, 2010, pp. 19471.
101- Lwoff A, Horne RW, Tournier P, A virus system, in C. R. Hebd. Seances Acad. Sci., vol. 254, 1962, pp. 4225–7.
102- Lwoff A, Horne R, Tournier P, A system of viruses, in Cold Spring Harb. Symp. Quant. Biol., vol. 27, 1962, pp. 51–5.
103- King AMQ, Lefkowitz E, Adams MJ, Carstens EB, Virus Taxonomy: Ninth Report of the International Committee on Taxonomy of Viruses, Elsevier, 2011, p. 6.
104- MJ. Adams, EJ. Lefkowitz, AM. King e EB. Carstens, Recently agreed changes to the International Code of Virus Classification and Nomenclature., in Archives of Virology, vol. 158, nº 12, Dec 2013, pp. 2633–9.
105- As defined therein, “A species is the lowest taxonomic level in the hierarchy approved by the ICTV. A species is a monophyletic group of viruses whose properties can be distinguished from those of other species by multiple criteria.”
106- Delwart EL, Viral metagenomics, in Rev. Med. Virol., vol. 17, nº 2, 2007, pp. 115–31.
107- Virus Taxonomy 2013. International Committee on Taxonomy of Viruses. Retrieved on 24 December 2011.
108- ICTV Master Species List 2013 v2 Archiviato il 2 ottobre 2015 in Internet Archive.
This Excel file contains the official ICTV Master Species list for 2014 and lists all approved virus taxa. This is version 11 of the MSL published on 24 August 2014. Retrieved on 24 December 2014
109- Baltimore D, The strategy of RNA viruses, in Harvey Lect., 70 Series, 1974, pp. 57–74.
110- van Regenmortel MH, Mahy BW, Emerging issues in virus taxonomy, in Emerging Infect. Dis., vol. 10, nº 1, 2004, pp. 8–13.
111- Mayo MA, Developments in plant virus taxonomy since the publication of the 6th ICTV Report. International Committee on Taxonomy of Viruses, in Arch. Virol., vol. 144, nº 8, 1999, pp. 1659–66.
112- Komaroff AL, Is human herpesvirus-6 a trigger for chronic fatigue syndrome?, in J. Clin. Virol., 37 Suppl 1, 2006, pp. S39–46.
113- Chen C, Chiu Y, Wei F, Koong F, Liu H, Shaw C, Hwu H, Hsiao K, High seroprevalence of Borna virus infection in schizophrenic patients, family members and mental health workers in Taiwan, in Mol Psychiatry, vol. 4, nº 1, 1999, pp. 33–8.
114- Margolis TP, Elfman FL, Leib D, et al., Spontaneous reactivation of herpes simplex virus type 1 in latently infected murine sensory ganglia, in J. Virol., vol. 81, nº 20, 2007, pp. 11069–74.
115- Whitley RJ, Roizman B, Herpes simplex virus infections, in Lancet, vol. 357, nº 9267, 2001, pp. 1513–8.
116- Barton ES, White DW, Cathelyn JS, et al., Herpesvirus latency confers symbiotic protection from bacterial infection, in Nature, vol. 447, nº 7142, 2007, pp. 326–9, Bibcode:2007Natur.447..326B.
117- Bertoletti A, Gehring A, Immune response and tolerance during chronic hepatitis B virus infection, in Hepatol. Res., 37 Suppl 3, 2007, pp. S331–8.
118- Rodrigues C, Deshmukh M, Jacob T, Nukala R, Menon S, Mehta A, Significance of HBV DNA by PCR over serological markers of HBV in acute and chronic patients, in Indian journal of medical microbiology, vol. 19, nº 3, 2001, pp. 141–4.
119- Nguyen VT, McLaws ML, Dore GJ, Highly endemic hepatitis B infection in rural Vietnam, in Journal of Gastroenterology and Hepatology, vol. 22, nº 12, 2007, p. 2093.
120- Fowler MG, Lampe MA, Jamieson DJ, Kourtis AP, Rogers MF, Reducing the risk of mother-to-child human immunodeficiency virus transmission: past successes, current progress and challenges, and future directions, in Am. J. Obstet. Gynecol., vol. 197, 3 Suppl, 2007, pp. S3–9.
121- Sauerbrei A, Wutzler P, The congenital varicella syndrome, in Journal of perinatology : official journal of the California Perinatal Association, vol. 20, 8 Pt 1, 2000, pp. 548–54.
122- Garnett GP, Role of herd immunity in determining the effect of vaccines against sexually transmitted disease, in J. Infect. Dis., 191 Suppl 1, 2005, pp. S97–106.
123- Platonov AE, (The influence of weather conditions on the epidemiology of vector-borne diseases by the example of West Nile fever in Russia), in Vestn. Akad. Med. Nauk SSSR, nº 2, 2006, pp. 25–9.
124- Shors, p. 198.
125- Shors, pp. 199, 209.
126- Shors, p. 19.
127- Shors, pp. 193–194.
128- Shors, p. 194.
129- Shors, pp. 192–193.
130- Ranlet P, The British, the Indians, and smallpox: what actually happened at Fort Pitt in 1763?, in Pa Hist, vol. 67, nº 3, 2000, pp. 427–41.
- Van Rijn K, “Lo! The poor Indian!” colonial responses to the 1862–63 smallpox epidemic in British Columbia and Vancouver Island, in Can Bull Med Hist, vol. 23, nº 2, 2006, pp. 541–60.
- Patterson KB, Runge T, Smallpox and the Native American, in Am. J. Med. Sci., vol. 323, nº 4, 2002, pp. 216–22.
- Sessa R, Palagiano C, Scifoni MG, di Pietro M, Del Piano M, The major epidemic infections: a gift from the Old World to the New?, in Panminerva Med, vol. 41, nº 1, 1999, pp. 78–84.
- Bianchine PJ, Russo TA, The role of epidemic infectious diseases in the discovery of America, in Allergy Proc, vol. 13, nº 5, 1992, pp. 225–32, DOI:10.2500/108854192778817040, PMID 1483570. URL consultato il 19 dicembre 2014.
- Hauptman LM, Smallpox and American Indian; Depopulation in Colonial New York, in N Y State J Med, vol. 79, nº 12, 1979, pp. 1945–9.
- Fortuine R, Smallpox decimates the Tlingit (1787), in Alaska Med, vol. 30, nº 3, 1988, p. 109.
131- Collier, pp. 409-415.
132- Patterson KD, Pyle GF, The geography and mortality of the 1918 influenza pandemic, in Bull Hist Med., vol. 65, nº 1, 1991, pp. 4–21.
133- Johnson NP, Mueller J, Updating the accounts: global mortality of the 1918–1920 “Spanish” influenza pandemic, in Bull Hist Med, vol. 76, nº 1, 2002, pp. 105–15.
134- Gao F, Bailes E, Robertson DL, et al., Origin of HIV-1 in the Chimpanzee Pan troglodytes troglodytes, in Nature, vol. 397, nº 6718, 1999, pp. 436–441.
135- Shors, p. 447.
136- Mawar N, Saha S, Pandit A, Mahajan U, The third phase of HIV pandemic: social consequences of HIV/AIDS stigma & discrimination & future needs (PDF), in Indian J. Med. Res., vol. 122, nº 6, 2005, pp. 471–84.
137- Status of the global HIV epidemic (PDF), UNAIDS, 2008.
138- Towner JS, Khristova ML, Sealy TK, et al., Marburgvirus genomics and association with a large hemorrhagic fever outbreak in Angola, in J. Virol., vol. 80, nº 13, 2006, pp. 6497–516.
139- World Health Organisation report, 24 September 2014.
140- Einstein MH, Schiller JT, Viscidi RP, Strickler HD, Coursaget P, Tan T, Halsey N, Jenkins D, Clinician’s guide to human papillomavirus immunology: knowns and unknowns, in The Lancet Infectious Diseases, vol. 9, nº 6, 2009, pp. 347–56.
141- Shuda M, Feng H, Kwun HJ, Rosen ST, Gjoerup O, Moore PS, Chang Y, T antigen mutations are a human tumor-specific signature for Merkel cell polyomavirus, in Proceedings of the National Academy of Sciences of the United States of America, vol. 105, nº 42, 2008, pp. 16272–7.
142- Pulitzer MP, Amin BD, Busam KJ, Merkel cell carcinoma: review, in Advances in Anatomic Pathology, vol. 16, nº 3, 2009, pp. 135–44.
143- Koike K, Hepatitis C virus contributes to hepatocarcinogenesis by modulating metabolic and intracellular signalling pathways, in J. Gastroenterol. Hepatol., 22 Suppl 1, 2007, pp. S108–11.
144- Hu J, Ludgate L, HIV-HBV and HIV-HCV coinfection and liver cancer development, in Cancer Treat. Res., vol. 133, 2007, pp. 241–52.
145- Bellon M, Nicot C, Telomerase: a crucial player in HTLV-I-induced human T-cell leukemia, in Cancer genomics & proteomics, vol. 4, nº 1, 2007, pp. 21–5.
146- Schiffman M, Castle PE, Jeronimo J, Rodriguez AC, Wacholder S, Human papillomavirus and cervical cancer, in Lancet, vol. 370, nº 9590, 2007, pp. 890–907.
147- Klein E, Kis LL, Klein G, Epstein-Barr virus infection in humans: from harmless to life endangering virus-lymphocyte interactions, in Oncogene, vol. 26, nº 9, 2007, pp. 1297–305.
148- zur Hausen H, Novel human polyomaviruses—re-emergence of a well known virus family as possible human carcinogens, in International Journal of Cancer. Journal International Du Cancer, vol. 123, nº 2, 2008, pp. 247–50.
149- Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walters, Molecular Biology of the Cell; Fourth Edition, New York and London, Garland Science, 2002.
150- Ding SW, Voinnet O, Antiviral immunity directed by small RNAs, in Cell, vol. 130, nº 3, 2007, pp. 413–26.
151- Patton JT, Vasquez-Del Carpio R, Spencer E, Replication and transcription of the rotavirus genome, in Curr. Pharm. Des., vol. 10, nº 30, 2004, pp. 3769–77.
152- Jayaram H, Estes MK, Prasad BV, Emerging themes in rotavirus cell entry, genome organization, transcription and replication, in Virus Res., vol. 101, nº 1, 2004, pp. 67–81.
153- Greer S, Alexander GJ, Viral serology and detection, in Baillieres Clin. Gastroenterol., vol. 9, nº 4, 1995, pp. 689–721.
154- Matter L, Kogelschatz K, Germann D, Serum levels of rubella virus antibodies indicating immunity: response to vaccination of subjects with low or undetectable antibody concentrations, in J. Infect. Dis., vol. 175, nº 4, 1997, pp. 749–55.
155- Mallery DL, McEwan WA, Bidgood SR, Towers GJ, Johnson CM, James LC, McEwan, Bidgood, Towers, Johnson e James, Antibodies mediate intracellular immunity through tripartite motif-containing 21 (TRIM21), in Proceedings of the National Academy of Sciences of the United States of America, vol. 107, nº 46, novembre 2010, pp. 19985–90.
156- Cascalho M, Platt JL, Novel functions of B cells, in Crit. Rev. Immunol., vol. 27, nº 2, 2007, pp. 141–51.
157- Le Page C, Génin P, Baines MG, Hiscott J, Interferon activation and innate immunity, in Rev Immunogenet, vol. 2, nº 3, 2000, pp. 374–86.
158- Hilleman MR, Strategies and mechanisms for host and pathogen survival in acute and persistent viral infections, in Proc. Natl. Acad. Sci. U.S.A., 101 Suppl 2, 2004, pp. 14560–6.
159- Asaria P, MacMahon E, Measles in the United Kingdom: can we eradicate it by 2010?, in BMJ, vol. 333, nº 7574, 2006, pp. 890–5.
160- Lane JM, Mass vaccination and surveillance/containment in the eradication of smallpox, in Curr. Top. Microbiol. Immunol., vol. 304, 2006, pp. 17–29.
161- Arvin AM, Greenberg HB, New viral vaccines, in Virology, vol. 344, nº 1, 2006, pp. 240–9.
162- Pastoret PP, Schudel AA, Lombard M, Conclusions—future trends in veterinary vaccinology, in Rev. – Off. Int. Epizoot., vol. 26, nº 2, 2007, pp. 489–94, 495–501, 503–9.
163- Palese P, Making better influenza virus vaccines?, in Emerging Infect. Dis., vol. 12, nº 1, 2006, pp. 61–5.
164- Thomssen R, Live attenuated versus killed virus vaccines, in Monographs in allergy, vol. 9, 1975, pp. 155–76.
165- McLean AA, Development of vaccines against hepatitis A and hepatitis B, in Rev. Infect. Dis., vol. 8, nº 4, 1986, pp. 591–8.
166- Casswall TH, Fischler B, Vaccination of the immunocompromised child, in Expert review of vaccines, vol. 4, nº 5, 2005, pp. 725–38.
167- Barnett ED, Wilder-Smith A, Wilson ME, Yellow fever vaccines and international travelers, in Expert Rev Vaccines, vol. 7, nº 5, 2008, pp. 579–87.
168- Magden J, Kääriäinen L, Ahola T, Inhibitors of virus replication: recent developments and prospects, in Appl. Microbiol. Biotechnol., vol. 66, nº 6, 2005, pp. 612–21.
169- Mindel A, Sutherland S, Genital herpes — the disease and its treatment including intravenous acyclovir, in J. Antimicrob. Chemother., 12 Suppl B, 1983, pp. 51–9.
170- Witthöft T, Möller B, Wiedmann KH, et al., Safety, tolerability and efficacy of peginterferon alpha-2a and ribavirin in chronic hepatitis C in clinical practice: The German Open Safety Trial, in J. Viral Hepat., vol. 14, nº 11, 2007, pp. 788–96.
171- Rudin D, Shah SM, Kiss A, Wetz RV, Sottile VM, Interferon and lamivudine vs. interferon for hepatitis B e antigen-positive hepatitis B treatment: meta-analysis of randomized controlled trials, in Liver Int., vol. 27, nº 9, 2007, pp. 1185–93.
172- sciencedirect.com/topics/immunology-and-microbiology/human-virome.
173- Francis, J.W., Ingle, M., and Wood, T.C., Bacteriophages as beneficial regulators of the mammalian Microbiome, Proc. Int. Conf. Creationism 8:152–157, 2018.
174- Barber, M.R. et al., Association of RIG-I with innate immunity of ducks to influenza, PNAS 107(13):5913–5918, 2010.
175- Terborg, P., The ‘VIGE-first hypothesis–how easy it is to swap cause and effect, J. Creation 27(3):105–112, 2013. (VIGE = Variation-Inducing Genetic Element).

L’ha ripubblicato su The sense.
"Mi piace""Mi piace"