- Piccolo preambolo
Quello che verrà riportato in questo e negli altri articoli della serie che seguiranno, è il frutto di un lavoro di ricerca ed estrapolazione di informazioni che trovano la loro origine nel ottimo lavoro di Chest Rockwell sull’uso del Ormone della Crescita a fini ipertrofici intitolato “The Most Effective Growth Hormone Protocol for Hypertrophy”.
Nota introduttiva

Se volete un metodo altamente efficace per spingere un Bodybuilder a guardarvi prima con confusione e, in seguito, con totale irritazione, basta che usiate qualsiasi variazione della seguente affermazione:
L’Ormone della Crescita determina un aumento significativo della massa corporea magra, è altamente anabolico, ma non causa la crescita del tessuto muscolare…
Nel corso di questi articoli, spiegherò come questa affermazione sia precisa al 100% nonostante sembri un po’ assurdo ad una prima lettura. Per impostare alcuni parametri in anticipo, si parlerà di AAS e della loro relazione sinergica con il GH, ma ci saranno solo alcune menzioni sull’Insulina. Questa serie di articoli rappresenta già di suo un’impresa enorme. Penso che per impostare in modo corretto l’argomento, il tema GH/Insulina meriti un articolo a parte (cosa parzialmente già fatta) a causa delle immense complessità che esistono nella loro correlazione. Non ho nemmeno intenzione di toccare l’argomento dei secretagoghi del GH, dei peptidi sperimentali o di altri analoghi in modo che ci si possa concentrare principalmente sui fondamentali della questione GH ed Ipertrofia. Se non diversamente specificato nell’articolo, si parlerà esplicitamente dell’Ormone della Crescita di origine endogena o ricombinante (esogeno).
E, infine, questi articoli sono rivolti esclusivamente agli uomini. Mi dispiace per le atlete, ma i maschi sono molto più sensibili agli effetti anabolici della supplementazione con GH rispetto alle donne, data la spiccata natura sessualmente dimorfica del GH.(1) Quindi, a meno che non dichiari specificatamente il contrario, le informazioni che seguiranno saranno orientate verso l’uomo. In futuro è probabile che realizzerò un articolo in merito dedicato alle donne.
Introduzione all’Anabolismo e alla Crescita Muscolare
La prima cosa da fare è conoscere concisamente le corrette definizioni di termini quali anabolismo, ipertrofia e iperplasia. Li vedo spesso usati quasi in modo intercambiabile, ma ci sono alcune differenze chiave. Ad esempio, solo perché qualcosa è anabolico non significa automaticamente che causerà la crescita del tessuto muscolare. Viceversa solo perché qualcosa è catabolico non significa automaticamente che non possa contribuire alla crescita del tessuto muscolare in modo positivo.

L’anabolismo può essere definito come qualsiasi stato in cui la ritenzione d’azoto nella massa magra è positiva, sia attraverso la stimolazione della sintesi proteica che attraverso la soppressione dei tassi di proteolisi.(2) Il primo chiarimento da fare in riferimento alla mia precedente affermazione è che la misurazione della massa corporea magra non include soltanto la massa muscolare ma, per esempio, anche gli organi, le ossa e l’acqua ivi contenuta (3), fattore quest’ultimo soggetto all’azione dell’Ormone della Crescita. Quindi, leggere uno studio nel quale si afferma che la massa corporea magra è aumentata in seguito al trattamento con GH, non vuol dire che ci si riferisca ad un aumento della massa muscolare.
L’apparato muscolare è un tessuto plastico molto complesso e in grado di adattarsi alle mutevoli esigenze funzionali alle quali viene sottoposto. Quando parliamo di aumento della massa muscolare, stiamo parlando principalmente di un evento che si verifica attraverso due meccanismi primari – ipertrofia e iperplasia.

L’ipertrofia è il processo attraverso il quale l’aumento della massa muscolare si verifica tramite l’aumento delle dimensioni dell’area della sezione trasversa di una fibra muscolare esistente (CSA). Il processo ipertrofico è mediato da molti fattori come con l’ipertrofia indotta dall’esercizio, di particolare interesse per i Bodybuilder, essendo essa mediata da una combinazione di tensione meccanica, danno muscolare e stress metabolico.(4)

L’iperplasia, ivece, è il processo mediante il quale l’aumento della massa muscolare viene raggiunto attraverso un incremento del numero effettivo di fibre muscolari. È generalmente accettato che, negli esseri umani, il numero di fibre all’interno del muscolo sia geneticamente predeterminato e fissato durante il periodo perinatale.(5) Esistono alcuni studi svolti su animali i quali hanno dimostrato che l’iperplasia può verificarsi (6-7), spesso in condizioni di test unici, ma il tentativo di dedurre da ciò che essa si possa verificare negli esseri umani (8-9) è altamente speculativo nella migliore delle ipotesi. Anche se l’iperplasia si verifica nell’apparato muscolare umano, è molto probabile che sia solo un fattore minore che determina la massa complessiva. Tuttavia, a causa di una cattiva comprensione (se così la vogliamo chiamare) degli studi prima citati spesso vengono formulate affermazioni definitive secondo cui il GH causa iperplasia. Vale quindi la pena di ribadire che questi tipi di affermazioni dovrebbero essere considerate nient’altro che speculative.
La scoperta dell'”Ormone della Crescita”

Sono trascorsi oltre 100 anni da quando Harvey Cushing suppose per la prima volta l’esistenza di un “Ormone della Crescita” (10), e questo ormone venne successivamente isolato, identificato ed estratto dall’ipofisi umana negli anni ’40.(11) Nel decennio successivo, si fece largo un’ipotesi cardine secondo cui la “crescita” non era direttamente attribuibile al GH, ma piuttosto ad un gruppo di fattori serici regolati dall’espressione del GH.(12) Questi fattori serici sono stati in seguito chiamati fattori di solfatazione, termine volto ad indicare sostanze controllate dal GH che stimolavano l’assorbimento di solfato nella cartilagine e nei tessuti. Questa ipotesi ha cercato di aiutare i ricercatori a conciliare meglio il modo in cui la crescita somatica veniva regolata da una sostanza secreta dall’Ipofisi, mentre allo stesso tempo rinforzava il fatto che questa sostanza ipofisaria non agiva direttamente sui suoi tessuti bersaglio per promuovere la crescita.(13-14)
Nei decenni successivi, molti esperimenti hanno dimostrato l’ampia varietà di funzioni possedute da questa famiglia di fattori di solfatazione e il termine “somatomedina” è stato proposto per includere tutti i membri di questa famiglia.(15) È interessante notare che l’ipotesi originale che descrive la regolazione di questi fattori di solfatazione mediati dal GH è ancora oggi generalmente indicata come “l’ipotesi della somatomedina”.(16) L’ipotesi originale affermava che la crescita somatica è causata dall’azione del GH a livello epatico, dove stimola la sintesi di IGF-1 che viene successivamente rilasciato agendo sui tessuti bersaglio con modello endocrino. Questa ipotesi è rimasta il modello accettato per decenni fino a quando non sono stati identificati i ruoli autocrini del IGF (17-18) insieme agli effetti diretti che il GH ha nella crescita ossea.(19-20)Per riconciliare queste nuove scoperte, l’ipotesi originaria è stata leggermente modificata prendendo il nome di “Teoria del Doppio Effetto”, che ha definito sia un ruolo autocrino che endocrino del IGF-1.(21)
Tornando indietro di qualche tempo, verso la fine degli anni ’70, l’identità chimica di questi fattori di solfatazione era più intimamente riconosciuta come la manifestazione di due peptidi con un’elevatissima somiglianza con l’Insulina e quindi ribattezzati “fattori di crescita isulino-simili (IGF)”.(22-24) Fu all’incirca nello stesso periodo nel quale vennero identificate anche le proteine leganti l’IGF (IGFBP), e di conseguenza la conoscenza della biologia dell’IGF-1 decollò ad un tasso esponenziale.(25)

Nel frattempo, gli estratti ipofisari umani diventarono disponibili tramite l’estrazione dai cadaveri e gli esperimenti iniziali svolti su animali ed esseri umani mostrarono quanto complesse fossero realmente le azioni del GH umano. (26-33) La pratica dell’uso di questi estratti ipofisari venne interrotta dai medici in seguito alla comparsa della malattia di Creutzfeldt-Jakob (CJD) in pazienti a cui era stato precedentemente somministrato il GH contenuto nel Ipofisi estratta dai cadaveri.(34) La CJD è una malattia cerebrale particolarmente sgradevole e universalmente fatale, con la stragrande maggioranza dei soggetti affetti che muoiono poco dopo la sua diagnosi.

Fortunatamente, nel 1985, nello stesso periodo in cui questi casi di CJD cominciarono a fare notizia, la FDA approvò il primo GH ricombinante sintetico (rHGH) per l’utilizzo su soggetti con deficit dell’Ormone della Crescita. Questa versione di rHGH è stata prodotta dalla Genentech e denominata Protropin.(35-36) Vale la pena notare che, analizzando la composizione dei vecchi farmaci contenenti GH si può osservare che erano costituiti da una catena di 192 amminoacidi (met-hGH) rispetto al rHGH che consiste in una catena di 191 amminoacidi.(37) In ogni caso, con l’rHGH, ora di facile disponibilità, è stata inaugurata un’era completamente nuova, con condizioni cliniche molto più sicure, per il numero in continua crescita di pazienti trattati.
Effetti dell’Ormone della Crescita sulla sintesi proteica
All’inizio dell’articolo, ho definito a grandi linee cos’è l’anabolismo ed ho anche affermato che l’Ormone della Crescita possiede una natura anabolica. Adesso, descriverò ciò che rende anabolizzante l’Ormone della Crescita e approfondirò parte della letteratura scientifica esistente sull’argomento.
Nel corso degli anni, il GH è stato ampiamente studiato in diversi modi. La maggior parte degli studi svolti, quando considerati nel loro insieme, suggeriscono che il GH sia anabolico. Più specificamente, il GH è anabolico perché stimola la sintesi proteica di tutto il corpo con o nessun effetto, o un effetto soppressivo, sui tassi di degradazione proteica. [38] Tuttavia, quando si approfondisce l’argomento, le cose diventano un po’ meno chiare dal momento che i risultati degli studi tendono ad essere diversi. I diversi risultati sono un riflesso diretto dell’ immensa complessità del GH.

Il GH esplica i suoi effetti sulla sintesi proteica legandosi prima con il suo recettore specifico (GHR) e successivamente aumentando la trascrizione del gene muscolare attraverso i percorsi di segnalazione a valle, in definitiva attivando la segnalazione del mTOR. [39-40] Questi effetti si manifestano in acuto, spesso si verificano in pochi minuti e sono di natura simile all’Insulina, usando molte delle stesse vie anaboliche. [41-44] La rapida comparsa di questi cambiamenti metabolici legati alle proteine suggerisce che essi siano direttamente causati dal GH e non secondariamente mediati tramite l’IGF-1 [45]. L’impatto del GH sulla proteolisi, d’altro canto, è molto probabilmente di natura indiretta. A detta di tutti, ciò ha più a che fare con i suoi effetti inibitori sull’Insulina, che è stata vista avere effetti diretti sulla proteolisi.[46]

Ora, poiché sarete interessati principalmente alla crescita muscolare, riporterò come il GH influenza specificamente i tassi di sintesi delle proteine muscolari (MPS). Vi sono numerosi studi in letteratura nei quali il GH è stato somministrato a soggetti adulti sani senza aver mostrato alcun impatto sui tassi di MPS. [45,47-52] Ciò che risulta affascinante di questi risultati è che un paio di studi includevano anche una allenamento di resistenza, sebbene, nella fattispecie, non sono stati comunque riscontrati aumenti nei tassi di MPS locali. Al contrario, ci sono una serie di studi che hanno riportato di aumenti nei tassi di MPS senza cambiamenti significativi nei tassi di sintesi proteica dell’intero corpo. [53-55]
Ci sono molte ragioni per cui questi risultati appaiono non del tutto coerenti all’interno del corpo della letteratura scientifica. Uno dei motivi principali è rappresentato dal modo in cui gli studi sono stati svolti per quanto riguarda il tipo di somministrazione del GH (ad esempio, le concentrazione di dosaggio, se somministrato localmente o in modo sistemico, nonché se l’ormone è stato somministrato in modo pulsatile o costante). Alcune delle altre ragioni includono come è stata misurata la sintesi proteica, se i soggetti esaminati erano a digiuno o nutriti, che tipo di muscolo scheletrico è stato esaminato e, anche, per quanto tempo è durato lo studio. Come menzionato in precedenza, molti degli effetti che il GH ha sul metabolismo proteico avvengono in acuto.
Sebbene questa serie di articoli è principalmente incentrata sull’ipertrofia, ritengo comunque che valga la pena di discutere le differenze che il GH ha sul metabolismo delle proteine in condizioni di digiuno e nutrizione. Ciò aiuterà ad avere un quadro generale più chiaro di come il comportamento di questo ormone sia spesso il risultato diretto dell’ambiente nel quale è introdotto. Come ho spiegato dettagliatamente nell’articolo dedicato a GH e lipolisi, la secrezione di GH subisce un aumento durante periodi prolungati di digiuno. Questo è un meccanismo di sopravvivenza, con l’obiettivo principale di conservare preziosi pool amminoacidici immagazzinati prevenendo la degradazione delle proteine. [56] Questo stesso comportamento di risparmio di proteine può essere visto, in misura minore, in soggetti trattati con GH e sottoposti a severe restrizioni dietetiche [57], soggetti obesi sottoposti a vari tipi di dieta ipocalorica [58-61] e soggetti privati di proteine dietetiche [ 62].

È stato dimostrato che l’IGF-1 inibisce allo stesso modo la disgregazione proteica a livello sistemico [63], il che avrebbe senso a causa della stretta co-relazione con il GH. Quando gli amminoacidi e l’Insulina vengono somministrati ai soggetti esaminati, già sottoposti a somministrazione di IGF-1, è stato dimostrato, sia negli uomini che negli animali, che i tassi di sintesi proteica aumentano a livello sistemico [64-65]. Vale la pena notare che l’IGF-1 è bifasico nel senso che quando è somministrato ad alto dosaggio e, di conseguenza, i livelli serici diventano elevati, il suo comportamento cambia passando da un azione “GH-simile” ad una “insulino-simile”. Tratterò nel dettaglio l’argomento in seguito.
Per riassumere, il GH è molto adatto per prevenire la degradazione proteica, e lo fa in una vasta gamma di condizioni alimentari a ristretto apporto calorico. Tuttavia, in presenza di un apporto energetico sufficiente, il suo comportamento cambia. L’effetto principale del GH sul metabolismo proteico è volto dapprima a creare un ambiente con una ossidazione amminoacidica ridotta [47,66] e successivamente ad aumentare la sintesi proteica sistemica. [67]
Il ruolo di GH e IGF-1 nella crescita postnatale

È noto che il GH regola la crescita postnatale e che questi effetti di promozione della crescita sono principalmente mediati dall’IGF-1. [68-69] Tuttavia, giusto per ribadirlo, è necessario chiarire che questi effetti di induzione della crescita non sono esclusivi dell’ipertrofia muscolare. La crescita lineare di un organismo include cambiamenti nell’apparato scheletrico, negli organi e nei muscoli.
Per riportare esempi di un certo rilievo sull’importanza che GH e IGF-1 hanno sulla crescita postnatale, basta osservare gli individui con mutazioni o disturbi correlati all’Asse GH/IGF. Una revisione dettagliata su questo tema va oltre lo scopo di questo articolo ma, in generale, e penso sia abbastanza risaputo, i disturbi che sopprimono/inibiscono l’Asse GH/IGF in soggetti in giovane età si caratterizzano in una bassa statura di questi mentre i disturbi che stimolano l’Asse GH/IGF si caratterizzano nel gigantismo. [70-71]

La stragrande maggioranza degli effetti del GH sulla promozione della crescita sono mediati tramite l’IGF-1, tuttavia ci sono una serie di processi che sono GH-mediati o IGF-indipendenti. L’esempio più eloquente di questo è rappresentato nei modelli animali in cui i topi “knockout” mutati e deficitari di GH e IGF-1 hanno mostrato una maggiore gravità nel ritardo della crescita rispetto ai “knockout” GH-deficienti o IGF-deficienti [72]. Ma osserviamo nel dettaglio alcuni degli effetti più specifici che sono stati identificati nei modelli umani.
Il primo è legato alla steatosi epatica, nota anche come “malattia del fegato grasso” [73]. È stato dimostrato sia negli esseri umani con la sindrome di Laron che negli animali con soppressione del GHR che questa condizione può ancora verificarsi in presenza di livelli di IGF-1 soppressi[74]. La sindrome di Laron fornisce alcune intuizioni piuttosto uniche sul sistema GH/IGF-1 a causa del fatto che è causata da una mutazione nel GHR che si traduce in livelli significativamente bassi di IGF-1 endocrino, dal momento che al GH viene impedito di legarsi al suo sito recettore e di stimolare efficacemente la produzione di IGF-1.

Un’altra azione specifica del GH è legata alla sua capacità di migliorare lo sviluppo del follicolo preantrale ovarico. In effetti, il GH è stato anche recentemente oggetto di studi per i suoi potenziali miglioramenti sulla fertilità femminile. I risultati indicano che alcuni gruppi che utilizzano la fecondazione in vitro (FIV) sembrano beneficiare della somministrazione di GH. [75-76] Anche i modelli animali con deficit di GHR hanno mostrato un numero inferiore di follicoli primari preantrali e antrali rispetto ai loro simili di controllo.

Una delle prime e più interessanti scoperte riguardanti l’azione del GH , è stata il ruolo specifico del GH nel promuovere la crescita ossea longitudinale attraverso i suoi effetti sulla generazione dei condrociti (cellule cartilaginee) nella regione delle placche di crescita epifisaria. [19-20,77-80]. Il GH ha in realtà due ruoli nella promozione della crescita ossea longitudinale; sia attraverso i suddetti effetti sulla generazione dei condrociti nella piastra di crescita che attraverso un ruolo mediato dall’IGF-1 nella promozione dell’ipertrofia dei condrociti.[81] Vale la pena notare che i livelli endocrini di IGF-1 completamente intatti non sono nemmeno una necessità quando si tratta di crescita ossea postnatale. Infatti, fino a quando sono presenti almeno il 10-20% dei livelli di IGF-1 endocrino circolante, la combinazione di IGF-1 e GH autocrini può comunque garantire la normale crescita ossea postnatale. [82] Ciò è probabilmente dovuto ai ruoli sovrapposti di IGF-1 autocrino ed endocrino in relazione alla crescita ossea longitudinale. [83]
Il GH promuove un aumento dei tassi di fusione delle cellule muscolari tardive che possono avere la capacità di aumentare la dimensione delle fibre muscolari in un modo completamente indipendente dalla sovraregolazione dell’IGF-1.[84] Utilizzando una nuova tecnica di sperimentazione su cellule animali, i ricercatori sono stati in grado di dimostrare che il GH promuove la fusione dei mioblasti con i miotubi nascenti senza un aumento dell’espressione effettiva dell’mRNA del IGF-1. I miotubi nascenti sono presenti negli stadi successivi della fusione delle cellule muscolari [85] e il GH ha dimostrato di aumentare il numero di nuclei per miotubo.
La relazione tra secrezione di GH e IGF-1

L’Ormone della Crescita è noto per aumentare i livelli di IGF-1 circolante così come la sintesi locale di IGF-1, in modo autocrino. Entrambe queste azioni giocano un ruolo fondamentale nella regolazione della massa muscolare e, quindi, in conseguenza di ciò, risulta utile comprendere meglio come la secrezione di GH porta ad un aumento dei livelli endocrino e autocrino di IGF-1.
La stragrande maggioranza dell’Ormone della Crescita negli adulti sani è secreto dalla ghiandola pituitaria e, più specificamente, dalle cellule somatotrope nel lobo anteriore mediate dal fattore di trascrizione Prophet of Pit-1 (PROP1).[86-87] Il GH può anche essere sintetizzato localmente in molti tessuti come il cervello, le cellule immunitarie, il tessuto mammario, i denti e la placenta che sono tutti al di fuori della regolazione dell’ipofisi. [88] Questo supporta l’idea secondo cui il GH abbia ruoli autocrini oltre ai suoi già consolidati ruoli endocrini.
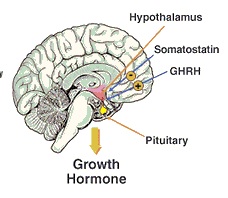
Il GH è secreto in modo pulsatile in tutte le specie [89-90] e questo modello secretorio gioca un ruolo fisiologico importante in tutte le sue caratteristiche, da quelle dimorfiche sessuali all’RNA del IGF-1, di cui scopriremo di più in seguito. I giovani maschi adulti sani secernono tra 0,4-0,5mg di GH ogni 24 ore e molte di queste secrezioni si verificano come “impulsi all’interno di impulsi”. [91] Normalmente, ci sono circa 10-12 impulsi secretorie ogni giorno con gli uomini che presentano un modello di impulso significativamente più regolare rispetto alle donne. Nei maschi, il GH viene secreto in modo episodico, con la ben nota grande ondata serale che si verifica in prossimità dell’inizio del sonno ad onde lente. I maschi hanno anche secrezioni più contenute che si verificano poche ore dopo aver consumato i pasti.[92-94] Le femmine hanno livelli ematici inter-secretori più elevati, in particolare nella fase follicolare del ciclo mestruale, con impulsi di GH più frequenti durante il giorno e un impulso notturno significativamente più basso rispetto ai maschi [95-96]. Non è del tutto chiaro perché esista questo schema secretivo sessualmente dimorfico.

La secrezione di GH è regolata in un modo molto complesso che coinvolge la partecipazione di diversi neurotrasmettitori, così come di feedback sia ormonali che metabolici. È regolato principalmente in modo positivo dal GHRH (Ormone di Rilascio della Somatotropina o Somatorelina) [97], e in modo negativo dalla SRIF (Somatostatina). Entrambi questi peptidi sono prodotti all’interno dell’ipotalamo. Infatti, oltre al suo ruolo di base nella produzione ormonale, l’ipotalamo monitora costantemente il rapporto GHRH/SRIF e di conseguenza opera un controllo sulla secrezione ipofisaria. [98]
Oltre alla sua funzione primaria di stimolazione della secrezione di GH, il GHRH svolge anche un ruolo essenziale nella proliferazione e nello sviluppo delle suddette cellule somatotrope. Infatti, in un sistema con GHRH alterato o assente, è stata osservata ipoplasia anteriore dell’ipofisi che è probabilmente il risultato di un alterato sviluppo somatotropo.[99-100] Gli esseri umani con il GHRH soppresso per azione di un antagonista hanno mostrato un rilascio pulsatile di GH gravemente compromesso e una risposta soppressa del GH al GHRH [101], quindi è chiaramente una componente vitale all’interno dell’Asse GH/IGF-1.
La SRIF, il principale regolatore negativo della secrezione di GH, sopprime il TSH. Inoltre, in misura minore, sopprime sia la Prolattina che l’Ormone Adrenocorticotropo [97]. Tutti questi ormoni sono noti per avere strette relazioni con l’Asse GH/IGF-1. La SRIF ha un’emivita breve di circa 2-3 minuti nel siero e viene quindi rapidamente inattivata dalle peptidasi tissutali. Durante la sua vita attiva, sopprime non solo il rilascio spontaneo di GH, ma anche la risposta del GH a tutti gli stimoli esterni incluso il GHRH, l’ipoglicemia, l’Arginina e l’esercizio fisico solo per nominarne alcuni. I suoi effetti soppressivi apparentemente sono limitati all’ampiezza della liberazione basale e pulsatile di GH, poiché non è stato dimostrato che alteri la frequenza degli impulsi di GH.[102]

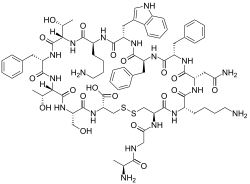
Il GH circolante è in gran parte legato alle proteine di trasporto chiamate GHBP o proteine leganti l’ormone della crescita. Queste proteine carrier sono essenzialmente una forma solubile e troncata del dominio extracellulare del GHR – GHR circolanti mobili che non si trovano all’interno delle membrane cellulari.[103] Il GH nel flusso ematico può anche esistere in forma libera o non legata e il rapporto tra frazione legata e non legata dipende dal modello pulsatile della sua secrezione. [104] I complessi di GH circolante nell’uomo possono essere costituiti da una delle due distinte forme di GH (22-kDa e 20-kDa), con circa il 90% rappresentato dalla forma molecolare da 22-kDa nonostante le prime stime abbiano ridotto tale numero.[105-106] Le moderne metodologie utilizzate nei test antidoping per la rilevazione indiretta del GH possono effettivamente sfruttare i rapporti in tempo reale delle molecole di GH circolanti all’interno del sistema di un atleta per determinare se questo ha usato rHGH nelle ultime 24-36 ore prima del test. La molecola dell’Ormone della Crescita, nella sua forma corretta da 22-kDa, è raffigurata di seguito. [107]:

In definitiva, questo GH circolante si lega al GHR, recettore dell’Ormone della Crescita appartenente alla superfamiglia delle proteine transmembrana presenti in tutte le cellule del corpo e che include il recettore della Prolattina e un certo numero di recettori delle citochine [108-110]. I livelli sulla superficie cellulare, o la densità recettoriale, dei GHR sono il determinante principale dell’affinità di legame del GH con le cellule. La traslocazione del GHR, cioè il recettore che si sposta dal nucleo di una cellula alla sua membrana esterna, è direttamente inibita dall’IGF-1 – che è uno dei molti meccanismi di feedback che esistono tra questi ormoni strettamente correlati. Mediante l’inibizione della traslocazione dei GHR, l’IGF-1 contribuisce direttamente ad abbassare la reattività di queste cellule a uno stimolo esterno di GH. [111]
Una analisi profonda dell’attivazione della Tirosina Chinasi, delle vie di segnalazione a valle e dell’espressione genica va oltre lo scopo di questo articolo. Quindi, mi limiterò a trattarlo superficialmente. E’ necessario comunque toccare alcuni dei punti più importanti della segnalazione intracellulare per comprendere veramente le basi del processo ipertrofico e del perché esiste sia sinergie composte che potenziali strategie ottimizzate per massimizzare il processo.

Come già accennato, i GHR esistono sulle membrane cellulari come omodimeri preformati e inattivi. Questo significa che il GHR ha due dimeri identici del recettore della proteina, e questi omodimeri saranno sempre accoppiati al JAK2 quando sono privi di attività enzimatica. Questo accoppiamento al JAK2 provoca un’azione inibitoria complessiva sul recettore. [112-113] In altre parole, il GHR rimane dormiente finché non viene attivato come parte del processo di legame GH/GHR. Quando una molecola di GH si lega al GHR, si verifica un cambiamento strutturale all’interno del GHR che si traduce in movimento effettivo dei domini intracellulari del recettore separatamente l’uno dall’altro. Questo smorza quell’azione inibitoria data dal JAK2 e consente loro di attivarsi l’un l’altro.[114-116]
Successivamente, la molecola di GH si lega sequenzialmente a uno dei due omodimeri di GHR e il completamento di questo processo di legame facilita le interazioni con il secondo omodimero. Dopo questo, i domini intracellulari di questo dimero-GHR appena formato subiscono una rotazione effettiva. La rotazione del nuovo dimero-GHR consente ai domini chinasi del JAK2 di essere in contatto l’uno con l’altro, consentendo loro di transactivare e ciascuno successivamente si lega a una molecola di JAK2. [117-118] Ciascuna molecola di JAK2 eseguirà quindi la fosforilazione incrociata (attivazione) dei residui di Tirosina, e sono proprio questi residui che formano “punti di attracco” per molte delle diverse molecole di segnalazione che costituiscono le vie di segnalazione a valle, e alla fine portano all’espressione genica. [114,118 -120] Uno dei più importanti percorsi a valle di maggior interesse per l’argomento specifico che qui vado trattando è il percorso JAK-STAT. Questo percorso è di vitale importanza sia per la trascrizione epatica di IGF-1 dal GH che per molti dei processi anabolici mediati dal GH all’interno del tessuto muscolare.
Nella seconda parte di questa serie di articoli mi occuperò più nel dettaglio del IGF-1, della “somatopausa” e della reale efficacia dell’uso del GH nello sport.
Stay tuned!
Gabriel Bellizzi
Riferimenti:
- The Most Effective Growth Hormone Protocol for Hypertrophy – by Chest Rockwell
- Dall R, Longobardi S, Ehrnborg C, Keay N, Rosén T, Jørgensen JO, Cuneo RC,Boroujerdi MA, Cittadini A, Napoli R, Christiansen JS, Bengtsson BA, Sacca L,Baxter RC, Basset EE, Sönksen PH. The effect of four weeks of supraphysiological growth hormone administration on the insulin-like growth factor axis in women and men. GH-2000 Study Group. J Clin Endocrinol Metab. 2000 Nov;85(11):4193-200.
- Kuhn CM. Anabolic steroids. Recent Prog Horm Res. 2002;57:411-34. Review.
- Ribeiro SML, Kehayias JJ. Sarcopenia and the Analysis of Body Composition. Advances in Nutrition. 2014;5(3):260-267.
- Schoenfeld BJ. The mechanisms of muscle hypertrophy and their application to resistance training. J Strength Cond Res. 2010 Oct;24 (10):2857-72.
- Stickland NC. Muscle development in the human fetus as exemplified by m.sartorius: a quantitative study. J Anat. 1981 Jun;132(Pt 4):557-79.
- Antonio J, Gonyea WJ. Skeletal muscle fiber hyperplasia. Med Sci Sports Exerc. 1993 Dec;25(12):1333-45. Review.
- Fernández AM, Dupont J, Farrar RP, Lee S, Stannard B, Le Roith D.Muscle-specific inactivation of the IGF-I receptor induces compensatory hyperplasia in skeletal muscle. J Clin Invest. 2002 Feb;109(3):347-55.
- Kadi F, Thornell LE. Training affects myosin heavy chain phenotype in the trapezius muscle of women. Histochem Cell Biol. 1999 Jul;112(1):73-8.
- D’Antona G, Lanfranconi F, Pellegrino MA, Brocca L, Adami R, Rossi R, Moro G, Miotti D, Canepari M, Bottinelli R.Skeletal muscle hypertrophy and structure and function of skeletal muscle fibres in male body builders. J Physiol. 2006 Feb 1;570(Pt 3):611-27.
- Cohen-Gadol AA, Liu JK, Laws ER Jr. Cushing’s first case of transsphenoidal surgery: the launch of the pituitary surgery era. J Neurosurg. 2005 Sep;103(3):570-4.
- Li CH, Evans HM. THE ISOLATION OF PITUITARY GROWTH HORMONE. Science. 1944 Mar 3;99(2566):183-4.
- SALMON WD Jr, DAUGHADAY WH. A hormonally controlled serum factor which stimulates sulfate incorporation by cartilage in vitro. J Lab Clin Med. 1957 Jun;49(6):825-36.
- Daughaday WH, Reeder C. Synchronous activation of DNA synthesis in hypophysectomized rat cartilage by growth hormone. J Lab Clin Med. 1966 Sep;68(3):357-68.
- Garland JT, Lottes ME, Kozak S, Daughaday WH. Stimulation of DNA synthesis in isolated chondrocytes by sulfation factor. Endocrinology. 1972 Apr;90(4):1086-90.
- Daughaday WH, Hall K, Raben MS, Salmon WD Jr, van den Brande JL, van Wyk JJ.Somatomedin: proposed designation for sulphation factor. Nature. 1972 Jan 14;235(5333):107.
- Le Roith D, Bondy C, Yakar S, Liu JL, Butler A. The somatomedin hypothesis: 2001. Endocr Rev. 2001 Feb;22(1):53-74. Review.
- D’Ercole AJ, Applewhite GT, Underwood LE. Evidence that somatomedin is synthesized by multiple tissues in the fetus. Dev Biol. 1980 Mar 15;75(2):315-28.
- Han VK, Lund PK, Lee DC, D’Ercole AJ. Expression of somatomedin/insulin-like growth factor messenger ribonucleic acids in the human fetus: identification, characterization, and tissue distribution. J Clin Endocrinol Metab. 1988 Feb;66(2):422-9.
- Isaksson OG, Jansson JO, Gause IA. Growth hormone stimulates longitudinal bone growth directly. Science. 1982 Jun 11;216 (4551):1237-9.
- Isaksson OG, Lindahl A, Nilsson A, Isgaard J. Mechanism of the stimulatory effect of growth hormone on longitudinal bone growth. Endocr Rev. 1987 Nov;8(4):426-38. Review.
- Green H, Morikawa M, Nixon T. A dual effector theory of growth-hormone action. Differentiation. 1985;29(3):195-8. Review.
- Rinderknecht E, Humbel RE. The amino acid sequence of human insulin-like growth factor I and its structural homology with proinsulin. J Biol Chem. 1978 Apr 25;253(8):2769-76.
- Klapper DG, Svoboda ME, Van Wyk JJ. Sequence analysis of somatomedin-C: confirmation of identity with insulin-like growth factor I. Endocrinology. 1983 Jun;112(6):2215-7.
- Daughaday WH, Rotwein P. Insulin-like growth factors I and II. Peptide, messenger ribonucleic acid and gene structures, serum, and tissue concentrations. Endocr Rev. 1989 Feb;10(1):68-91. Review.
- Hintz RL, Liu F. Demonstration of specific plasma protein binding sites for somatomedin. J Clin Endocrinol Metab. 1977 Nov;45(5):988-95.
- BECK JC, McGARRY EE, DYRENFURTH I, VENNING EH. The metabolic effects of human and monkey growth hormone in man. Ann Intern Med. 1958 Nov;49(5):1090-105.
- IKKOS D, LUFT R, GEMZELL CA. The effect of human growth hormone in man. Lancet. 1958 Apr 5;1(7023):720-1.
- RABEN MS, HOLLENBERG CH. Effect of growth hormone on plasma fatty acids. J Clin Invest. 1959 Mar;38(3):484-8. PubMed PMID: 13641397
- RABEN MS. Growth hormone. 1. Physiologic aspects. N Engl J Med. 1962 Jan 4;266:31-5.
- RABEN MS. Growth hormone. 2. Clinical use of human growth hormone. N Engl J Med. 1962 Jan 11;266:82-6 concl.
- ZIERLER KL, RABINOWITZ D. ROLES OF INSULIN AND GROWTH HORMONE, BASED ON STUDIES OF FOREARM METABOLISM IN MAN. Medicine (Baltimore). 1963 Nov;42:385-402.
- RABINOWITZ D, KLASSEN GA, ZIERLER KL. EFFECT OF HUMAN GROWTH HORMONE ON MUSCLE AND ADIPOSE TISSUE METABOLISM IN THE FOREARM OF MAN. J Clin Invest. 1965 Jan;44:51-61.
- Fineberg SE, Merimee TJ. Acute metabolic effects of human growth hormone. Diabetes. 1974 Jun;23(6):499-504.
- Appleby BS, Lu M, Bizzi A, et al. Iatrogenic Creutzfeldt-Jakob Disease from Commercial Cadaveric Human Growth Hormone. Emerging Infectious Diseases. 2013;19(4):682-684. doi:10.3201/eid1904.121504.
35.https://www.gene.com/media/press-releases/4235/1985-10-18/fda-approves-genentechs-drug-to-treat-ch
- Flodh H. Human growth hormone produced with recombinant DNA technology: development and production. Acta Paediatr Scand Suppl. 1986;325:1-9.
- Crist DM, Peake GT, Egan PA, Waters DL. Body composition response to exogenous GH during training in highly conditioned adults. J Appl Physiol (1985). 1988 Aug;65(2):579-84.
- Møller N, Copeland KC, Nair KS. Growth hormone effects on protein metabolism. Endocrinol Metab Clin North Am. 2007 Mar;36(1):89-100. Review.
- Argetsinger LS, Carter-Su C. Mechanism of signaling by growth hormone receptor. Physiol Rev. 1996 Oct;76(4):1089-107. Review.
- Hayashi AA, Proud CG. The rapid activation of protein synthesis by growth hormone requires signaling through mTOR. Am J Physiol Endocrinol Metab. 2007 Jun;292(6):E1647-55.
- Kostyo JL. Rapid effects of growth hormone on amino acid transport and protein synthesis. Ann N Y Acad Sci. 1968 Feb 5;148(2):389-407.
- Cameron CM, Kostyo JL, Adamafio NA, Brostedt P, Roos P, Skottner A, Forsman A, Fryklund L, Skoog B. The acute effects of growth hormone on amino acid transport and protein synthesis are due to its insulin-like action. Endocrinology. 1988 Feb;122(2):471-4.
- Vanderkuur JA, Butch ER, Waters SB, Pessin JE, Guan KL, Carter-Su C. Signaling molecules involved in coupling growth hormone receptor to mitogen-activated protein kinase activation. Endocrinology. 1997 Oct;138(10):4301-7.
- Costoya JA, Finidori J, Moutoussamy S, Seãris R, Devesa J, Arce VM. Activation of growth hormone receptor delivers an antiapoptotic signal: evidence for a role of Akt in this pathway. Endocrinology. 1999 Dec;140(12):5937-43.
- Copeland KC, Nair KS. Acute growth hormone effects on amino acid and lipid metabolism. J Clin Endocrinol Metab. 1994 May;78(5):1040-7.
- Umpleby AM, Boroujerdi MA, Brown PM, Carson ER, Sönksen PH. The effect of metabolic control on leucine metabolism in type 1 (insulin-dependent) diabetic patients. Diabetologia. 1986 Mar;29(3):131-41.
- Horber FF, Haymond MW. Human growth hormone prevents the protein catabolic side effects of prednisone in humans. J Clin Invest. 1990 Jul;86(1):265-72.
- Yarasheski KE, Campbell JA, Smith K, Rennie MJ, Holloszy JO, Bier DM. Effect of growth hormone and resistance exercise on muscle growth in young men. Am J Physiol. 1992 Mar;262(3 Pt 1):E261-7.
- Zachwieja JJ, Bier DM, Yarasheski KE. Growth hormone administration in older adults: effects on albumin synthesis. Am J Physiol. 1994 Jun;266(6 Pt 1):E840-4.
- Yarasheski KE, Zachwieja JJ, Campbell JA, Bier DM. Effect of growth hormone and resistance exercise on muscle growth and strength in older men. Am J Physiol. 1995 Feb;268(2 Pt 1):E268-76.
- Healy ML, Gibney J, Russell-Jones DL, Pentecost C, Croos P, Sönksen PH, Umpleby AM. High dose growth hormone exerts an anabolic effect at rest and during exercise in endurance-trained athletes. J Clin Endocrinol Metab. 2003 Nov;88(11):5221-6.
- Giannoulis MG, Jackson N, Shojaee-Moradie F, Nair KS, Sonksen PH, Martin FC, Umpleby AM. The effects of growth hormone and/or testosterone on whole body protein kinetics and skeletal muscle gene expression in healthy elderly men: a randomized controlled trial. J Clin Endocrinol Metab. 2008 Aug;93(8):3066-74.
- Fryburg DA, Gelfand RA, Barrett EJ. Growth hormone acutely stimulates forearm muscle protein synthesis in normal humans. Am J Physiol. 1991 Mar;260(3 Pt 1):E499-504.
- Fryburg DA, Louard RJ, Gerow KE, Gelfand RA, Barrett EJ. Growth hormone stimulates skeletal muscle protein synthesis and antagonizes insulin’s antiproteolytic action in humans. Diabetes. 1992 Apr;41(4):424-9.
- Fryburg DA, Barrett EJ. Growth hormone acutely stimulates skeletal muscle but not whole-body protein synthesis in humans. Metabolism. 1993 Sep;42(9):1223-7.
- Nørrelund H, Nair KS, Jørgensen JO, Christiansen JS, Møller N. The protein-retaining effects of growth hormone during fasting involve inhibition of muscle-protein breakdown. Diabetes. 2001 Jan;50(1):96-104.
- Manson JM, Wilmore DW. Positive nitrogen balance with human growth hormone and hypocaloric intravenous feeding. Surgery. 1986 Aug;100(2):188-97.
- Clemmons DR, Snyder DK, Williams R, Underwood LE. Growth hormone administration conserves lean body mass during dietary restriction in obese subjects. J Clin Endocrinol Metab. 1987 May;64(5):878-83.
- Snyder DK, Clemmons DR, Underwood LE. Treatment of obese, diet-restricted subjects with growth hormone for 11 weeks: effects on anabolism, lipolysis, and body composition. J Clin Endocrinol Metab. 1988 Jul;67(1):54-61.
- Tagliaferri M, Scacchi M, Pincelli AI, Berselli ME, Silvestri P, Montesano A, Ortolani S, Dubini A, Cavagnini F. Metabolic effects of biosynthetic growth hormone treatment in severely energy-restricted obese women. Int J Obes Relat Metab Disord. 1998 Sep;22(9):836-41.
- Nørrelund H, Børglum J, Jørgensen JO, Richelsen B, Møller N, Nair KS, Christiansen JS. Effects of growth hormone administration on protein dynamics andsubstrate metabolism during 4 weeks of dietary restriction in obese women. Clin Endocrinol (Oxf). 2000 Mar;52(3):305-12.
- Lundeberg S, Belfrage M, Wernerman J, von der Decken A, Thunell S, Vinnars E. Growth hormone improves muscle protein metabolism and whole body nitrogen economy in man during a hyponitrogenous diet. Metabolism. 1991 Mar;40(3):315-22
- Fryburg DA. Insulin-like growth factor I exerts growth hormone- and insulin-like actions on human muscle protein metabolism. Am J Physiol. 1994 Aug;267(2 Pt 1):E331-6.
- Russell-Jones DL, Umpleby AM, Hennessy TR, Bowes SB, Shojaee-Moradie F, Hopkins KD, Jackson NC, Kelly JM, Jones RH, Sönksen PH. Use of a leucine clamp to demonstrate that IGF-I actively stimulates protein synthesis in normal humans. Am J Physiol. 1994 Oct;267(4 Pt 1):E591-8.
- Jacob R, Hu X, Niederstock D, Hasan S, McNulty PH, Sherwin RS, Young LH. IGF-I stimulation of muscle protein synthesis in the awake rat: permissive role of insulin and amino acids. Am J Physiol. 1996 Jan;270(1 Pt 1):E60-6.
- Buijs MM, Romijn JA, Burggraaf J, De Kam ML, Cohen AF, Frölich M, Stellaard F, Meinders AE, Pijl H. Growth hormone blunts protein oxidation and promotes protein turnover to a similar extent in abdominally obese and normal-weight women. J Clin Endocrinol Metab. 2002 Dec;87(12):5668-74.
- Gibney J, Wolthers T, Johannsson G, Umpleby AM, Ho KK. Growth hormone and testosterone interact positively to enhance protein and energy metabolism in hypopituitary men. Am J Physiol Endocrinol Metab. 2005 Aug;289(2):E266-71.
- Le Roith D, Scavo L, Butler A. What is the role of circulating IGF-I? Trends Endocrinol Metab. 2001 Mar;12(2):48-52. Review.
- Mauras N, Haymond MW. Are the metabolic effects of GH and IGF-I separable? Growth Horm IGF Res. 2005 Feb;15(1):19-27. Review.
- Laron Z. Laron syndrome (primary growth hormone resistance or insensitivity): the personal experience 1958-2003. J Clin Endocrinol Metab. 2004 Mar;89(3):1031-44.
- Muhammad A, van der Lely AJ, Neggers SJ. Review of current and emerging treatment options in acromegaly. Neth J Med. 2015 Oct;73(8):362-7. Review.
- Lupu F, Terwilliger JD, Lee K, Segre GV, Efstratiadis A. Roles of growth hormone and insulin-like growth factor 1 in mouse postnatal growth. Dev Biol. 2001 Jan 1;229(1):141-62.
- Waters MJ. The growth hormone receptor. Growth Horm IGF Res. 2016 Jun;28:6-10.
- Laron Z, Ginsberg S, Webb M. Nonalcoholic fatty liver in patients with Laron syndrome and GH gene deletion – preliminary report. Growth Horm IGF Res. 2008 Oct;18(5):434-8.
- Sharara FI. Value of growth hormone in ovulation induction? Fertil Steril. 1996 Jun;65(6):1259-61.
- Kolibianakis EM, Venetis CA, Diedrich K, Tarlatzis BC, Griesinger G. Addition of growth hormone to gonadotrophins in ovarian stimulation of poor responders treated by in-vitro fertilization: a systematic review and meta-analysis. Hum Reprod Update. 2009 Nov-Dec;15(6):613-22.
- Russell SM, Spencer EM. Local injections of human or rat growth hormone or of purified human somatomedin-C stimulate unilateral tibial epiphyseal growth in hypophysectomized rats. Endocrinology. 1985 Jun;116(6):2563-7.
- Schlechter NL, Russell SM, Greenberg S, Spencer EM, Nicoll CS. A direct growth effect of growth hormone in rat hindlimb shown by arterial infusion. Am J Physiol. 1986 Mar;250(3 Pt 1):E231-5.
- Isaksson OG, Ohlsson C, Nilsson A, Isgaard J, Lindahl A. Regulation of cartilage growth by growth hormone and insulin-like growth factor I. Pediatr Nephrol. 1991 Jul;5(4):451-3. Review.
- Ohlsson C, Bengtsson BA, Isaksson OG, Andreassen TT, Slootweg MC. Growth hormone and bone. Endocr Rev. 1998 Feb;19(1):55-79. Review.
- Wang J, Zhou J, Cheng CM, Kopchick JJ, Bondy CA. Evidence supporting dual, IGF-I-independent and IGF-I-dependent, roles for GH in promoting longitudinal bone growth. J Endocrinol. 2004 Feb;180(2):247-55.
- Yakar S, Rosen CJ, Bouxsein ML, Sun H, Mejia W, Kawashima Y, Wu Y, Emerton K, Williams V, Jepsen K, Schaffler MB, Majeska RJ, Gavrilova O, Gutierrez M, Hwang D, Pennisi P, Frystyk J, Boisclair Y, Pintar J, Jasper H, Domene H, Cohen P, Clemmons D, LeRoith D. Serum complexes of insulin-like growth factor-1 modulate skeletal integrity and carbohydrate metabolism. FASEB J. 2009 Mar;23(3):709-19.
- Ohlsson C, Mohan S, Sjögren K, Tivesten A, Isgaard J, Isaksson O, Jansson JO, Svensson J. The role of liver-derived insulin-like growth factor-I. Endocr Rev. 2009 Aug;30(5):494-535.
- Sotiropoulos A, Ohanna M, Kedzia C, Menon RK, Kopchick JJ, Kelly PA, Pende M. Growth hormone promotes skeletal muscle cell fusion independent of insulin-like growth factor 1 up-regulation. Proc Natl Acad Sci U S A. 2006 May 9;103(19):7315-20.
- Wakelam MJ. The fusion of myoblasts. Biochem J. 1985 May 15;228(1):1-12. Review.
- Pfäffle RW, Blankenstein O, Wüller S, Kentrup H. Combined pituitary hormone deficiency: role of Pit-1 and Prop-1. Acta Paediatr Suppl. 1999 Dec;88(433):33-41. Review.
- Hemchand K, Anuradha K, Neeti S, Vaman K, Roland P, Werner B, Sharmila B. Entire prophet of Pit-1 (PROP-1) gene deletion in an Indian girl with combined pituitary hormone deficiencies. J Pediatr Endocrinol Metab. 2011;24(7-8):579-80.
- Waters MJ, Shang CA, Behncken SN, Tam SP, Li H, Shen B, Lobie PE. Growth hormone as a cytokine. Clin Exp Pharmacol Physiol. 1999 Oct;26(10):760-4. Review.
- Jansson JO, Edén S, Isaksson O. Sexual dimorphism in the control of growth hormone secretion. Endocr Rev. 1985 Spring;6(2):128-50. Review.
- Giustina A, Veldhuis JD. Pathophysiology of the neuroregulation of growth hormone secretion in experimental animals and the human. Endocr Rev. 1998 Dec;19(6):717-97. Review.
- Hartman ML, Faria AC, Vance ML, Johnson ML, Thorner MO, Veldhuis JD. Temporal structure of in vivo growth hormone secretory events in humans. Am J Physiol. 1991 Jan;260(1 Pt 1):E101-10.
- Takahashi Y, Kipnis DM, Daughaday WH. Growth hormone secretion during sleep. J Clin Invest. 1968 Sep;47(9):2079-90.
- Parker DC, Sassin JF, Mace JW, Gotlin RW, Rossman LG. Human growth hormone release during sleep: electroencephalographic correlation. J Clin Endocrinol Metab. 1969 Jun;29(6):871-4.
- Ho KY, Veldhuis JD, Johnson ML, Furlanetto R, Evans WS, Alberti KG, Thorner MO. Fasting enhances growth hormone secretion and amplifies the complex rhythms of growth hormone secretion in man. J Clin Invest. 1988 Apr;81(4):968-75.
- Jaffe CA, Ocampo-Lim B, Guo W, Krueger K, Sugahara I, DeMott-Friberg R, Bermann M, Barkan AL. Regulatory mechanisms of growth hormone secretion are sexually dimorphic. J Clin Invest. 1998 Jul 1;102(1):153-64.
- Jessup SK, Dimaraki EV, Symons KV, Barkan AL. Sexual dimorphism of growth hormone (GH) regulation in humans: endogenous GH-releasing hormone maintains basal GH in women but not in men. J Clin Endocrinol Metab. 2003 Oct;88(10):4776-80.
- Goldenberg N, Barkan A. Factors regulating growth hormone secretion in humans. Endocrinol Metab Clin North Am. 2007 Mar;36(1):37-55. Review.
- Müller EE, Locatelli V, Cocchi D. Neuroendocrine control of growth hormone secretion. Physiol Rev. 1999 Apr;79(2):511-607. Review.
- Murray RA, Maheshwari HG, Russell EJ, Baumann G. Pituitary hypoplasia in patients with a mutation in the growth hormone-releasing hormone receptor gene. AJNR Am J Neuroradiol. 2000 Apr;21(4):685-9.
- Murray PG, Higham CE, Clayton PE. 60 YEARS OF NEUROENDOCRINOLOGY: The hypothalamo-GH axis: the past 60 years. J Endocrinol. 2015 Aug;226(2):T123-40.
- Russell-Aulet M, Dimaraki EV, Jaffe CA, DeMott-Friberg R, Barkan AL. Aging-related growth hormone (GH) decrease is a selective hypothalamic GH-releasing hormone pulse amplitude mediated phenomenon. J Gerontol A Biol Sci Med Sci. 2001 Feb;56(2):M124-9
- Dimaraki EV, Jaffe CA, Demott-Friberg R, Russell-Aulet M, Bowers CY, Marbach P, Barkan AL. Generation of growth hormone pulsatility in women: evidence against somatostatin withdrawal as pulse initiator. Am J Physiol Endocrinol Metab. 2001 Mar;280(3):E489-95.
- Baumann G. Growth hormone heterogeneity: genes, isohormones, variants, and binding proteins. Endocr Rev. 1991 Nov;12(4):424-49. Review.
- Vijayakumar A, Novosyadlyy R, Wu Y, Yakar S, LeRoith D. Biological effects of growth hormone on carbohydrate and lipid metabolism. Growth Horm IGF Res. 2010 Feb;20(1):1-7. doi: 10.1016/j.ghir.2009.09.002. Epub 2009 Oct 1. Review.
- Herrington J, Carter-Su C. Signaling pathways activated by the growth hormone receptor. Trends Endocrinol Metab. 2001 Aug;12(6):252-7. Review.
- Baumann G. Growth hormone binding protein. The soluble growth hormone receptor. Minerva Endocrinol. 2002 Dec;27(4):265-76. Review.
- Bairoch A, Apweiler R. The SWISS-PROT protein sequence data bank and its new supplement TREMBL. Nucleic Acids Res. 1996 Jan 1;24(1):21-5.
- Kelly PA, Djiane J, Postel-Vinay MC, Edery M. The prolactin/growth hormone receptor family. Endocr Rev. 1991 Aug;12(3):235-51. Review.
- Vikman K, Carlsson B, Billig H, Edén S. Expression and regulation of growth hormone (GH) receptor messenger ribonucleic acid (mRNA) in rat adipose tissue, adipocytes, and adipocyte precursor cells: GH regulation of GH receptor mRNA. Endocrinology. 1991 Sep;129(3):1155-61.
- Zou L, Menon RK, Sperling MA. Induction of mRNAs for the growth hormone receptor gene during mouse 3T3-L1 preadipocyte differentiation. Metabolism. 1997 Jan;46(1):114-8.
- Leung KC, Waters MJ, Markus I, Baumbach WR, Ho KK. Insulin and insulin-like growth factor-I acutely inhibit surface translocation of growth hormone receptors in osteoblasts: a novel mechanism of growth hormone receptor regulation. Proc Natl Acad Sci U S A. 1997 Oct 14;94(21):11381-6.
- Birzniece V, Sata A, Ho KK. Growth hormone receptor modulators. Rev Endocr Metab Disord. 2009 Jun;10(2):145-56.
- Sawada T, Arai D, Jing X, Miyajima M, Frank SJ, Sakaguchi K. Molecular interactions of EphA4, growth hormone receptor, Janus kinase 2, and signal transducer and activator of transcription 5B. PLoS One. 2017 Jul 7;12(7):e0180785.
- Brooks AJ, Dai W, O’Mara ML, Abankwa D, Chhabra Y, Pelekanos RA, Gardon O, Tunny KA, Blucher KM, Morton CJ, Parker MW, Sierecki E, Gambin Y, Gomez GA, Alexandrov K, Wilson IA, Doxastakis M, Mark AE, Waters MJ. Mechanism of activation of protein kinase JAK2 by the growth hormone receptor. Science. 2014 May 16;344(6185):1249783.
- Liu Y, Berry PA, Zhang Y, Jiang J, Lobie PE, Paulmurugan R, Langenheim JF, Chen WY, Zinn KR, Frank SJ. Dynamic analysis of GH receptor conformational changes by split luciferase complementation. Mol Endocrinol. 2014 Nov;28(11):1807-19.
- Waters MJ, Brooks AJ. JAK2 activation by growth hormone and other cytokines. Biochem J. 2015 Feb 15;466(1):1-11.
- Brown RJ, Adams JJ, Pelekanos RA, Wan Y, McKinstry WJ, Palethorpe K, Seeber RM, Monks TA, Eidne KA, Parker MW, Waters MJ. Model for growth hormone receptor activation based on subunit rotation within a receptor dimer. Nat Struct Mol Biol. 2005 Sep;12(9):814-21. Epub 2005 Aug 21.
- Lanning NJ, Carter-Su C. Recent advances in growth hormone signaling. Rev Endocr Metab Disord. 2006 Dec;7(4):225-35. Review.
- Carter-Su C, Schwartz J, Smit LS. Molecular mechanism of growth hormone action. Annu Rev Physiol. 1996;58:187-207. Review.
- Brooks AJ, Waters MJ. The growth hormone receptor: mechanism of activation and clinical implications. Nat Rev Endocrinol. 2010 Sep;6(9):515-25.

Buon Giorno la mia domanda riguarda i reali effetti collaterali del GH quali ; diabete di tipo 2 ,resistenza insulinica proliferazione di leucemie edi altre patologie , ipotiroidismo per la capacità del gh di trasformare L ormone t4 in t 3 , grazie
"Mi piace""Mi piace"
La sua non è una domanda in realtà… Ha semplicemente mal elencato effetti potenziali con l’abuso di GH, sia diretti che indiretti… Il diabete di tipo 2 è una cronicizzazione dello stato di insulino resistenza…. e una sua cronicizzazione necessità di un abuso prolungato e accompagnato da stati di ipernutrizione i quali facilitano i processi di alterazione metabolica glucidico/lipidica … La proliferazione delle cellule tumorali è legata all’IGF-1 e alla presenza di mutazioni maligne pre-esistenti per lo più… Quindi non si limita alla Leucemia … L’ipotiroidismo è reversibile in breve tempo una volta cessato lo scorretto utilizzo del GH…in oltre è una condizione facilmente trattabile dal momento che gli utilizzatori inseriscono nel loro protocollo tiroidei sintetici in concomitanza con il peptide in questione…
"Mi piace""Mi piace"
Grazie , quindi per scongiurare tali effetti un dosaggio dai 2 / 4 ui al giorno per quanto tempo poi essere tenuto ?🤔
"Mi piace""Mi piace"
E’ questione di soggettività… Non per nulla vi è un numero non indifferente di soggetti che manifestano neuropatia già a 4UI/die e in tempi brevi… Questo le basti per realizzare quanto possa cambiare il risultato a seconda di dose e tempo in soggetti differenti… Le ricordo inoltre che questo sito è di informazione scientifica e non un servizio “domanda/risposta” al fine di ottenere indicazioni protocollari personalizzate…
"Mi piace""Mi piace"